BridgeBio berichtet �über positive Phase-3-Ergebnisse für orales Infigratinib mit den ersten statistisch signifikanten Verbesserungen der Körperproportionen bei Achondroplasie
- PROPEL 3 erreichte erfolgreich den primären Endpunkt der Veränderung der AHV gegenüber dem Ausgangswert in Woche 52 (p<0,0001)
- Die Veränderung der AHV gegenüber dem Ausgangswert war in Woche 52 gegenüber Placebo überlegen, mit einem durchschnittlichen Behandlungsunterschied von +2,10 cm/Jahr; der LS-Mittelwert betrug +1,74 cm/Jahr
- In einer vordefinierten explorativen Analyse des wichtigsten sekundären Endpunkts erzielte orales Infigratinib die erste statistisch signifikante Verbesserung der Körperproportionalität gegenüber Placebo bei Achondroplasie und zeigte einen LS-Mittelwert-Behandlungsunterschied von -0,05 (p<0,05) gegenüber Placebo bei Kindern unter 8 Jahren (>50 % der Teilnehmer)
- PROPEL 3 erreichte erfolgreich den wichtigsten sekundären Endpunkt der Veränderung des Height-Z-Scores (Referenzpopulation Achondroplasie) gegenüber dem Ausgangswert in Woche 52 (p<0,0001), mit einem LS-Mittelwert-Anstieg im Behandlungsarm von +0,41 SD
- Orales Infigratinib wurde gut vertragen, ohne Abbrüche oder schwerwiegende Nebenwirkungen im Zusammenhang mit dem Studienmedikament; 3 Fälle (4 %) von Hyperphosphatämie wurden als mild und vorübergehend eingestuft, kein einziger Fall erforderte eine Dosisreduktion oder einen Abbruch, und keine Nebenwirkungen im Zusammenhang mit der Hemmung von FGFR1 oder 2 (z. B. Netzhaut oder Hornhaut)
- NDA- und MAA-Einreichungen sind für die zweite Jahreshälfte 2026 für Achondroplasie geplant; orales Infigratinib ist die einzige in Entwicklung befindliche therapeutische Option für Achondroplasie, die von der FDA die Breakthrough Therapy Designation erhalten hat
- Angesichts der Stärke dieser Daten plant BridgeBio, die Entwicklung von oralem Infigratinib bei Hypochondroplasie zu beschleunigen und rekrutiert Teilnehmer für den Beobachtungslauf der Phase-3-Studie
PALO ALTO, Kalifornien, 12. Februar 2026 (GLOBE NEWSWIRE) -- BridgeBio Pharma, Inc. (Nasdaq: BBIO) (“BridgeBio” oder das “Unternehmen”), ein biopharmazeutisches Unternehmen, das sich auf die Entwicklung von Medikamenten für genetische Erkrankungen konzentriert, gab heute positive Topline-Ergebnisse aus PROPEL 3, der globalen Phase-3-Studie zu oralem Infigratinib bei Kindern mit Achondroplasie bekannt. BridgeBio wird am 12. Februar 2026 um 8:00 Uhr ET eine Investoren-Telefonkonferenz abhalten, um diese Ergebnisse zu diskutieren.
"Achondroplasie ist eine genetische Erkrankung, die durch FGFR3 verursacht wird und nicht nur die Körpergröße betrifft, sondern auch Auswirkungen auf die körperliche Funktion und Unabhängigkeit hat, die sich über die gesamte Lebensspanne auswirken können", sagte Ravi Savarirayan, M.D., Ph.D. vom Murdoch Children’s Research Institute in Melbourne, Australien, und globaler leitender Prüfarzt für PROPEL 3. "Infigratinib ist die erste orale Therapie, die gezielt FGFR3 adressiert und die zugrunde liegende Ursache der Achondroplasie direkt behandelt. In der bislang am breitesten untersuchten Altersgruppe zeigte orales Infigratinib die höchste und signifikanteste Verbesserung der jährlichen Wachstumsgeschwindigkeit sowie die erste statistisch signifikante Verbesserung der Körperproportionalität bei Kindern im Alter von 3 bis 8 Jahren, berichtet für jede zugelassene oder in Entwicklung befindliche Therapie für diese Erkrankung. Zusammengenommen unterstreichen diese best-in-class Ergebnisse das transformative Potenzial von Infigratinib, Aspekte der Achondroplasie über die lineare Körpergröße hinaus anzugehen, und dies mit einem oral verabreichten Produkt."
PROPEL 3 war eine globale, einjährige, 2:1 randomisierte, doppelblinde, placebokontrollierte klinische Studie zur Bewertung der Wirksamkeit und Sicherheit von Infigratinib bei Kindern mit Achondroplasie im Alter von 3 bis <18 Jahren mit offenen Wachstumsfugen. Wichtige Ergebnisse der Studie bis Woche 52 umfassen:
- Primärer Endpunkt:
- Veränderung der jährlichen Wachstumsgeschwindigkeit (AHV) gegenüber dem Ausgangswert war Placebo überlegen, mit einem LS-Mittelwert-Behandlungsunterschied von +1,74 cm/Jahr (p<0,0001) und einem durchschnittlichen Behandlungsunterschied von +2,10 cm/Jahr
- Sekundäre Endpunkte:
- Im Einklang mit dem primären Endpunkt zeigte der sekundäre Endpunkt der absoluten AHV in Woche 52 eine signifikante Verbesserung mit Infigratinib im Vergleich zu Placebo, wobei der Infigratinib-Arm den höchsten bislang in einer randomisierten Studie zur Achondroplasie berichteten LS-Mittelwert der absoluten AHV erreichte (5,96 cm/Jahr gegenüber 4,22 cm/Jahr unter Placebo)
- Die Veränderung des Height-Z-Scores (Referenzpopulation Achondroplasie) gegenüber dem Ausgangswert war Placebo überlegen, mit einem LS-Mittelwert-Behandlungsunterschied von +0,32 SD (p<0,0001), dem größten Unterschied, der je in einer randomisierten Studie zu Achondroplasie beobachtet wurde; die Veränderung des LS-Mittelwerts im Behandlungsarm gegenüber dem Ausgangswert betrug +0,41 SD, die größte Verbesserung, die jemals in einem Behandlungsarm einer randomisierten Studie zu Achondroplasie beobachtet wurde
- In einer vordefinierten explorativen Analyse (Kinder unter 8 Jahren; >50 % der Teilnehmer) des wichtigsten sekundären Endpunkts der Veränderung der Ober-zu-Unterkörper-Proportionalität in Woche 52 ist orales Infigratinib die erste therapeutische Option, die in einer randomisierten Studie zu Achondroplasie statistische Signifikanz gegenüber Placebo zeigt, mit einem LS-Mittelwert-Rückgang von -0,05 gegenüber Placebo (p<0,05)
- In der Gesamtpopulation erreichte Infigratinib einen LS-Mittelwert-Rückgang von -0,05, den größten Rückgang, der je in einem Behandlungsarm einer randomisierten Achondroplasie-Studie beobachtet wurde, mit einem günstigen LS-Behandlungsunterschied von -0,02 gegenüber Placebo in Woche 52 (p=0,1849)
- Infigratinib wurde gut vertragen, mit:
- Keinen abbrüchen im Zusammenhang mit dem Studienmedikament
- Keinen schwerwiegenden Nebenwirkungen im Zusammenhang mit dem Studienmedikament
- 3 Fällen (4 %) von Hyperphosphatämie, alle mild, vorübergehend, asymptomatisch und ohne Notwendigkeit einer Dosisreduktion oder eines Abbruchs
- Keine Nebenwirkungen im Zusammenhang mit Hemmung von FGFR1 oder FGFR2 (z. B. Netzhaut oder Hornhaut)
- Keine Nebenwirkungen im Zusammenhang mit CNP-Analoga: symptomatische Hypotonie, Reaktionen an der Injektionsstelle oder Hypertrichose
„Es besteht weiterhin ein erheblicher ungedeckter Bedarf an therapeutischen Optionen, die wirksam, praktisch und weniger invasiv für Kinder mit Achondroplasie sind“, sagte Daniela Rogoff, M.D., Chief Medical Officer, Skeletal Dysplasia von BridgeBio. „Die PROPEL-3-Daten unterstützen das Potenzial eines oralen Medikaments, das direkt auf die FGFR3-Überaktivität abzielt, um wichtige klinische Bedürfnisse zu adressieren und sich gleichzeitig in den Alltag von Familien einzufügen, die eine nicht-invasive Option suchen. Diese Ergebnisse stellen einen bedeutenden Fortschritt für diejenigen dar, die auf einen besseren Ansatz gewartet haben, und wir freuen uns darauf, dieses Programm in Richtung globaler Einreichung weiterzuentwickeln. Wir danken den Studienteilnehmern, ihren Familien, den Prüfern und dem Studienteam, die uns vertraut und uns auf diesem Weg begleitet haben.“
Basierend auf diesen Ergebnissen plant BridgeBio, sich mit den Zulassungsbehörden zu treffen, um die Einreichung eines New Drug Application (NDA) und einer Marketing Authorization Application (MAA) für Infigratinib in der zweiten Jahreshälfte 2026 zu besprechen, um eine Zulassung zu unterstützen. Das Unternehmen beabsichtigt außerdem, die Entwicklung von Infigratinib für Hypochondroplasie zu beschleunigen und rekrutiert Teilnehmer für den Beobachtungslauf der Phase-3-Studie. Zudem läuft eine klinische Studie mit Infigratinib für Neugeborene bis <3 Jahre bei Achondroplasie in der PROPEL Infant & Toddler-Studie. Infigratinib hat von der FDA für Achondroplasie die Breakthrough Designation sowie die Orphan Drug Designation (FDA & EMA), Fast Track Designation und Rare Pediatric Disease Designation erhalten.
„Die heutige Ankündigung stellt einen weiteren Meilenstein in der Achondroplasie-Forschung dar und erweitert, vorbehaltlich der behördlichen Prüfung, die verfügbaren Behandlungsoptionen um eine orale Therapieoption, die Einzelpersonen und Familien eine zusätzliche Wahlmöglichkeit bietet, wenn sie ihre Gesundheitsziele und Präferenzen abwägen“, sagte Michael Hughes, Vorsitzender des Biotech Industry Liaison Committee von Little People of America. „BridgeBios Engagement für den Austausch mit und das Lernen von der Kleinwuchs-Community spiegelt den Fokus wider, auf die gelebten Erfahrungen zu hören und unterschiedliche Prioritäten bei der Gestaltung der Forschungsbemühungen anzuerkennen. In diesem Zusammenhang ist die beobachtete Verbesserung der Körperproportionalität nach einem Jahr Behandlung in der PROPEL-3-Studie ein Ergebnis, das von Betroffenen und Familien als bedeutsam erachtet wird, möglicherweise für die körperliche Funktion relevant ist und weiterhin untersucht wird, um seine breitere Bedeutung zu verstehen.“
Informationen zur PROPEL Infant & Toddler-Studie (NCT07169279) finden sich auf clinicaltrials.gov. Informationen zu ACCEL, der Beobachtungsstudie des Unternehmens für Infigratinib in der Phase-3-Studie zu Hypochondroplasie (NCT06410976), sowie zu ACCEL 2/3, der Phase 2/3-Studie von BridgeBio zu Infigratinib bei Hypochondroplasie (NCT06873035), sind verfügbar. BridgeBio ist bestrebt, das Potenzial von Infigratinib hinsichtlich weitergehender medizinischer und funktionaler Auswirkungen von Achondroplasie, Hypochondroplasie und anderen skelettalen Dysplasien zu untersuchen, die einen erheblichen ungedeckten Bedarf für Familien darstellen.
Informationen zum Webcast
BridgeBio wird am 12. Februar 2026 um 8:00 Uhr ET eine Investorenkonferenz und einen gleichzeitigen Webcast abhalten, um die Ergebnisse der Phase-3-Studie PROPEL 3 zu Infigratinib bei Kindern mit Achondroplasie zu diskutieren. Ein Link zum Webcast ist auf der Event-Kalender-Seite der BridgeBio-Website verfügbar. Eine Aufzeichnung der Telefonkonferenz und des Webcasts wird auf der Website des Unternehmens archiviert und mindestens 30 Tage nach der Veranstaltung zugänglich sein.
Über Achondroplasie
Achondroplasie ist die häufigste Ursache für eine unverhältnismäßige Kleinwüchsigkeit und betrifft etwa 55.000 Menschen in den USA und der Europäischen Union (EU), darunter bis zu 10.000 Kinder und Jugendliche mit offenen Wachstumsfugen. Achondroplasie wirkt sich auf die allgemeine Gesundheit und Lebensqualität aus und führt zu medizinischen Komplikationen wie obstruktiver Schlafapnoe, Mittelohrdysfunktion, Kyphose und Spinalkanalstenose. Die Erkrankung wird einheitlich durch eine aktivierende Variante im FGFR3 verursacht.
Über BridgeBio Pharma, Inc.
BridgeBio existiert, um transformative Medikamente für genetische Erkrankungen zu entwickeln. Millionen Menschen weltweit leben mit genetischen Erkrankungen und haben keine Behandlungsoptionen, oft weil die Entwicklung von Medikamenten für kleine Patientengruppen kommerziell herausfordernd sein kann. Unser Ziel ist es, die Lücke zwischen Fortschritten in der Genetik und sinnvollen Medikamenten für unterversorgte Patientengruppen zu schließen. Unser dezentralisiertes Hub-and-Spoke-Modell ist auf Geschwindigkeit, Präzision und Skalierbarkeit ausgelegt. Autonome und befähigte Teams konzentrieren sich auf einzelne Erkrankungen, während ein zentrales Hub die klinischen, regulatorischen und kommerziellen Fähigkeiten bereitstellt, die erforderlich sind, um Innovationen auf den Markt zu bringen. Weitere Informationen finden Sie unter und folgen Sie uns auf , , , , , und .
Haftungsausschluss: Der Inhalt dieses Artikels gibt ausschließlich die Meinung des Autors wieder und repräsentiert nicht die Plattform in irgendeiner Form. Dieser Artikel ist nicht dazu gedacht, als Referenz für Investitionsentscheidungen zu dienen.
Das könnte Ihnen auch gefallen
Google hat Sundar Pichai kürzlich ein Vergütungspaket im Wert von 692 Millionen Dollar gewährt

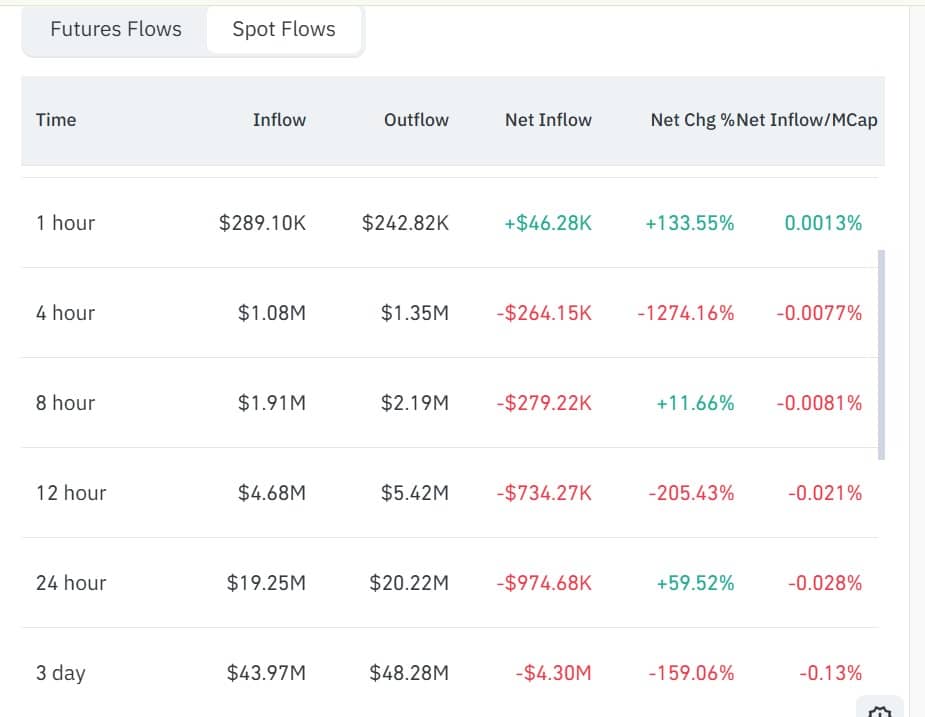
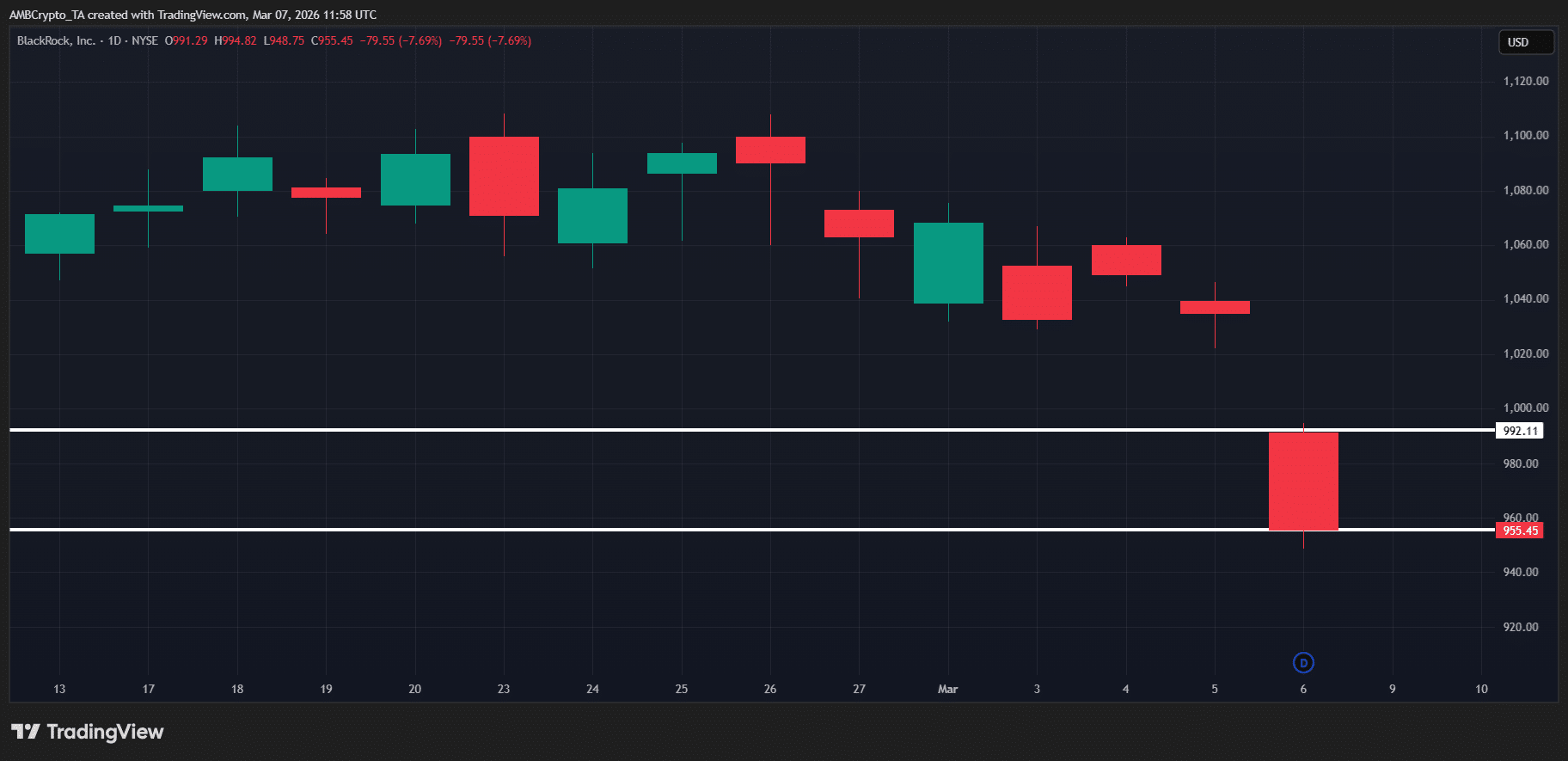
1,2 Milliarden Dollar Liquiditätswarnung – Wie BlackRock den Kryptomarkt ‚erschüttern‘ könnte
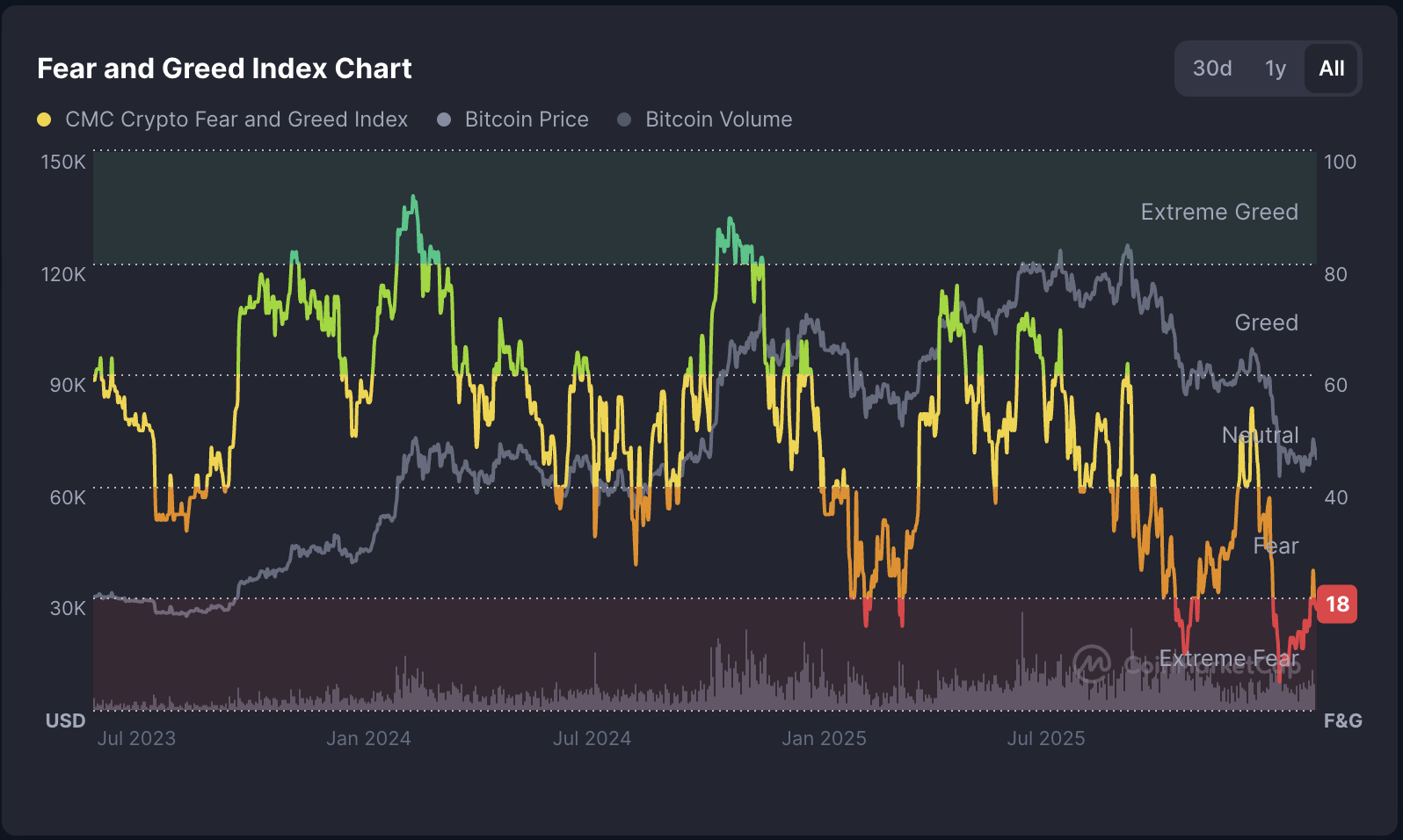
Der Crypto Fear and Greed Index fällt wieder auf das Niveau „extremer Angst“ zurück.
Bewertung, ob die $200-Unterstützung von Zcash nach einem 8%igen Rückgang von ZEC gefährdet ist