Europa genehmigt GSKs neue zweimal jährlich anzuwendende Asthmatherapie
Die Europäische Kommission hat am Dienstag GSK plc’s (NYSE:GSK) Exdensur (Depemokimab) für zwei Indikationen zugelassen, darunter:
- Als zusätzliche Erhaltungstherapie für schweres Asthma mit Typ-2-Entzündung, gekennzeichnet durch eine erhöhte Eosinophilenzahl im Blut bei Erwachsenen und Jugendlichen ab 12 Jahren, die trotz hochdosierter inhalativer Kortikosteroide plus eines weiteren Asthmakontrollers unzureichend kontrolliert sind.
- Als Zusatztherapie mit intranasalen Kortikosteroiden für erwachsene Patienten mit schwerer CRSwNP, bei denen eine Therapie mit systemischen Kortikosteroiden und/oder eine Operation keine ausreichende Krankheitskontrolle bietet.
Die Zulassung basiert auf Daten aus den Phase-3-Studien SWIFT und ANCHOR, die eine anhaltende Wirksamkeit mit einem halbjährlichen Dosierungsschema für Depemokimab zeigten.
Studiendaten
Jede der vier Studien erreichte ihre primären oder ko-primären Endpunkte mit statistisch signifikanten und klinisch relevanten Ergebnissen, wobei die Zugabe von Depemokimab zur Standardtherapie mit der Standardtherapie allein verglichen wurde.
Asthma betrifft mehr als 42 Millionen Menschen in Europa. Etwa 5-10 % der Patienten leiden an schwerem Asthma, wobei viele trotz Behandlung weiterhin Exazerbationen und eine verminderte Lebensqualität erfahren.
Darüber hinaus leiden Patienten mit CRSwNP unter belastenden täglichen Symptomen, und fast die Hälfte bleibt unkontrolliert.
Exdensur ist eine neuartige Therapie, die eine hohe Bindungsaffinität zu Interleukin-5 (IL-5) und hohe Potenz mit einer verlängerten Halbwertszeit kombiniert, was eine anhaltende Unterdrückung der krankheitstreibenden Typ-2-Entzündung mit einer halbjährlichen Dosierung ermöglicht.
In den SWIFT-Phase-3-Studien führte die Behandlung mit Depemokimab zu einer signifikanten Reduktion der jährlichen Asthma-Exazerbationsrate (Asthmaanfälle) um 58 % bzw. 48 % über 52 Wochen in SWIFT-1 bzw. SWIFT-2.
Bei einem sekundären Endpunkt aus SWIFT-1 und SWIFT-2 hatten Patienten, die mit Depemokimab behandelt wurden, numerisch weniger Exazerbationen, die einen Krankenhausaufenthalt und/oder Notaufnahmebesuch erforderten (1 % und 4 %) im Vergleich zu Placebo (8 % und 10 %).
Eine vordefinierte gepoolte Analyse der beiden Studien zeigte eine Reduktion von 72 % der jährlichen Rate klinisch signifikanter Exazerbationen, die einen Krankenhausaufenthalt und/oder einen Notaufnahmebesuch erforderten, über 52 Wochen für Depemokimab im Vergleich zu Placebo.
Zusätzlich führte in den ANCHOR-Phase-3-Studien die Behandlung mit Depemokimab zu einer Verbesserung (Reduktion) des Nasenpolypen-Scores (Skala: 0-8) gegenüber dem Ausgangswert nach 52 Wochen und auf der verbalen Skala zur nasalen Obstruktion in den Wochen 49-52.
Hintergrund
Im Dezember 2025 hat die U.S. Food and Drug Administration (FDA) Exdensur als Zusatz-Erhaltungstherapie bei schwerem Asthma mit eosinophilem Phänotyp bei Patienten ab 12 Jahren zugelassen.
Außerdem wurde Exdensur kürzlich im Vereinigten Königreich und in Japan für die Behandlung von schwerem Asthma und CRSwNP zugelassen.
Kursentwicklung: Die Aktie von GSK steigt laut Benzinga Pro Daten im vorbörslichen Handel am Dienstag zuletzt um 2,65 % auf 60,49 $.
Foto von JPC_PROD via Shutterstock
Haftungsausschluss: Der Inhalt dieses Artikels gibt ausschließlich die Meinung des Autors wieder und repräsentiert nicht die Plattform in irgendeiner Form. Dieser Artikel ist nicht dazu gedacht, als Referenz für Investitionsentscheidungen zu dienen.
Das könnte Ihnen auch gefallen
Straße von Hormus geschlossen, Inflation bei 5 %: Wird Bitcoin explodieren oder zusammenbrechen?

Der verlorene Bitcoin von Mt. Gox könnte zurückgewonnen werden, ehemaliger CEO schlägt seltenen Hard Fork vor

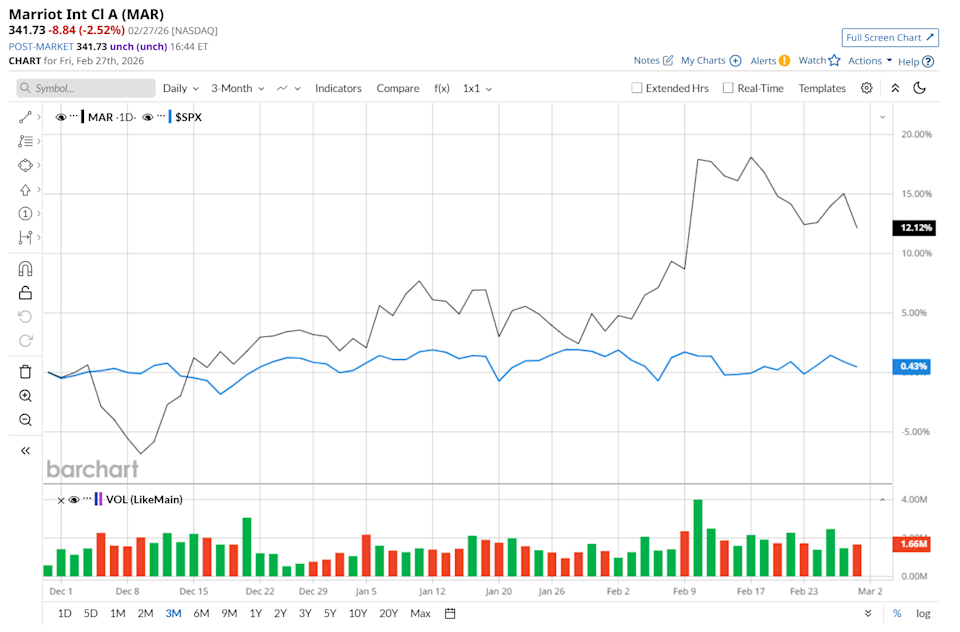
Schlägt die Aktie von Marriott International den S&P 500 Index?