Harrow kündigt Cash-Pay Direct-to-Prescriber PharmaPack Kits an
PharmaPack-Programm zur Erweiterung des Zugangs zu erschwinglichen, von der FDA zugelassenen Marken-Augenheiltherapien
NASHVILLE, Tenn., 17. Februar 2026 (GLOBE NEWSWIRE) -- Harrow (Nasdaq: HROW), ein führender Anbieter von Lösungen für das Management von Augenerkrankungen in Nordamerika, gab heute die Einführung eines neuen Direct-to-Prescriber (DTP) Cash-Pay-Angebots namens PharmaPack bekannt. Dieses Angebot erweitert das Engagement des Unternehmens, erschwingliche, von der FDA zugelassene Markenprodukte als Alternativen zu nicht zugelassenen, zusammengestellten Formulierungen bereitzustellen.
PharmaPack-Kits erweitern den Zugang zu von der FDA zugelassenen Augenheilprodukten für die Millionen Amerikaner, die jedes Jahr Infektionskontrolle sowie die Behandlung von Schmerzen und Entzündungen im Zusammenhang mit Kataraktoperationen benötigen. PharmaPack-Kits beseitigen zudem den administrativen Aufwand im Zusammenhang mit Versicherungen und reduzieren regulatorische sowie medizinisch-rechtliche Risiken, die bei nicht zugelassenen, zusammengestellten Produkten bestehen. Harrow bietet die folgenden PharmaPack-Kits zu erschwinglichen und vollständig transparenten Preisen an:
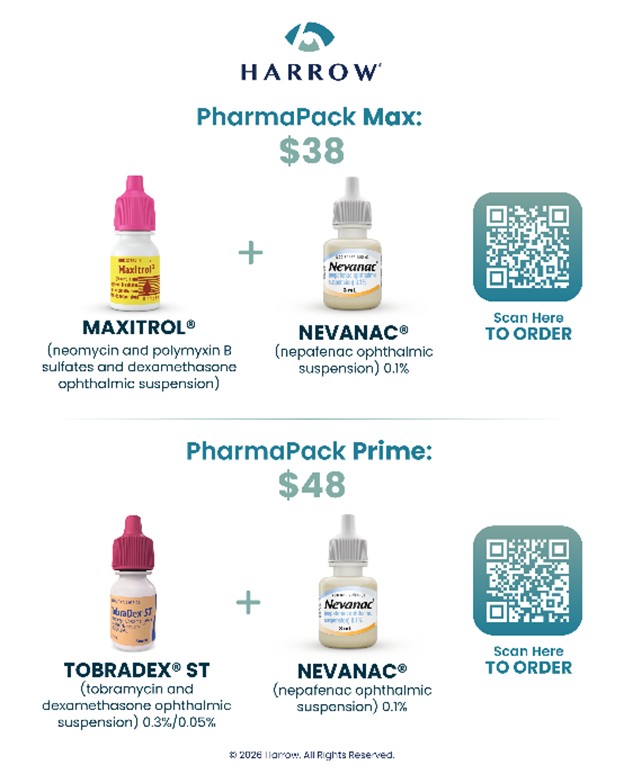
„Harrow‘s PharmaPack-Programm adressiert eine langjährige Herausforderung in der Augenheilkunde – Patienten FDA-zugelassene Therapien bereitzustellen, die sowohl zuverlässig als auch erschwinglich sind“, sagte Dr. Scott Spector. „Die Kombination aus bewährten Markenprodukten, Preistransparenz und diesen attraktiven Barzahlungs-Preisen ist ermutigend und unterstützt eine unkomplizierte Verschreibung sowie größeres Vertrauen bei der Berücksichtigung von FDA-zugelassenen Markenalternativen zu zusammengestellten Produkten. Aufgrund der Stärke dieses Angebots und seines Wertes habe ich PharmaPack Prime bereits für meine Patienten bestellt.“
„Der Zugang zu FDA-zugelassenen Therapien zu erschwinglichen und transparenten Preisen ist etwas, nach dem Optometristen gefragt haben“, sagte Dr. Maria Pribis. „PharmaPack hilft, diese Lücke zu schließen, indem hochwertige Markenprodukte im Alltag der Patientenversorgung besser zugänglich gemacht werden.“
So bestellen Sie:
PharmaPack-Kits werden zunächst in Kalifornien, Mississippi, Arkansas, Connecticut und Alabama verfügbar sein, mit Plänen für eine landesweite Ausweitung in den kommenden Wochen. Verschreiber können auf PharmaPack-Angebote vom Startbildschirm ihres Account-Dashboards aus zugreifen oder über die folgenden Links:
- PharmaPack Max
- PharmaPack Prime
Wenden Sie sich bei Fragen an Ihren Harrow- oder ImprimisRx-Vertreter oder senden Sie eine E-Mail an[email protected].
Über NEVANAC
ANWENDUNGSGEBIET UND VERWENDUNG
NEVANAC Augensuspension ist ein nichtsteroidales, entzündungshemmendes Prodrug, das zur Behandlung von Schmerzen und Entzündungen im Zusammenhang mit Kataraktoperationen angezeigt ist.
KONTRAINDIKATIONEN
Überempfindlichkeit gegen einen der Bestandteile der Formel oder gegen andere NSAIDs.
WARNHINWEISE & VORSICHTSMASSNAHMEN
- Verlängerte Blutungszeit: Bei einigen nichtsteroidalen Antirheumatika, einschließlich NEVANAC ®, besteht die Möglichkeit einer verlängerten Blutungszeit aufgrund einer Beeinträchtigung der Thrombozytenaggregation. Es gibt Berichte, dass topisch verabreichte nichtsteroidale Antirheumatika bei Augenoperationen zu verstärkten Blutungen des Augengewebes (einschließlich Hyphäma) führen können. Es wird empfohlen, NEVANAC®Augensuspension mit Vorsicht bei Patienten mit bekannter Blutungsneigung oder bei gleichzeitiger Einnahme anderer Medikamente, die die Blutungszeit verlängern können, anzuwenden.
- Verzögerte Heilung: Topische nichtsteroidale Antirheumatika (NSAIDs), einschließlich NEVANAC ®, können die Heilung verlangsamen oder verzögern. Topische Kortikosteroide sind ebenfalls dafür bekannt, die Heilung zu verzögern. Die gleichzeitige Anwendung von topischen NSAIDs und topischen Steroiden kann das Risiko von Heilungsproblemen erhöhen.
- Hornhauteffekte: Die Anwendung von topischen NSAIDs kann zu Keratitis führen. Bei einigen anfälligen Patienten kann die fortgesetzte Anwendung topischer NSAIDs zu Epithelabbau, Hornhautverdünnung, Hornhauterosion, Hornhautulkus oder Hornhautperforation führen. Diese Ereignisse können das Sehvermögen gefährden. Patienten mit Anzeichen eines Hornhautepithelabbaus sollten die Anwendung von topischen NSAIDs, einschließlich NEVANAC ®, sofort beenden und hinsichtlich der Hornhautgesundheit engmaschig überwacht werden.
Nach der Markteinführung wurde bei topischen NSAIDs berichtet, dass Patienten mit komplizierten Augenoperationen, Hornhautdenervation, Hornhautepitheldefekten, Diabetes mellitus, Erkrankungen der Augenoberfläche (z. B. Syndrom des trockenen Auges), rheumatoider Arthritis oder wiederholten Augenoperationen innerhalb kurzer Zeit ein erhöhtes Risiko für hornhautbezogene Nebenwirkungen haben, die das Sehvermögen gefährden können. Topische NSAIDs sollten bei diesen Patienten mit Vorsicht angewendet werden.
Nach der Markteinführung von topischen NSAIDs wurde ebenfalls berichtet, dass die Anwendung mehr als einen Tag vor der Operation oder länger als 14 Tage nach der Operation das Risiko und die Schwere hornhautbezogener Nebenwirkungen erhöhen kann.
- Kontaktlinsentragen: NEVANAC sollte nicht während des Tragens von Kontaktlinsen verabreicht werden.
NEBENWIRKUNGEN
Da klinische Studien unter sehr unterschiedlichen Bedingungen durchgeführt werden, können die in den klinischen Studien eines Medikaments beobachteten Nebenwirkungsraten nicht direkt mit denen eines anderen Medikaments verglichen werden und spiegeln möglicherweise nicht die in der Praxis beobachteten Raten wider.
Bitte beachten Sie weitere wichtige Sicherheitsinformationen im gesamten Text und die beiliegende vollständige Fachinformation.
Über TOBRADEX
ANWENDUNGSGEBIET UND VERWENDUNG
TOBRADEX ST (Tobramycin und Dexamethason Augensuspension) 0,3%/0,05% ist eine topische Kombination aus Antibiotikum und Kortikosteroid für steroidempfindliche entzündliche Augenerkrankungen, bei denen ein Kortikosteroid angezeigt ist und eine oberflächliche bakterielle Augeninfektion oder ein Risiko für eine bakterielle Augeninfektion besteht.
Wichtige Sicherheitsinformationen
KONTRAINDIKATIONEN:
Die meisten viralen Erkrankungen der Hornhaut und Bindehaut, einschließlich epithelialer Herpes-simplex-Keratitis (dendritische Keratitis), Vaccinia, Varizella, sowie bei mykobakteriellen Infektionen des Auges und Pilzerkrankungen der okulären Strukturen. Überempfindlichkeit gegen einen der Bestandteile des Medikaments.
WARNHINWEISE & VORSICHTSMASSNAHMEN:
- Erhöhung des Augeninnendrucks (IOP)— Eine längere Anwendung kann zu Glaukom mit Schädigung des Sehnervs sowie zu Beeinträchtigungen der Sehschärfe und des Gesichtsfeldes führen. Der IOP sollte überwacht werden.
- Aminoglykosid-Empfindlichkeit— Es kann zu einer Überempfindlichkeit gegen topisch verabreichte Aminoglykoside kommen.
- Katarakte— Es kann zur Bildung eines posterioren subkapsulären Katarakts kommen.
- Verzögerte Heilung— Kann die Heilung verzögern und die Inzidenz von Bleb-Bildungen erhöhen. Perforationen der Hornhaut oder Sklera sind aufgetreten. Spaltlampenbiomikroskopie und Fluoreszeinfärbung sollten durchgeführt werden.
- Bakterielle Infektionen— Kann die Immunantwort des Wirts unterdrücken und sekundäre okuläre Infektionen erhöhen. Bei akuten eitrigen Zuständen können Steroide Infektionen maskieren oder verschlimmern. Wenn sich die Symptome nach 2 Tagen nicht bessern, sollte der Patient erneut untersucht werden.
- Virale Infektionen— Die Anwendung bei Patienten mit Herpes-simplex-Vorgeschichte erfordert besondere Vorsicht. Der Verlauf und die Schwere vieler viraler Augenerkrankungen (einschließlich Herpes simplex) können verstärkt werden.
- Pilzinfektionen— Pilzinfektionen der Hornhaut können auftreten und sollten bei jeder anhaltenden Hornhautulzeration in Betracht gezogen werden.
- Verschwommenes Sehen— Nach der Anwendung von TOBRADEX ®ST kann das Sehvermögen vorübergehend verschwommen sein. Beim Bedienen von Maschinen oder Autofahren ist Vorsicht geboten.
- Kontaminationsrisiko— Die Tropferspitze der Flasche nicht mit einer Oberfläche in Berührung bringen, da dies den Inhalt kontaminieren kann.
- Kontaktlinsengebrauch— TOBRADEX ®ST enthält Benzalkoniumchlorid, ein antimikrobielles Konservierungsmittel, das von weichen Kontaktlinsen absorbiert werden kann. Kontaktlinsen sollten während der Anwendung von TOBRADEX®ST nicht getragen werden.
NEBENWIRKUNGEN:
- Die häufigsten Nebenwirkungen (<4%) von topischem, okularem Tobramycin sind Überempfindlichkeit und lokale okulare Toxizität, einschließlich Augenschmerzen, Juckreiz der Augenlider, Lidödem und Bindehautrötung.
- Die Reaktionen aufgrund der Steroidkomponente sind erhöhter IOP mit möglicher Schädigung des Sehnervs und Entwicklung von Glaukom, subkapsulärer Katarakt und beeinträchtigter Heilung.
- Das Auftreten von Sekundärinfektionen wurde beobachtet. Pilzinfektionen der Hornhaut können auftreten. Sekundäre bakterielle Augeninfektionen nach Unterdrückung der Immunantwort kommen ebenfalls vor.
- Nicht-okulare Nebenwirkungen (0,5 % bis 1 %) waren Kopfschmerzen und erhöhter Blutdruck.
Die folgenden zusätzlichen Nebenwirkungen wurden für die einzelnen Komponenten berichtet:
- Aminoglykoside: Neurotoxizität, Ototoxizität und Nephrotoxizität wurden bei Patienten beobachtet, die systemisch Aminoglykosid-Therapie erhielten. Aminoglykoside können bei Patienten mit bekannten oder vermuteten neuromuskulären Erkrankungen wie Myasthenia gravis oder Parkinson-Krankheit aufgrund ihres potenziellen Effekts auf die neuromuskuläre Funktion Muskelschwäche verstärken.
- Dexamethason: Cushing-Syndrom und Nebennierensuppression können nach Anwendung von Dexamethason über die angegebenen Dosierungsanweisungen hinaus bei dafür prädisponierten Patienten, einschließlich Kindern und Patienten, die mit CYP3A4-Inhibitoren behandelt werden, auftreten.
Bitte beachten Sie die vollständige Fachinformation.
Über MAXITROL
ANWENDUNGSGEBIETE UND VERWENDUNG:
- Für steroidempfindliche entzündliche Augenerkrankungen, bei denen ein Kortikosteroid angezeigt ist und eine bakterielle Infektion oder das Risiko einer bakteriellen Augeninfektion besteht.
- Okuläre Steroide sind angezeigt bei Entzündungen der tarsalen und bulbaren Bindehaut, der Hornhaut und des vorderen Augenabschnitts, wenn das inhärente Risiko der Steroidanwendung bei bestimmten infektiösen Konjunktivitiden akzeptiert wird, um eine Verringerung von Ödem und Entzündung zu erreichen. Sie sind ebenfalls angezeigt bei chronischer anteriorer Uveitis und Hornhautverletzungen durch Chemikalien, Strahlung oder thermische Verbrennungen oder das Eindringen von Fremdkörpern.
- Die Anwendung eines Kombinationspräparats mit einem antiinfektiven Bestandteil ist angezeigt, wenn das Infektionsrisiko hoch ist oder erwartet wird, dass potenziell gefährliche Mengen von Bakterien im Auge vorhanden sein werden.
- Das spezielle Antiinfektivum in diesem Produkt ist gegen die folgenden häufigen bakteriellen Augenpathogene wirksam: Staphylococcus aureus, Escherichia coli, Haemophilus influenzae, Klebsiella/Enterobacter-Arten, Neisseria-Arten und Pseudomonas aeruginosa.
- Dieses Produkt bietet keinen ausreichenden Schutz gegen: Serratia marcescens und Streptokokken, einschließlich Streptococcus pneumoniae.
KONTRAINDIKATIONEN:
Maxitrol ist kontraindiziert bei Patienten mit epithelialer Herpes-simplex-Keratitis (dendritische Keratitis), Vaccinia, Varizella sowie vielen anderen viralen Infektionen der Hornhaut und Bindehaut, mykobakteriellen Infektionen des Auges, Pilzerkrankungen der okulären Strukturen sowie Überempfindlichkeit gegen einen Bestandteil des Medikaments.
WARNHINWEISE:
- Maxitrol darf nicht injiziert oder intraokular verabreicht werden.
- Die Anwendung von okulären Steroiden kann die Krankheitsdauer verlängern und die Schwere vieler viraler Augeninfektionen verstärken. Eine längere Anwendung kann zu Glaukom mit Schädigung des Sehnervs, Beeinträchtigungen der Sehschärfe und des Gesichtsfeldes sowie zur Bildung eines posterioren subkapsulären Katarakts führen. Eine Langzeitbehandlung kann die Immunantwort unterdrücken und damit das Risiko einer sekundären okulären Infektion erhöhen.
- Wenn dieses Produkt 10 Tage oder länger angewendet wird, sollte der Augeninnendruck routinemäßig kontrolliert werden.
- Neomycinsulfat kann zu kutaner Sensibilisierung führen. Bei einigen Patienten kann eine Empfindlichkeit gegenüber topisch verabreichten Aminoglykosiden wie Neomycin auftreten. Entwickelt sich eine Überempfindlichkeit, sollte die Behandlung abgebrochen werden. Es kann zu Kreuzempfindlichkeiten gegenüber anderen Aminoglykosiden kommen und Patienten, die gegenüber topischem Neomycin sensibilisiert sind, können auch gegenüber anderen topischen und/oder systemischen Aminoglykosiden empfindlich sein.
VORSICHTSMASSNAHMEN:
Wenn Entzündungen oder Schmerzen länger als 48 Stunden anhalten oder sich verschlimmern, sollte der Patient die Anwendung abbrechen und einen Arzt konsultieren. Patienten sollten darauf hingewiesen werden, dass ihr Sehvermögen nach der Anwendung von Maxitrol vorübergehend verschwommen sein kann.
NEBENWIRKUNGEN:
Die am häufigsten auftretenden Reaktionen auf den antiinfektiven Bestandteil sind allergische Sensibilisierungen. Die Nebenwirkungen des Steroidbestandteils sind: Erhöhung des Augeninnendrucks (IOP) mit möglicher Entwicklung von Glaukom und selten Schädigung des Sehnervs; Bildung eines posterioren subkapsulären Katarakts; sowie verzögerte Wundheilung.
Die vollständige Fachinformation zu Maxitrol finden Sie unter Maxitrol Fachinformation.
Über Harrow
Harrow, Inc. (Nasdaq: HROW) ist ein führender Anbieter von Lösungen für das Management von Augenerkrankungen in Nordamerika und bietet ein umfassendes Portfolio an Produkten, die Erkrankungen sowohl des vorderen als auch des hinteren Augenabschnitts adressieren, wie z. B. trockene Augenkrankheit, feuchte (oder neovaskuläre) altersbedingte Makuladegeneration, Katarakte, refraktive Fehler, Glaukom sowie eine Vielzahl anderer Erkrankungen der Augenoberfläche und Netzhauterkrankungen. Harrow wurde mit dem Ziel gegründet, sichere, wirksame, zugängliche und erschwingliche Medikamente bereitzustellen, die die Therapietreue der Patienten verbessern und zu besseren klinischen Ergebnissen führen. Weitere Informationen über Harrow finden Sie auf Harrow und verbinden Sie sich mit uns auf LinkedIn.
Vorausschauende Aussagen
Haftungsausschluss: Der Inhalt dieses Artikels gibt ausschließlich die Meinung des Autors wieder und repräsentiert nicht die Plattform in irgendeiner Form. Dieser Artikel ist nicht dazu gedacht, als Referenz für Investitionsentscheidungen zu dienen.
Das könnte Ihnen auch gefallen
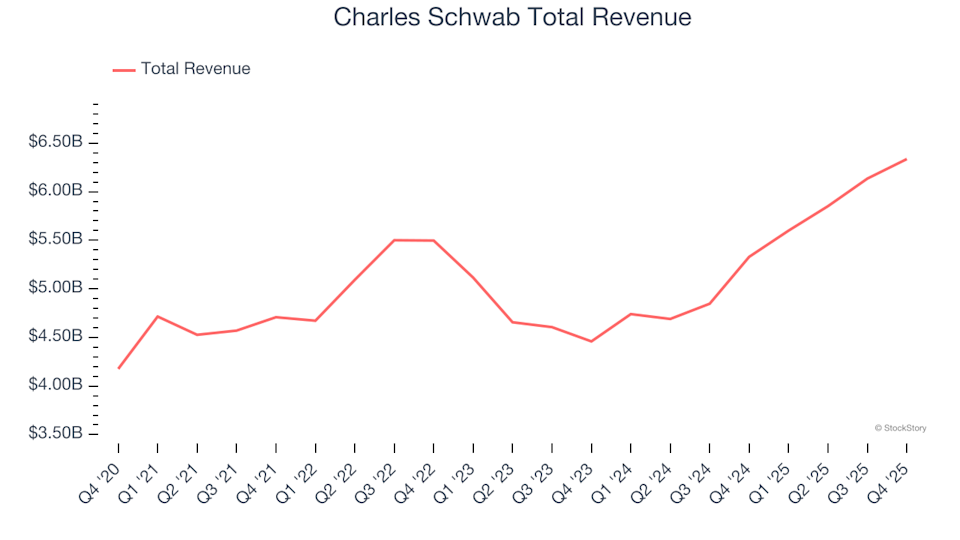
DOJ's Behauptung von 7,58 $ Gebühr: Die Einnahmequelle des Monopols
Zacks startet Berichterstattung über MUEL und vergibt eine neutrale Bewertung
Liebe Costco-Aktionäre, merken Sie sich das Datum vor: 5

