Cytokinetics gibt die Zulassung von MYQORZO (aficamten) durch die Europäische Kommission zur Behandlung von Erwachsenen mit symptomatischer obstruktiver hypertropher Kardiomyopathie bekannt
Zulassung der Europäischen Kommission basierend auf den Ergebnissen der SEQUOIA-HCM-Studie
Erste europäische Markteinführung in Deutschland im 2. Quartal 2026 erwartet
SOUTH SAN FRANCISCO, Kalifornien, 17. Februar 2026 (GLOBE NEWSWIRE) -- Cytokinetics, Incorporated (Nasdaq: CYTK) gab heute bekannt, dass die Europäische Kommission (EC) MYQORZO® (aficamten), Tabletten zu 5 mg, 10 mg, 15 mg und 20 mg für die Behandlung der symptomatischen (New York Heart Association, NYHA, Klasse II-III) obstruktiven hypertrophen Kardiomyopathie (oHCM) bei erwachsenen Patienten zugelassen hat. MYQORZO ist ein allosterischer und reversibler Inhibitor der kardialen Myosin-Motoraktivität. Bei Patienten mit oHCM führt die Myosin-Inhibition durch MYQORZO zu einer verringerten kardialen Kontraktilität und folglich zur Reduktion der linksventrikulären Ausflusstraktobstruktion (LVOT).
„Die Zulassung von MYQORZO in der Europäischen Union ist ein wichtiger Meilenstein, um dieses Medikament mehr Patienten mit obstruktiver HCM weltweit zugänglich zu machen“, sagte Robert I. Blum, Präsident und Chief Executive Officer von Cytokinetics. „Wir freuen uns, dass das europäische Label den Behandlern die Flexibilität gibt, je nach Schweregrad der LVOT-Obstruktion des Patienten entweder mit 5 mg oder 10 mg zu beginnen. Wir freuen uns darauf, MYQORZO in Europa verfügbar zu machen, beginnend mit unserer ersten Einführung in Deutschland im zweiten Quartal dieses Jahres.“
„Die Myosin-Inhibition etabliert sich als wichtige Therapie, die das Leben von Patienten mit hypertropher obstruktiver Kardiomyopathie verbessern kann. Die Zulassung von aficamten durch die Europäische Kommission bringt eine weitere Behandlungsoption in unsere klinische Praxis und erlaubt mehr Flexibilität, um mehr Patienten zu erreichen“, sagte Prof. Benjamin Meder, FESC, Lehrstuhlinhaber für Precision Digital Health, Leiter des Instituts für Kardiomyopathien Heidelberg und stellvertretender Ärztlicher Direktor, Abteilung für Kardiologie, Angiologie und Pneumologie, Universitätsklinikum Heidelberg.
„Die obstruktive HCM kann das Leben der Patienten erheblich beeinträchtigen und zwingt sie häufig zu schwierigen Entscheidungen basierend auf ihren Symptomen und ihrem Befinden“, sagte Emil Tsenov, Gründer und Geschäftsführer der HCM Patient Foundation. „Die Zulassung von MYQORZO in der Europäischen Union bringt Hoffnung für Patienten und stellt einen bedeutenden Fortschritt für die HCM-Gemeinschaft dar.“
Die EC-Zulassung folgt auf die positive Stellungnahme des Ausschusses für Humanarzneimittel (CHMP) der Europäischen Arzneimittel-Agentur (EMA), der die Marktzulassung von MYQORZO für die Behandlung der symptomatischen (NYHA Klasse II-III) oHCM bei erwachsenen Patienten in der Europäischen Union (EU) empfohlen hat.
MYQORZO wurde von der U.S. Food and Drug Administration (FDA) zur Behandlung von Erwachsenen mit symptomatischer oHCM zur Verbesserung der funktionellen Kapazität und der Symptome zugelassen, sowie von der China National Medical Products Administration (NMPA) zur Behandlung von Erwachsenen mit NYHA Klasse II-III oHCM, um die körperliche Leistungsfähigkeit und Symptome zu verbessern.
Die Zusammenfassung der Produkteigenschaften für MYQORZO ist auf der EMA-Website verfügbar.
Über SEQUOIA-HCM
Die EC-Zulassung basiert auf den positiven Ergebnissen der wegweisenden Phase-3-Studie SEQUOIA-HCM, veröffentlicht im New England Journal of Medicine, die eine robuste Wirksamkeit, Sicherheit und klinisch bedeutsame Vorteile hinsichtlich Symptomen, körperlicher Leistungsfähigkeit, Hämodynamik und Biomarker-Endpunkten zeigte. Die Ergebnisse der SEQUOIA-HCM-Studie zeigten, dass die Behandlung mit MYQORZO über 24 Wochen die körperliche Leistungsfähigkeit im Vergleich zu Placebo signifikant verbesserte, wobei die maximale Sauerstoffaufnahme (pVO
Während der 24-wöchigen Behandlungsperiode erlebten 3,5% der Patienten in der Behandlungsgruppe eine reversible, dosisabhängige Reduktion der linksventrikulären Ejektionsfraktion (LVEF) auf < 50% (Median 47%; Spanne 34% bis 49%). Ein Patient in der Behandlungsgruppe hatte eine asymptomatische LVEF < 40%. Reduktionen der LVEF auf < 50% erforderten keinen Therapieabbruch und waren nicht mit klinischer Herzinsuffizienz verbunden.
Die am häufigsten berichteten Nebenwirkungen unter MYQORZO waren Schwindel (4,2%), systolische Dysfunktion, definiert als LVEF < 50% (3,5%), Palpitationen (7%) und Hypertonie (7,7%).
Über MYQORZO® (aficamten)
MYQORZO® (aficamten) ist ein kardialer Myosin-Inhibitor, der in den USA, China und der Europäischen Union für die Behandlung der symptomatischen obstruktiven hypertrophen Kardiomyopathie (oHCM) zugelassen ist. Bei Patienten mit HCM führt die Myosin-Inhibition durch MYQORZO zu einer verringerten kardialen Kontraktilität und folglich zu einer Reduktion der linksventrikulären Ausflusstraktobstruktion (LVOT). MYQORZO wurde entwickelt, um eine vorhersehbare Expositions-Wirkungs-Beziehung, einen raschen Wirkbeginn und Reversibilität zu erreichen.
Aficamten wird zudem in der klinischen Studie ACACIA-HCM, einer Phase-3-Studie bei Patienten mit nicht-obstruktiver HCM (nHCM), und CEDAR-HCM, einer pädiatrischen Population mit oHCM, untersucht. Aficamten gilt in keiner dieser Patientengruppen als sicher oder wirksam. Darüber hinaus wird aficamten in FOREST-HCM, einer offenen Verlängerungsstudie, untersucht.
Über hypertrophe Kardiomyopathie
Die hypertrophe Kardiomyopathie (HCM) ist eine Erkrankung, bei der der Herzmuskel ungewöhnlich verdickt ist. HCM kann obstruktiv sein, wenn das verdickte Muskelgewebe den Blutfluss blockiert, oder nicht-obstruktiv, wenn der Blutfluss nicht blockiert ist, aber die Herzfunktion dennoch beeinträchtigt wird. Bei der obstruktiven HCM führt die Verdickung des Herzmuskels dazu, dass das Innere des linken Ventrikels kleiner, steifer und weniger in der Lage ist, sich zu entspannen und mit Blut zu füllen. Letztendlich wird durch die HCM die Pumpfunktion des Herzens eingeschränkt, was zu einer verringerten körperlichen Leistungsfähigkeit und einer Vielzahl von Symptomen führt.
HCM ist die häufigste monogen vererbte kardiovaskuläre Erkrankung und betrifft laut den Richtlinien der Europäischen Gesellschaft für Kardiologie etwa 1 von 500 Europäern.
Menschen mit HCM haben ein hohes Risiko, auch kardiovaskuläre Komplikationen wie Vorhofflimmern, Schlaganfall und Mitralklappenerkrankungen zu entwickeln.
Über Cytokinetics
Cytokinetics ist ein spezialisiertes kardiovaskuläres Biopharmaunternehmen, das auf mehr als 25 Jahre bahnbrechender wissenschaftlicher Innovationen in der Muskelbiologie aufbaut und eine Pipeline potenzieller neuer Medikamente für Patienten mit Erkrankungen der Herzmuskelfunktion vorantreibt. Cytokinetics’ MYQORZO™ (aficamten) ist ein kardialer Myosin-Inhibitor, der in den USA, Europa und China für die Behandlung von Erwachsenen mit symptomatischer obstruktiver hypertropher Kardiomyopathie (oHCM) zugelassen ist. Aficamten wird außerdem für die potenzielle Behandlung der nicht-obstruktiven HCM erforscht. Cytokinetics entwickelt auch omecamtiv mecarbil, einen experimentellen kardialen Myosin-Aktivator zur potenziellen Behandlung von Patienten mit Herzinsuffizienz mit stark reduzierter Auswurffraktion, sowie ulacamten, einen experimentellen kardialen Myosin-Inhibitor zur potenziellen Behandlung von Herzinsuffizienz mit erhaltener Auswurffraktion, und setzt die präklinische Forschung und Entwicklung in der Muskelbiologie fort.
CYTOKINETICS
MYQORZO™ ist eine Marke von Cytokinetics in den USA und eine eingetragene Marke in der Europäischen Union.
Quellen
- Maron, MS, et al. Aficamten für symptomatische obstruktive hypertrophe Kardiomyopathie. N Engl J Med. doi:10.1056/NEJMoa2401424
- Hartman JJ, Hwee DT, Roebrt-Paganin J, et al. Aficamten ist ein kleinmolekularer kardialer Myosin-Inhibitor zur Behandlung der hypertrophen Kardiomyopathie. Nat Cardiovasc Res. 2024;3(8) :1003-1016. doi:10.1038/s44161-024-00505-0
- ESC Leitlinien für die klinische Praxis. ESC Europäische Gesellschaft für Kardiologie. Abgerufen am 23. Juli 2025.
- Butzner M, et al. Epidemiologie der hypertrophen Kardiomyopathie in den Vereinigten Staaten von 2016 bis 2023. JACC Adv. 2026. 2026;5(2):102552. doi:10.1016/j.jacadv.2025.102552
- Gersh, B.J., Maron, B.J., Bonow, R.O., Dearani, J.A., Fifer, M.A., Link, M.S., et al. 2011 ACCF/AHA-Leitlinien für Diagnose und Behandlung der hypertrophen Kardiomyopathie. Ein Bericht der American College of Cardiology Foundation/American Heart Association Task Force on practice guidelines. Journal of the American College of Cardiology and Circulation, 58, e212-260.
- Hong Y, Su WW, Li X. Risikofaktoren für den plötzlichen Herztod bei hypertropher Kardiomyopathie. Current Opinion in Cardiology. 2022 Jan 1;37(1):15-21
Kontakt:
Cytokinetics
Diane Weiser
Senior Vice President, Corporate Affairs
(415) 290-7757
Haftungsausschluss: Der Inhalt dieses Artikels gibt ausschließlich die Meinung des Autors wieder und repräsentiert nicht die Plattform in irgendeiner Form. Dieser Artikel ist nicht dazu gedacht, als Referenz für Investitionsentscheidungen zu dienen.
Das könnte Ihnen auch gefallen
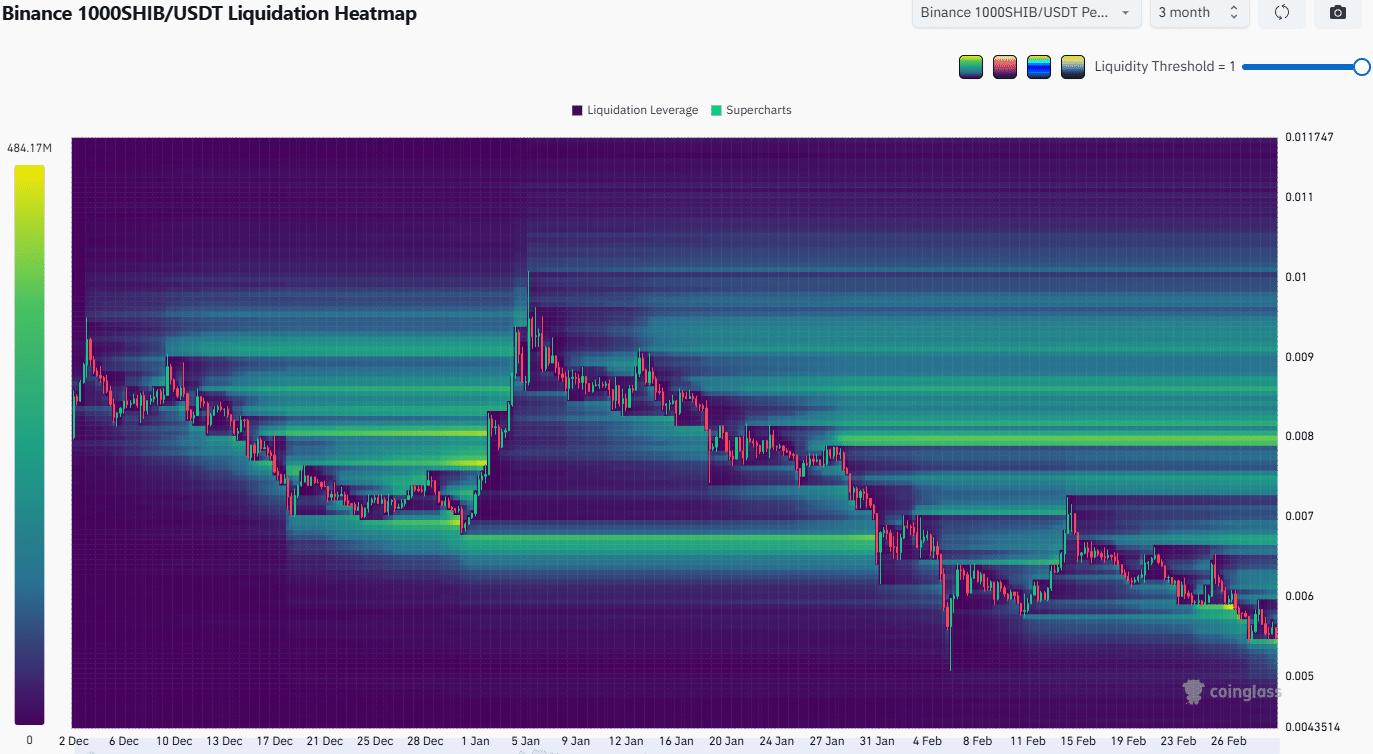
Shiba Inu-Bullen suchen nach einer Verkaufsmöglichkeit: Ist DAS der Moment?
Gates Capital investiert 150 Mio. $ in TIC: Bedeutende Investorenentscheidung oder cleverer Marktindikator?