Die US-amerikanische Food and Drug Administration (FDA) akzeptiert Tevas neuen Arzneimittelzulassungsantrag (NDA) für Olanzapin-Depotinjektion mit verlängerter Wirkstofffreisetzung (TEV-'749) zur einmal monatlichen Behandlung von Schizophrenie bei Erwachsenen.
- Olanzapin-Langzeitinjektion (LAI) Suspension (TEV-'749) hat das Potenzial, die Wirksamkeit von Olanzapin in einer einmal monatlichen, subkutanen Formulierung anzubieten 1
- Im Falle einer Zulassung könnte TEV-'749 dazu beitragen, einen bedeutenden ungedeckten Bedarf bei den verfügbaren Behandlungsoptionen für Schizophrenie zu adressieren indem der Mangel an praktikablen langwirksamen Olanzapin-Formulierungen behoben wird 1
- Teva verpflichtet sich, diese innovative Behandlungsoption weiterzuentwickeln und seine differenzierte LAI-Produktreihe sowie seine wissenschaftliche Führungsrolle bei komplexen neurologischen Erkrankungen im Rahmen seiner Pivot to Growth-Strategie weiter auszubauen
PARSIPPANY, N.J. und TEL AVIV, Israel und PARIS, 20. Februar 2026 (GLOBE NEWSWIRE) -- Teva Pharmaceuticals, eine US-Tochtergesellschaft von Teva Pharmaceutical Industries Ltd. (NYSE und TASE: TEVA), und Medincell (Euronext: MEDCL) gaben heute bekannt, dass die US-amerikanische Food and Drug Administration (FDA) ihren New Drug Application (NDA) für die Olanzapin-Depot-Injektionssuspension (TEV-'749) zur Behandlung von Schizophrenie bei Erwachsenen angenommen hat. TEV-'749 wurde entwickelt, um die Therapietreue in der realen Welt zu verbessern und Patienten dabei zu unterstützen, langfristige Stabilität zu bewahren, mit dem Ziel, eine entscheidende Behandlungslücke für Menschen mit Schizophrenie zu schließen.
Derzeit gibt es keine langwirksame Olanzapin-Formulierung ohne von der FDA vorgeschriebenes Risk Evaluation and Mitigation Strategy (REMS), das eine Verabreichung in einer zertifizierten Gesundheitseinrichtung und eine 3-stündige Überwachungszeit nach der Injektion vorschreibt. In der Phase-3-SOLARIS-Studie zeigte TEV-'749, verabreicht als einmal monatliche subkutane Injektion, ein Wirksamkeits- und Sicherheitsprofil, das mit derzeit verfügbaren Olanzapin-Formulierungen übereinstimmt, und zeigte keinen Hinweis auf die Notwendigkeit einer Überwachung nach der Injektion.
„Therapietreue bleibt eine große Herausforderung und ein ungedeckter Bedarf für Menschen mit Schizophrenie, einschließlich vieler, die auf orale Formen von Olanzapin angewiesen sind. TEV-'749, unser untersuchter subkutan verabreichter Olanzapin LAI, hat das Potenzial, Stabilität zu bieten, indem die bewährte Wirksamkeit und Sicherheit von Olanzapin als einmal monatliche Behandlung genutzt wird“, sagte Eric Hughes, MD, PhD, Executive Vice President, Global R&D und Chief Medical Officer bei Teva. „Zu lange hat das Fehlen einer praktikablen langwirksamen Olanzapin-Formulierung die verfügbaren Optionen für diese Menschen eingeschränkt, und wir freuen uns auf die Zusammenarbeit mit der FDA bei der Prüfung des NDA für TEV-'749, um diese Versorgungslücke zu schließen.“
„Täglich eingenommenes Olanzapin ist eines der am häufigsten verschriebenen Antipsychotika für Menschen mit Schizophrenie, und diese langwirksame Formulierung könnte besser in ihr Leben passen“, sagte Christophe Douat, CEO von Medincell. „Mit zunehmender Erfahrung mit langwirksamen Injektionen werden diese immer mehr als wichtige Behandlungsoption bei schweren psychiatrischen Erkrankungen anerkannt. Die potenzielle Reichweite einer praktischen langwirksamen Option ist erheblich.“
Das NDA für TEV-'749 basiert auf Ergebnissen der Phase-3-SOLARIS-Studie, einschließlich der Ergebnisse der Woche 56, die Wirksamkeit, Sicherheit und Verträglichkeit bei Teilnehmern im Alter von 18 bis 64 Jahren mit Schizophrenie untersuchte.
TEV-'749 ist eine in der Erprobung befindliche einmal monatlich subkutan zu verabreichende LAI des atypischen Antipsychotikums der zweiten Generation Olanzapin. Es ist derzeit von keiner Zulassungsbehörde für irgendeine Anwendung zugelassen.
TEV-'749 nutzt SteadyTeq™, eine von Medincell patentierte Copolymer-Technologie, die eine kontrollierte, stetige und anhaltende Freisetzung von Olanzapin ermöglicht.
Über die Studie zur subkutanen Olanzapin-Depot-Injektion (SOLARIS)
SOLARIS ist eine multinationale, multizentrische, randomisierte, doppelblinde, parallele Gruppen-, placebokontrollierte Studie zur Bewertung der Wirksamkeit, Sicherheit und Verträglichkeit der Olanzapin-Depot-Injektionssuspension zur subkutanen Anwendung als Behandlung bei Patienten (Alter 18-64 Jahre) mit Schizophrenie.
Über Schizophrenie
Schizophrenie ist eine chronische, fortschreitende und stark beeinträchtigende psychische Störung, die das Denken, Fühlen und Handeln beeinflusst.
Über Teva
Teva Pharmaceutical Industries Ltd. (NYSE und TASE: TEVA) wandelt sich zu einem führenden innovativen biopharmazeutischen Unternehmen, ermöglicht durch ein Weltklasse-Generikageschäft. Seit über 120 Jahren ist Tevas Engagement für bessere Gesundheit ungebrochen. Von Innovationen in den Bereichen Neurowissenschaften und Immunologie bis hin zur Bereitstellung komplexer Generika, Biosimilars und Apothekenmarken weltweit widmet sich Teva der Erfüllung der Patientenbedürfnisse, heute und in Zukunft. Bei Teva stehen wir alle für eine bessere Gesundheit ein. Erfahren Sie mehr darüber, wie, unter
Warnhinweis zu zukunftsgerichteten Aussagen
- Daten liegen vor. Parsippany, NJ: Teva Neuroscience, Inc.
- Substance Abuse and Mental Health Services Administration. Schizophrenie. . Zugriff im Februar 2026.
- Velligan DI, Rao S. Die Epidemiologie und globale Belastung durch Schizophrenie. J Clin Psychiatry. 2023;84(1):MS21078COM5.
- Wander C. (2020). Schizophrenie: Möglichkeiten zur Verbesserung der Ergebnisse und zur Reduzierung der wirtschaftlichen Belastung durch Managed Care. The Am J Manag Care. 26(3 Suppl), S62–S68.
- Emsley, R., & Kilian, S. (2018). Wirksamkeit und Sicherheitsprofil von Paliperidon-Palmitat-Injektionen bei der Behandlung von Patienten mit Schizophrenie: eine evidenzbasierte Übersicht. Neuropsychiatric Dis. Treat., 14, 205–223.
- Emsley, R., Chiliza, B., Asmal, L. et al. (2013) Die Natur des Rückfalls bei Schizophrenie. BMC Psychiatry 13, 50.
- Andreasen, N. C., et al. (2013). Rückfalldauer, Behandlungsintensität und Gewebeverlust im Gehirn bei Schizophrenie: eine prospektive longitudinale MRT-Studie. The Am J Psychiatry, 170(6), 609–615.
Presseanfragen Teva:
[email protected]
Teva Investor Relations Anfragen
Über Medincell
Medincell ist ein biopharmazeutisches Lizenzunternehmen in der klinischen und kommerziellen Phase, das langwirksame injizierbare Arzneimittel in zahlreichen Therapiegebieten entwickelt. Unsere innovativen Behandlungen sollen die Einhaltung medizinischer Verschreibungen gewährleisten, die Wirksamkeit und Zugänglichkeit von Medikamenten verbessern und deren ökologischen Fußabdruck verringern. Sie kombinieren pharmazeutische Wirkstoffe mit unserer proprietären BEPO®-Technologie, die die Abgabe eines Wirkstoffs auf therapeutischem Niveau für mehrere Tage, Wochen oder Monate nach einer subkutanen oder lokalen Injektion eines nur wenige Millimeter großen, vollständig resorbierbaren Depots steuert. Die erste auf BEPO®-Technologie basierende Behandlung, die zur Behandlung von Schizophrenie bestimmt ist, wurde im April 2023 von der FDA zugelassen und wird nun in den Vereinigten Staaten von Teva unter dem Namen UZEDY® (BEPO®-Technologie ist an Teva unter dem Namen SteadyTeq™ lizenziert) vertrieben. Wir arbeiten mit führenden Pharmaunternehmen und Stiftungen zusammen, um die globale Gesundheit durch neue Behandlungsoptionen zu verbessern. Mit Sitz in Montpellier beschäftigt Medincell derzeit mehr als 140 Mitarbeiter aus mehr als 25 verschiedenen Nationen.
Haftungsausschluss: Der Inhalt dieses Artikels gibt ausschließlich die Meinung des Autors wieder und repräsentiert nicht die Plattform in irgendeiner Form. Dieser Artikel ist nicht dazu gedacht, als Referenz für Investitionsentscheidungen zu dienen.
Das könnte Ihnen auch gefallen
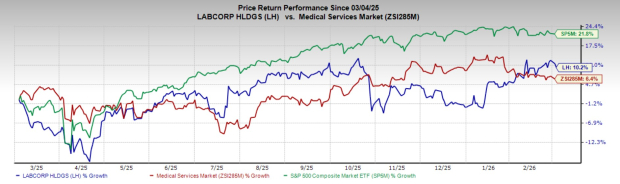
Ist jetzt ein idealer Zeitpunkt, um Labcorp-Aktien in Ihr Anlageportfolio aufzunehmen?
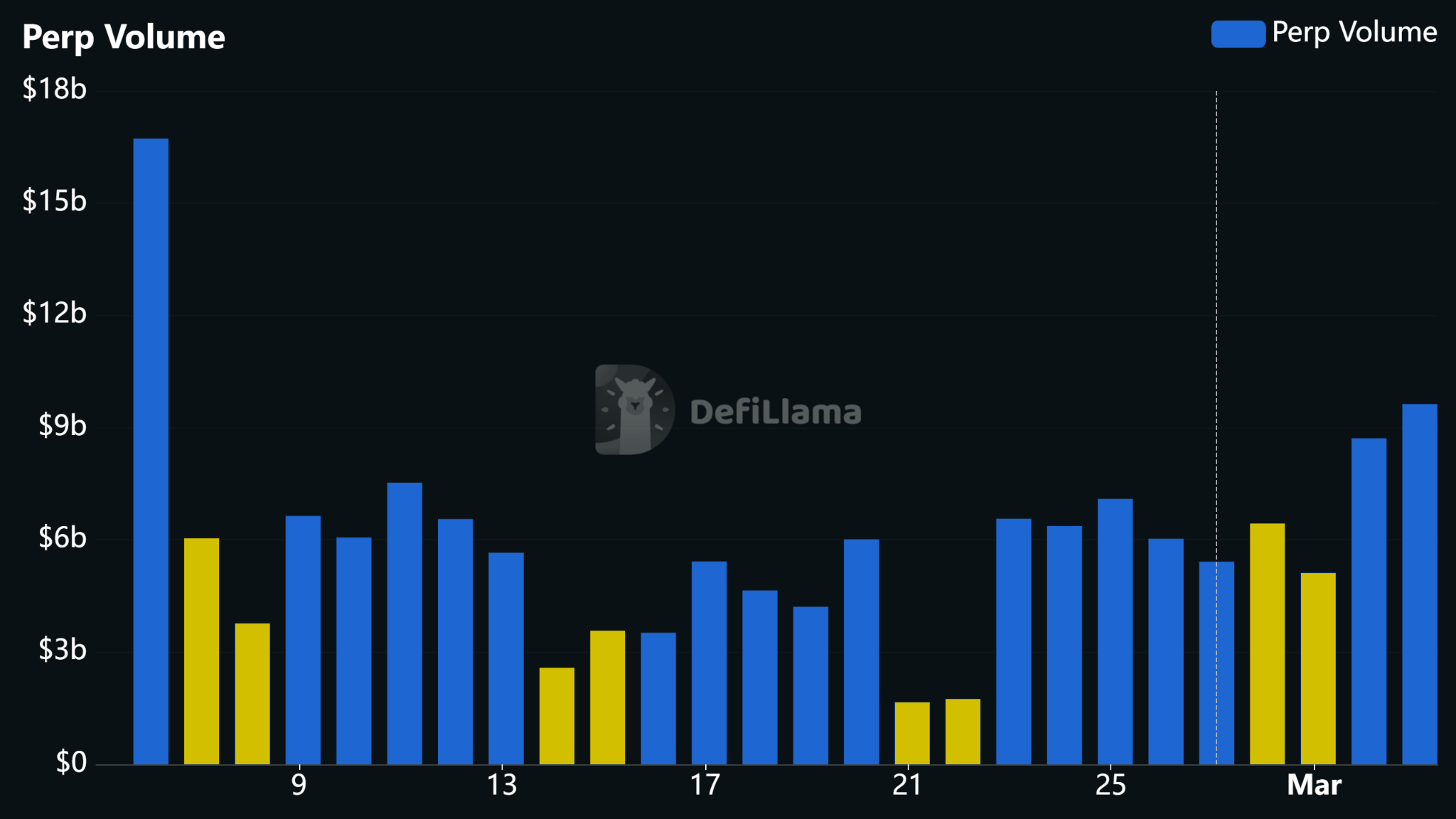
Bitcoin ist ein Echtzeit-Stimmungsbarometer für kriegerische Wochenenden
Ethereum steht vor der 2.100-Dollar-Herausforderung: Untersuchung von Akkumulations- und Widerstandsdynamiken
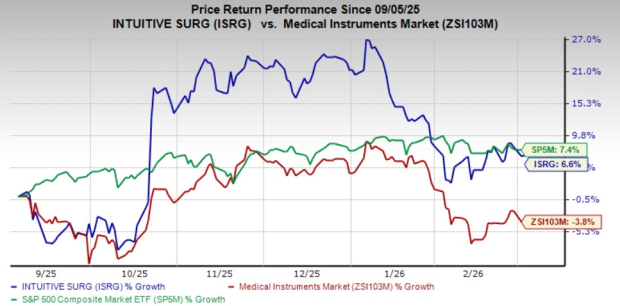
Intuitive Surgical erweitert seine Direktgeschäfte in ganz Europa