Das bevorstehende FDA-Urteil zu NeuroPace bezüglich IGE gilt als entscheidender Wendepunkt für Marktwachstum und Bewertungsänderung
NeuroPace: Zwei bedeutende Katalysatoren stehen bereit, um den Markt für das RNS-System zu erweitern
NeuroPace positioniert sich für ein erhebliches kurzfristiges Wachstum durch zwei Schlüsselinvestitionen, die den Markt für sein RNS-System deutlich vergrößern könnten. Der erste ist ein regulatorischer Antrag, der bereits eingereicht wurde, während der zweite eine neue Technologieplattform betrifft, die derzeit entwickelt wird.
Der unmittelbarste Katalysator ist das Premarket Approval Supplement (PMA-S), das im November 2025 bei der FDA eingereicht wurde. Dieser Antrag zielt darauf ab, die zugelassene Verwendung des RNS-Systems auf Patienten mit medikamentenresistenter idiopathischer generalisierter Epilepsie (IGE) zu erweitern, die generalisierte tonisch-klonische (GTC) Anfälle erleben. Der Antrag wird durch vielversprechende vorläufige Ergebnisse der 18-monatigen NAUTILUS-Studie unterstützt, die eine mediane Reduktion der GTC-Anfälle um 77% bei dieser schwierigen Patientengruppe zeigte. Bemerkenswert ist, dass diesen Betroffenen derzeit keine zugelassenen alternativen Therapien zur Verfügung stehen. Die FDA hat dieser Einreichung die Breakthrough Device Designation verliehen, was die Überprüfung beschleunigen könnte. Nach den aktuellen Richtlinien wird eine Entscheidung innerhalb von etwa 180 Tagen erwartet, was dieses Ereignis zu einem bedeutenden kurzfristigen Meilenstein macht.
Volatility Expansion Long-Only Strategie: Backtest-Zusammenfassung
- Einstiegssignal: Kaufe NEURO, wenn ATR(14) seinen 60-Tage-Simple Moving Average um mindestens 20% übersteigt.
- Ausstiegskriterien: Verkauf, wenn ATR(14) unter seinen 60-Tage-SMA fällt, nach 20 Handelstagen oder wenn Take-Profit (+8%) oder Stop-Loss (−4%) erreicht werden.
- Backtest-Zeitraum: Letzte 2 Jahre
Hauptergebnisse
- Gesamtrendite: 3.02%
- Jährliche Rendite: 2.15%
- Maximaler Drawdown: 15.46%
- Profit-Loss-Verhältnis: 1.8
- Gesamtanzahl Trades: 14
- Gewinn-Trades: 4
- Verlust-Trades: 6
- Gewinnrate: 28.57%
- Durchschnittliche Haltezeit: 6.21 Tage
- Maximal aufeinanderfolgende Verluste: 6
- Durchschnittlicher Gewinn pro Gewinn: 4.26%
- Durchschnittlicher Verlust pro Verlust: 2.21%
- Größter Einzelgewinn: 9.93%
- Größter Einzelnverlust: 5.11%
Parallel zu diesen regulatorischen Bemühungen entwickelt NeuroPace SeizureID™, eine künstliche Intelligenz-Plattform zur Analyse von intrakraniellen EEG (iEEG)-Daten, die vom RNS-System erfasst werden. Diese Technologie soll komplexe Hirnwellenaufzeichnungen in verwertbare Erkenntnisse umwandeln, wodurch Ärzte bessere Anfallsmuster erkennen und die Therapie individuell anpassen können. Obwohl SeizureID noch kein regulatorischer Antrag ist, stellt es eine strategische Maßnahme dar, um die klinische Nutzbarkeit und Anpassungsfähigkeit des RNS-Systems zu erhöhen, was zu besseren Patientenergebnissen und effizienterer Versorgung führen könnte. Erste Demonstrationen dieses KI-gestützten Werkzeugs finden bereits statt.
Gemeinsam bilden diese beiden Initiativen eine umfassende Wachstumsstrategie: Das IGE PMA-S soll eine neue, bislang unterversorgte Patientengruppe erschließen, während SeizureID darauf abzielt, die Erfahrungen und Ergebnisse für bestehende Nutzer zu verbessern. Sollten beide Initiativen erfolgreich sein, könnten sie die Nachfrage und die Verbreitung des RNS-Systems maßgeblich steigern.
Marktwachstumspotenzial und Wettbewerbsvorteil
Das PMA-S für IGE adressiert ein großes Segment des Epilepsiemarktes mit hohem Bedarf. Patienten mit medikamentenresistenter idiopathischer generalisierter Epilepsie und GTC-Anfällen leiden unter einer schwerwiegenden Erkrankung ohne zugelassene alternative Behandlungsmöglichkeiten. Dies bietet NeuroPace eine beträchtliche Gelegenheit, dessen RNS-System derzeit das einzige von der FDA zugelassene responsive Neurostimulationsgerät ist und dem Unternehmen einen klaren Vorteil als First Mover verschafft. Bei Zulassung wäre es die einzige speziell für diese Patientengruppe empfohlene Neuromodulationstherapie.
Diese regulatorischen Bestrebungen werden durch solide klinische Evidenz untermauert. Die vorläufigen 18-monatigen NAUTILUS-Studienergebnisse zeigten eine mediane Reduktion der GTC-Anfälle um 77%, ein starkes Wirksamkeitssignal, das die Verbreitung fördern könnte. Die Breakthrough Device Designation unterstreicht das potenzielle Gewicht und kann den Überprüfungsprozess beschleunigen.
Über die IGE-Indikation hinaus schafft NeuroPace mit seiner SeizureID™ KI-Plattform einen Wettbewerbsvorteil. Durch die Umwandlung von iEEG-Daten in klinische Erkenntnisse hilft dieses Werkzeug Ärzten, die Therapie zu optimieren und die Behandlungsergebnisse zu verbessern. Zudem entsteht ein wertvolles Datenökosystem, welches zukünftige regulatorische Einreichungen unterstützen und die Bindung der Ärzte vertiefen kann.
In Bezug auf die Konkurrenz bestehen zwar andere Neuromodulations-Therapien, jedoch sticht das RNS-System von NeuroPace als einziges von der FDA zugelassenes responsives Neurostimulationsgerät hervor. Seine Echtzeitüberwachung und adaptive Reaktion auf Gehirnaktivität differenzieren es von anderen Geräten. Die aktive Beteiligung des Unternehmens an bedeutenden wissenschaftlichen Konferenzen, darunter über 80 Präsentationen beim AES-Treffen, unterstreicht seine Führungsrolle in klinischer Forschung und Innovation.
Letztlich positionieren diese Katalysatoren NeuroPace so, dass es einen bedeutenden, bislang unterversorgten Markt erschließen und gleichzeitig den Wert des bestehenden Kundenstamms steigern kann. Die Kombination aus regulatorischer Führung und proprietärer KI-Technologie schafft die Voraussetzungen für anhaltendes Wachstum, das für Konkurrenten schwer zu erreichen ist.
Finanzielle Aussichten und Bewertungsüberlegungen
Die IGE-Chance stellt eine potenziell transformative Entwicklung dar, die NeuroPace’s Weg zur Rentabilität beschleunigen und die Wachstumsstory untermauern könnte. Das Kerngeschäft des Unternehmens läuft bereits gut, der Umsatz durch RNS stieg im Q4 2025 im Jahresvergleich um 26% und die Bruttomarge liegt fast bei 80%. Das Management rechnet für 2026 mit weiterem Wachstum von 20% bis 22% beim Kernumsatz mit RNS, ohne jeglichen Beitrag durch die IGE-Indikation. Dies markiert einen hohen Ausgangspunkt und macht die IGE-Erweiterung zu einem bedeutenden Potenzial, nicht zu einem moderaten Zusatz.
Obwohl es schwierig ist, die Umsatzwirkungen präzise abzuschätzen, ist der Zielmarkt groß und unterversorgt. Die Zulassung der IGE-Indikation würde das adressierbare Marktvolumen des RNS-Systems direkt erweitern. Aktuelle Aktienbewertungen mit einem Forward KGV von -15,8 und einem Kurs-Umsatz-Verhältnis von 4,8 spiegeln Erwartungen an erhebliches zukünftiges Wachstum wider, implizieren aber auch Risiken, falls der Katalysator ausbleibt.
Die Situation bleibt taktisch geprägt. Die Entscheidung der FDA, die für Mitte 2026 erwartet wird, stellt einen Wendepunkt dar, der die Wachstumsrichtung des Unternehmens drastisch verändern könnte. Ein positives Ergebnis würde wahrscheinlich die aktuelle Bewertung stützen, indem eine neue, bedeutende Umsatzquelle zu einem bereits starken Geschäft hinzukommt. Die Aktie reagiert empfindlich auf solche Entwicklungen, stieg in den letzten 120 Tagen um 45,9%, trotz eines jüngsten Rückgangs um 6,3%, was zeigt, dass der Markt bereits Unsicherheiten berücksichtigt.
Zusammenfassend könnte der IGE-Katalysator einen Wendepunkt für NeuroPace markieren und das Unternehmen auf dem Weg zu positivem Cash Flow und Rentabilität voranbringen. Für Investoren ergibt sich ein klares Risiko-Rendite-Profil: Die Erwartungen sind hoch, ein positives Urteil könnte die Strategie zur Markterweiterung bestätigen und eine Neubewertung der Aktie auslösen.
Wesentliche Katalysatoren, Risiken und Überwachungsaspekte
Die kurzfristige Perspektive konzentriert sich auf ein einziges, folgenreiches Ereignis: die Entscheidung der FDA bezüglich des IGE PMA-S. Etwa 180 Tage nach dem Antrag im November 2025 wird ein Urteil bis Mitte 2026 erwartet, was diesen Katalysator klar zeitlich definiert. Eine positive Entscheidung würde die klinischen Daten bestätigen, Zugang zu einem großen, bisher unterversorgten Markt eröffnen und vermutlich eine Neubewertung der Aktie auslösen. Eine negative oder verzögerte Entscheidung wäre hingegen ein signifikanter Rückschlag und würde eine Neubewertung der Wachstumsaussichten des Unternehmens erforderlich machen.
Das Haupt-Risiko besteht in den Ergebnissen der klinischen Studie. Zwar erreichte die NAUTILUS-Studie den primären Sicherheitsendpunkt, aber sie erreichte keine statistische Signifikanz für den primären Effektivitätsendpunkt in der gesamten Studienpopulation. Während eine Subgruppenanalyse eine signifikante Reaktion zeigte, bringen die Gesamtergebnisse regulatorische Unsicherheiten mit sich. Die Interpretation dieser Resultate durch die FDA ist entscheidend, und Investoren sollten die Entwicklungen in den Gesprächen des Unternehmens mit der Behörde zum regulatorischen Fahrplan verfolgen.
Neben der FDA-Entscheidung sind zwei weitere Meilensteine zu beobachten. Erstens ist die fortlaufende Umsetzung im Kerngeschäft des Unternehmens entscheidend. Das Management plant für 2026 ein Wachstum von 20% bis 22% beim RNS-Umsatz aus bestehenden Indikationen. Gute Quartalsergebnisse könnten negative Nachrichten zum IGE-Antrag abfedern. Zweitens sollte die regulatorische oder kommerzielle Entwicklung der SeizureID™ KI-Plattform, die der FDA bereits vorgelegt wurde, im Auge behalten werden. Fortschritte hier könnten den Wert des RNS-Ökosystems weiter unterstreichen.
Zusammengefasst steht NeuroPace vor einem klaren, taktischen Szenario. Der IGE-Katalysator ist ein binäres Ereignis mit festgelegtem Zeitplan. Das Hauptrisiko ist die fehlende statistische Signifikanz des primären Wirksamkeitsendpunkts in der Gesamtheit der Studienteilnehmer, was die FDA dazu veranlassen könnte, den Antrag zu verschieben oder abzulehnen. Vorläufig ist die Entwicklung des Unternehmens eng an die Entscheidung der Behörde gebunden, die für Mitte 2026 erwartet wird.
Haftungsausschluss: Der Inhalt dieses Artikels gibt ausschließlich die Meinung des Autors wieder und repräsentiert nicht die Plattform in irgendeiner Form. Dieser Artikel ist nicht dazu gedacht, als Referenz für Investitionsentscheidungen zu dienen.
Das könnte Ihnen auch gefallen
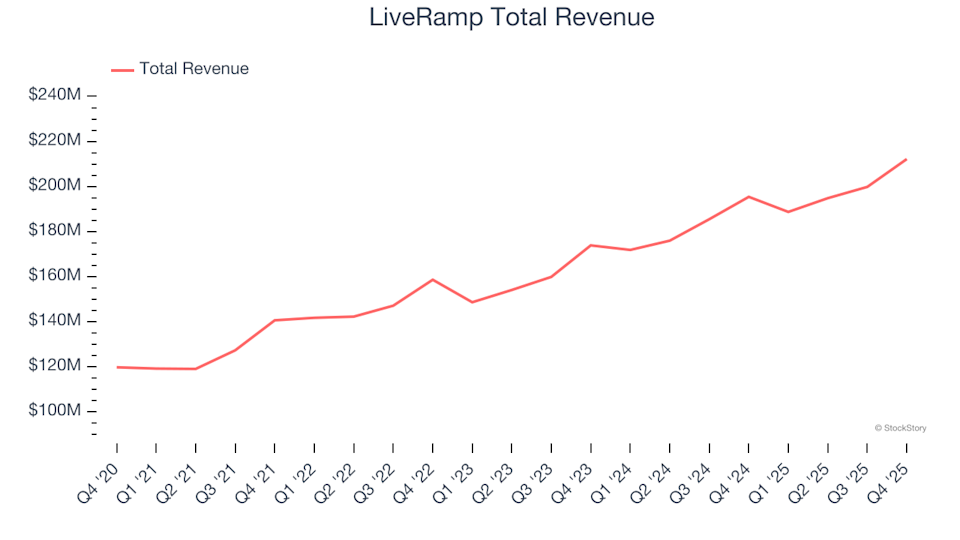
Quartalszahlen der Werbesoftware-Unternehmen Q4: Performance-Vergleich von LiveRamp (NYSE:RAMP)
Visa, Mastercard beschleunigen die Einführung von KI-Lösungen für Unternehmen
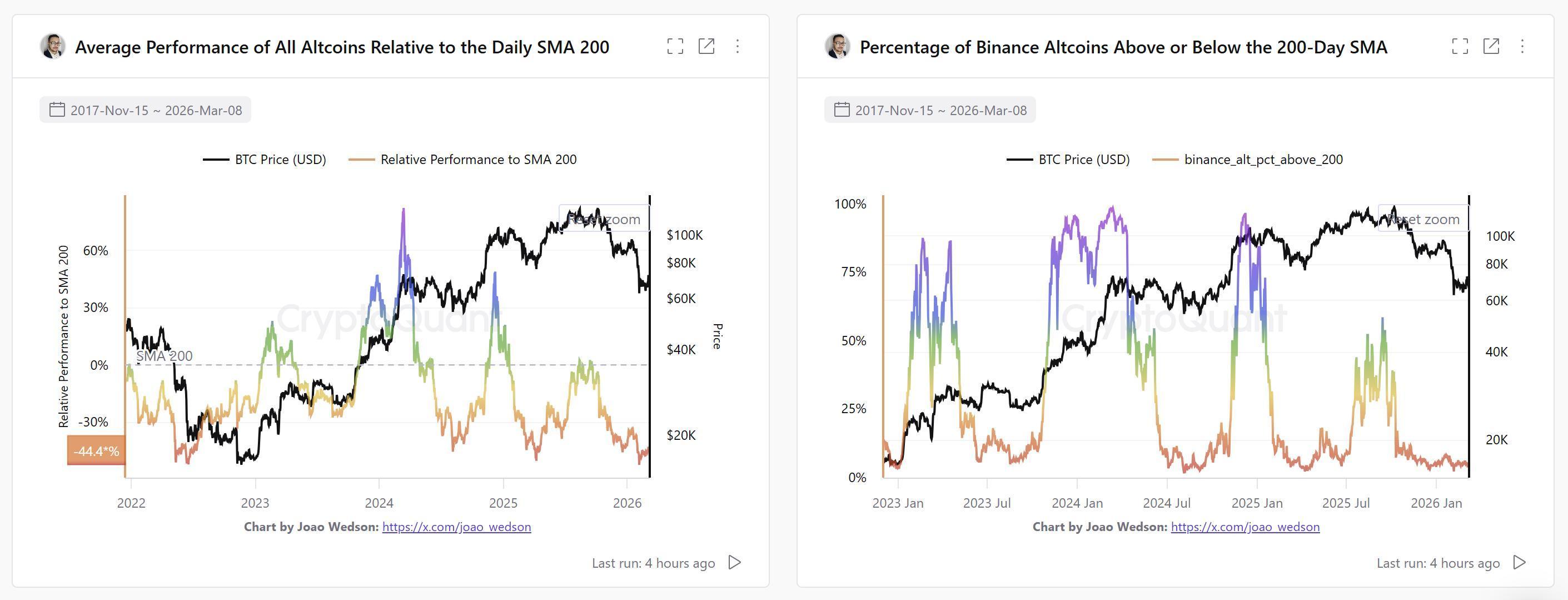
Bitcoin führt, Altcoin-Indikatoren fallen auf interessante Tiefstände: Zeit für eine Altseason?