DNLI rapporte une perte au quatrième trimestre inférieure aux prévisions, mise en avant du traitement du syndrome de Hunter
Vue d'ensemble financière de Denali Therapeutics pour le quatrième trimestre 2025
Denali Therapeutics (DNLI) a enregistré une perte nette de 0,73 $ par action au quatrième trimestre 2025, ce qui est légèrement meilleur que l'estimation consensuelle d'une perte de 0,75 $. À titre de comparaison, la perte était de 0,67 $ par action pour la même période l'année précédente.
L'augmentation annuelle de la perte par action a été principalement due à une hausse des dépenses opérationnelles.
Puisque Denali ne commercialise actuellement aucun produit, ses revenus sont limités aux produits des partenariats en cours. Au cours du trimestre rapporté, la société n'a enregistré aucun revenu de collaboration, ce qui est inférieur aux 18 millions de dollars attendus.
Au cours de l'année écoulée, les actions DNLI ont augmenté de 13,4 %, surperformant le secteur médical, biomédical et génétique, qui a connu une hausse de 11,5 %.
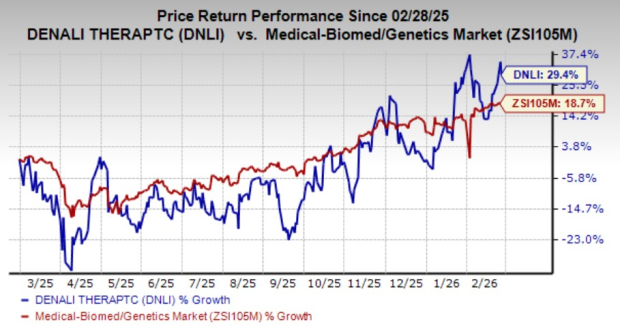
Source : Zacks Investment Research
Points clés des résultats du quatrième trimestre
- Les coûts de recherche et développement ont diminué de 1,9 % pour atteindre 97,9 millions de dollars, principalement en raison d'une réduction des dépenses liées aux projets de petites molécules.
- Les frais généraux et administratifs ont augmenté de 31,3 % pour atteindre 39,5 millions de dollars, reflétant les préparatifs en vue du lancement anticipé du tividenofusp alfa.
- Au 31 décembre 2025, Denali détenait environ 966,2 millions de dollars en liquidités, équivalents de trésorerie et titres négociables.
Résumé de l'année 2025
- Aucun revenu n'a été généré en 2025.
- La perte annuelle par action s'est creusée pour atteindre 2,97 $, contre 2,57 $ en 2024.
Progrès du principal candidat-médicament
Denali prépare activement l'introduction commerciale de son principal actif, le tividenofusp alfa.
La demande de licence de produit biologique (BLA) pour le tividenofusp alfa, destinée au traitement de la mucopolysaccharidose de type II (syndrome de Hunter), est actuellement en cours d'examen par les autorités réglementaires américaines.
La FDA a prolongé la date limite de son examen du 5 janvier 2026 au 5 avril 2026.
Le tividenofusp alfa a reçu plusieurs désignations de la FDA, notamment Breakthrough Therapy, Fast Track, Orphan Drug et Rare Pediatric Disease.
Cette thérapie expérimentale est conçue pour délivrer l'enzyme iduronate-2-sulfatase (IDS) à travers la barrière hémato-encéphalique, ciblant à la fois le corps et le cerveau.
La période d'examen de la BLA a été allongée après que Denali a fourni des données de pharmacologie clinique mises à jour en réponse à une demande de la FDA. L'entreprise a précisé que cette mise à jour n'était pas liée à l'efficacité, la sécurité ou les biomarqueurs.
La FDA a classé la soumission comme une modification majeure, entraînant une extension de la date d'action.
L'essai mondial de phase II/III COMPASS en cours devrait fournir des preuves supplémentaires pour les soumissions réglementaires mondiales, l'inclusion des participants neuronopathiques (Cohorte A) ayant été achevée en décembre 2025.
Développements de la pipeline
- Denali étudie DNL126 pour le syndrome de Sanfilippo de type A (MPS IIIA). Les premiers résultats de phase I/II présentés au WORLDSymposium ont montré des réductions significatives des biomarqueurs clés de la maladie et un profil de sécurité similaire aux thérapies de remplacement enzymatique existantes. Ces résultats pourraient soutenir une voie d'approbation accélérée, et une étude de confirmation de phase III est prévue.
- D'autres candidats de la pipeline sont développés en collaboration avec Takeda (TAK), Biogen (BIIB) et Sanofi (SNY).
- Denali et Takeda font avancer DNL593, un traitement potentiel pour la démence frontotemporale associée à la mutation granuline (FTD-GRN). L'inscription à l'étude de phase I/II est terminée, avec 40 participants. Les premières données sur les patients sont attendues en 2026.
- Denali a récemment obtenu l'approbation pour un essai de phase Ib de DNL628, dont les préparatifs sont en cours.
- Denali et Biogen développent conjointement BIIB122. Biogen dirige l'étude mondiale de phase IIb LUMA pour la maladie de Parkinson débutante, avec des résultats attendus à la mi-2026. Denali mène l'étude de phase IIa BEACON pour évaluer l'inhibition de LRRK2 dans la maladie de Parkinson associée à LRRK2.
- En octobre, Denali a soumis une demande IND pour DNL952 (ETV:GAA) afin de débuter des études cliniques dans la maladie de Pompe. La FDA a depuis levé la suspension clinique, et les préparatifs de l'étude de phase I sont en cours.
- Sanofi développe l'eclitasertib pour la colite ulcéreuse modérée à sévère, avec des données de phase II attendues au premier semestre de l'année.
Analyse des perspectives de Denali
L'approbation du tividenofusp alfa pourrait considérablement renforcer la trajectoire de croissance de Denali. Les progrès réalisés avec DNL126 sont également prometteurs.
Les solides réserves de trésorerie de l'entreprise soulignent sa capacité à soutenir les initiatives de recherche et développement en cours.
Avertissement : le contenu de cet article reflète uniquement le point de vue de l'auteur et ne représente en aucun cas la plateforme. Cet article n'est pas destiné à servir de référence pour prendre des décisions d'investissement.
Vous pourriez également aimer
Truist Financial chute de 3,4 % : quelle est la cause de cette forte baisse ?
Apple dévoile l'iPhone 17e économique et le MacBook Neo pour renforcer sa présence sur le marché
Voici la raison pour laquelle BorgWarner (BWA) se distingue en tant qu'action à forte croissance
