Seres fornisce aggiornamenti sui programmi e sull'azienda e dà priorità ai programmi emergenti nelle malattie infiammatorie e immunitarie
Seres ha finalizzato il protocollo per lo studio di Fase 2 di SER-155 in pazienti sottoposti a trapianto allogenico di cellule staminali ematopoietiche (allo-HSCT) con la FDA e ha avviato le principali attività di avvio dello studio e sospenderà ulteriori investimenti, mentre continuano gli sforzi per cercare finanziamenti per lo studio
Le azioni della società per estendere la propria liquidità, inclusa la riduzione della forza lavoro di circa il 30%, dovrebbero estendere la disponibilità di cassa fino al terzo trimestre del 2026
Seres si concentrerà sullo sviluppo dei suoi programmi di bioterapie vive in fase iniziale per malattie infiammatorie e immunitarie e supporterà la lettura dei risultati clinici dello studio su SER-155 sponsorizzato da investigatori in enterocolite correlata a checkpoint immunitari (irEC), un evento avverso frequente e grave nei destinatari della terapia ICI, prevista per l'inizio del secondo trimestre 2026
CAMBRIDGE, Mass., 12 febbraio 2026 (GLOBE NEWSWIRE) -- Seres Therapeutics, Inc. (Nasdaq: MCRB), una delle principali aziende di bioterapie vive, ha annunciato oggi che, dopo aver completato le principali attività di avvio per lo studio di Fase 2 di SER-155 in allo-HSCT, inclusa la presentazione del protocollo finale alla FDA, la valutazione e la qualificazione dei siti di studio con il proprio CRO e la produzione della sostanza farmaceutica per lo studio di Fase 2, Seres sospende ulteriori investimenti in quel programma e sposterà la propria attenzione operativa sui programmi della pipeline in fase iniziale a maggior valore, continuando a cercare finanziamenti per lo studio di Fase 2 su SER-155. Seres ha inoltre annunciato ulteriori misure per ridurre i costi operativi, tra cui una riduzione della forza lavoro di circa il 30%. Come risultato di queste e altre azioni per estendere la liquidità, e sulla base dei piani operativi attuali, l’azienda prevede di estendere la disponibilità di cassa fino al terzo trimestre del 2026, offrendo così ulteriori opportunità per sviluppare i propri programmi di bioterapie vive per malattie infiammatorie e immunitarie e perseguire potenziali collaborazioni.
Il programma SER-155 ha contribuito in modo significativo alla comprensione di Seres su come i microbi nel tratto gastrointestinale modulano funzionalmente i percorsi all'interfaccia barriera mucosale-immunitaria associati a malattie infiammatorie e immuno-correlate. Di conseguenza, la strategia futura dell’azienda darà priorità allo sviluppo dei suoi programmi in fase iniziale, incluso SER-603 che mira a indicazioni infiammatorie e immunitarie come colite ulcerosa, morbo di Crohn ed enterocolite correlata a checkpoint immunitari (irEC). Sono in corso discussioni con controparti per potenziali collaborazioni in questi ambiti.
“Seres ha adottato numerosi passaggi per prepararsi a uno studio di Fase 2 robusto su SER-155 in allo-HSCT, inclusa la presentazione del protocollo finale alla FDA, l’avanzamento della produzione della sostanza farmaceutica, la selezione di un CRO e il coinvolgimento con i potenziali siti di studio. Nel momento in cui spostiamo la nostra attenzione operativa verso la promettente pipeline in fase iniziale, siamo ora in grado di ottimizzare la nostra organizzazione e la struttura dei costi”, hanno dichiarato Thomas DesRosier e Marella Thorell, co-CEO di Seres. “Queste iniziative di riduzione dei costi e altre azioni dovrebbero estendere la nostra disponibilità di cassa fino alla fine del terzo trimestre di quest’anno, supportando lo sviluppo continuo dei nostri programmi per malattie infiammatorie e immuno-correlate, con target convalidati dai nostri dati preclinici e clinici precedentemente riportati, e offrendo ulteriore tempo per garantire finanziamenti per lo studio di Fase 2 su SER-155. Inoltre, mentre perseguiamo programmi in fase iniziale con le maggiori opportunità, come quelli che mirano alle malattie infiammatorie intestinali (IBD), stiamo esplorando collaborazioni per fornire capitale aggiuntivo alla società. Siamo molto grati per il contributo di tutti i membri del team che ci lasciano.”
Matthew Henn Ph.D., Chief Scientific Officer, ha aggiunto: “Siamo in attesa dei dati clinici imminenti su SER-155 nell’enterocolite correlata a checkpoint immunitari (irEC) che potrebbero dimostrare ulteriormente le ampie possibilità d’impiego di SER-155 e delle nostre bioterapie vive in generale. Lo studio sponsorizzato da investigatori in corso presso il Memorial Sloan Kettering Cancer Center sull’irEC, un evento avverso frequente per i pazienti che ricevono inibitori dei checkpoint immunitari (ICIs), è ora completamente arruolato e prevediamo di riportare i primi risultati clinici, inclusi i dati preliminari di sicurezza ed efficacia, all’inizio del secondo trimestre di quest’anno. Questi dati potrebbero mettere in luce l’opportunità per le bioterapie vive di rispondere a un bisogno medico insoddisfatto tra la vasta popolazione di pazienti oncologici che ricevono ICIs e potrebbero supportare un’ulteriore valutazione dell’approccio bioterapico di Seres in questo contesto.”
Valutazione SER-155 IST su irEC
Seres sta collaborando con il Memorial Sloan Kettering Cancer Center in uno studio sponsorizzato da investigatori (IST) che valuta SER-155 in 15 partecipanti con irEC. L’irEC è tra gli eventi avversi immuno-correlati (irAEs) più frequenti e gravi nei destinatari della terapia ICI e può essere osservata fino al 50% dei pazienti, con tassi che variano in base al farmaco oncologico e al regime terapeutico. Gli ICIs possono causare una vasta gamma di irAEs con collegamenti alla biologia delle cellule T e all’infiammazione della barriera epiteliale, entrambe funzioni biologiche che nei nostri dati preclinici e farmacologici clinici sono risultate positivamente influenzate da SER-155. I dati di questo IST potrebbero supportare ulteriormente il potenziale delle bioterapie vive come opzione di trattamento non immunosoppressiva per le malattie infiammatorie e immunitarie legate alla colite come le IBD e, più in generale, affrontare le tossicità della terapia immunitaria, entrambe rappresentando significativi bisogni medici insoddisfatti e potenziali opportunità commerciali.
Informazioni su Seres Therapeutics
Seres Therapeutics, Inc. (Nasdaq: MCRB) è un’azienda in fase clinica focalizzata sul miglioramento degli esiti per pazienti in condizioni di vulnerabilità medica attraverso la scoperta e lo sviluppo di nuove bioterapie vive. Seres ha guidato lo sviluppo e l’approvazione di VOWST™, la prima bioterapia del microbioma somministrata per via orale approvata dalla FDA e un farmaco designato Breakthrough Therapy, venduta a Nestlé Health Science a settembre 2024. L’azienda sta sviluppando SER-155 che ha dimostrato una significativa riduzione delle infezioni del flusso sanguigno e delle relative complicanze (rispetto al placebo) in uno studio clinico di Fase 1b in pazienti sottoposti ad allo-HSCT. SER-155 ha ricevuto le designazioni Breakthrough Therapy e Fast Track per lo sviluppo in questa popolazione e ha recentemente portato avanti le principali attività preparatorie per la Fase 2. Con una sovvenzione da CARB-X (Combating Antibiotic-Resistant Bacteria Biopharmaceutical Accelerator), Seres sta sviluppando una formulazione orale liquida di SER-155, per la somministrazione a pazienti che non possono assumere capsule orali, come i pazienti intubati in terapia intensiva, e altri pazienti vulnerabili ad alto rischio di infezioni da agenti antimicrobici resistenti. L’azienda sta portando avanti i suoi programmi sulla colite che includono l’enterocolite immuno-correlata (irEC) e la bioterapia viva sperimentale SER-603 nelle malattie infiammatorie e immunitarie, tra cui colite ulcerosa (UC) e morbo di Crohn. L’azienda ritiene che SER-155 e altri candidati bioterapici vivi coltivati possano essere sviluppati in ulteriori popolazioni di pazienti per affrontare il compromesso della barriera e le infezioni del flusso sanguigno e antimicrobico-resistenti oltre l’allo-HSCT, compresi i pazienti sottoposti ad autologo-HSCT, pazienti oncologici con neutropenia, destinatari CAR-T, persone con malattie epatiche croniche, destinatari di trapianto di organi solidi, nonché pazienti in unità di terapia intensiva e strutture per cure acute a lungo termine. Inoltre, l’azienda ritiene che SER-603 abbia il potenziale come opzione di trattamento non immunosoppressivo per le malattie infiammatorie e immunitarie legate alla colite e per affrontare in modo più ampio le tossicità della terapia immunitaria, entrambe rappresentando significativi bisogni medici insoddisfatti e potenziali opportunità commerciali.
Esclusione di responsabilità: il contenuto di questo articolo riflette esclusivamente l’opinione dell’autore e non rappresenta in alcun modo la piattaforma. Questo articolo non deve essere utilizzato come riferimento per prendere decisioni di investimento.
Ti potrebbe interessare anche
I risultati del quarto trimestre di Kamada (KMDA) non raggiungono le previsioni per utili e ricavi
5 fatti importanti da comprendere prima che il mercato azionario inizi a fare trading
Serve Robotics Inc. (SERV) registra una perdita nel quarto trimestre, supera le previsioni di fatturato
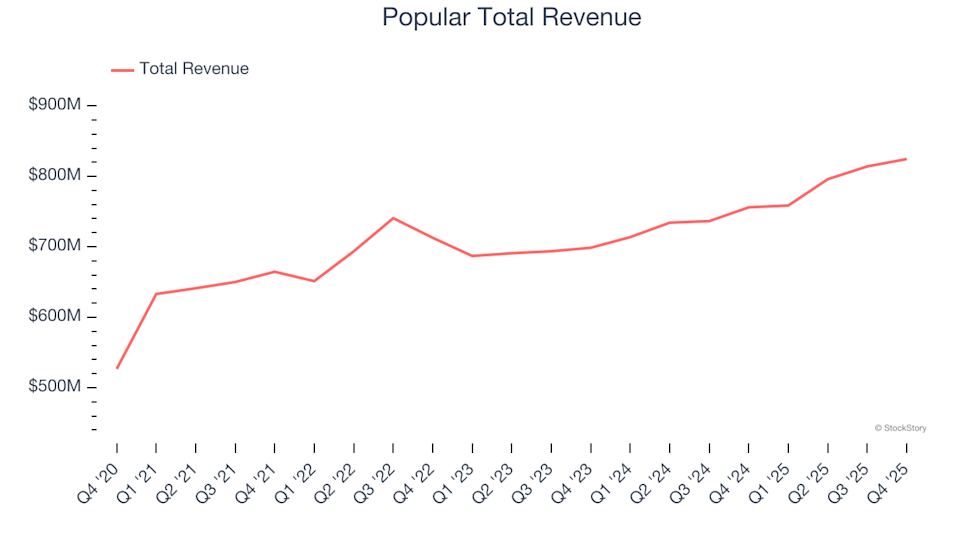
Riepilogo del quarto trimestre delle azioni delle banche regionali: Popular (NASDAQ:BPOP)