Emergent BioSolutions riceve l'approvazione della FDA statunitense per la domanda supplementare di nuovo farmaco (sNDA) per i multipack di spray nasale NARCAN
- L'approvazione amplierà il portafoglio di NARCAN ®Nasal Spray e migliorerà il rapporto costo-efficacia aumentando la flessibilità e l'efficienza distributiva di questo farmaco salvavita
GAITHERSBURG, Md., 12 febbraio 2026 (GLOBE NEWSWIRE) -- Oggi, Emergent BioSolutions (NYSE: EBS) ha annunciato che la U.S. Food and Drug Administration (FDA) ha approvato la sua supplemental New Drug Application (sNDA) per nuove configurazioni multipack di NARCAN da banco (OTC)
“In Emergent, lavoriamo a stretto contatto con i nostri partner per sviluppare soluzioni che aiutino a migliorare la consegna, la distribuzione e l'accessibilità di NARCAN
Questa approvazione si basa sull'impegno continuo di Emergent a migliorare l’accessibilità e l’usabilità di NARCAN
Informazioni su NARCAN
NARCAN
Informazioni su Emergent BioSolutions
In Emergent, la nostra missione è proteggere e salvare vite. Da oltre 25 anni, lavoriamo per preparare coloro che sono incaricati di proteggere la salute pubblica. Forniamo soluzioni di protezione e salvataggio contro minacce sanitarie come vaiolo, mpox, botulismo, Ebola, antrace ed emergenze da overdose di oppioidi. Per saperne di più su come aiutiamo le comunità di tutto il mondo a prepararsi alle sfide sanitarie di oggi e alle minacce di domani, visita il nostro sito web e seguici su LinkedIn, X, Instagram, Apple Podcasts e Spotify.
Esclusione di responsabilità: il contenuto di questo articolo riflette esclusivamente l’opinione dell’autore e non rappresenta in alcun modo la piattaforma. Questo articolo non deve essere utilizzato come riferimento per prendere decisioni di investimento.
Ti potrebbe interessare anche
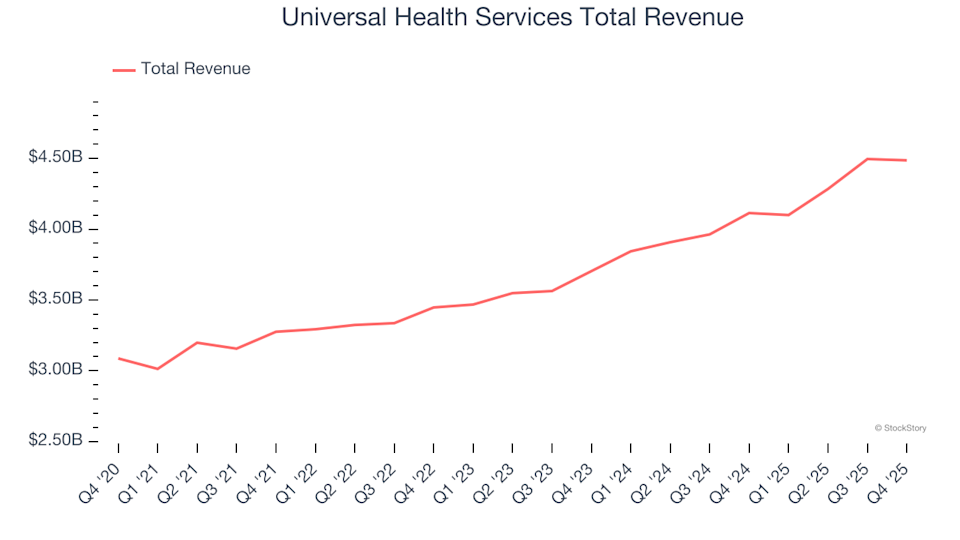
Riepilogo Q4 delle azioni delle catene ospedaliere: Universal Health Services (NYSE:UHS)