Candel Therapeutics annuncia un accordo di finanziamento di royalty da 100 milioni di dollari con RTW per sostenere il potenziale lancio di Aglatimagene Besadenovec (CAN-2409) nel trattamento del cancro alla prostata localizzato
- RTW ha impegnato 100 milioni di dollari per il finanziamento del lancio negli Stati Uniti, subordinato all’approvazione da parte della U.S. Food and Drug Administration (FDA) di aglatimagene besadenovec (aglatimagene o CAN-2409) per il tumore alla prostata localizzato a rischio intermedio-alto
- Le royalty saranno basate sulle vendite nette annuali di aglatimagene negli Stati Uniti.
- I fondi rafforzeranno il bilancio della Società in vista del potenziale lancio commerciale di aglatimagene negli Stati Uniti per il tumore alla prostata localizzato a rischio intermedio-alto
NEEDHAM, Mass., 19 febbraio 2026 (GLOBE NEWSWIRE) -- Candel Therapeutics, Inc. (Candel o la Società) (Nasdaq: CADL), azienda biofarmaceutica in fase clinica focalizzata sullo sviluppo di immunoterapie biologiche multimodali per aiutare i pazienti nella lotta contro il cancro, ha annunciato oggi un accordo di finanziamento royalty da 100 milioni di dollari con fondi gestiti da RTW Investments, LP (RTW), subordinato all’approvazione FDA di aglatimagene per il tumore alla prostata localizzato a rischio intermedio-alto.
“Questo finanziamento strategico non diluitivo supporterà il lancio statunitense di aglatimagene besadenovec, supponendo l’approvazione FDA, e ci consentirà di investire ulteriormente in quello che riteniamo sarà un programma commerciale di livello mondiale,” ha dichiarato Paul Peter Tak, M.D., Ph.D., FMedSci, Presidente e CEO di Candel. “Rimaniamo sulla buona strada per presentare la BLA per aglatimagene nel quarto trimestre di quest’anno e attendiamo con interesse la collaborazione con la FDA per perseguire un’approvazione rapida di aglatimagene. Siamo entusiasti della nostra partnership con RTW, mentre ci impegniamo a offrire una nuova opzione terapeutica ai pazienti nelle fasi iniziali del tumore alla prostata trattato con intento curativo, una patologia che ha visto poche innovazioni negli ultimi due decenni.”
“Lo studio clinico pivotale di fase 3 ha dimostrato il potenziale di aglatimagene besadenovec nel tumore alla prostata localizzato nelle fasi iniziali e l’impegno odierno riflette la nostra fiducia in Candel e nel forte potenziale commerciale di questa terapia,” ha affermato Roderick Wong, M.D., Managing Partner e Chief Investment Officer di RTW Investments, LP. “Siamo orgogliosi di collaborare con il management di Candel e non vediamo l’ora di supportare i loro sforzi per portare questo trattamento significativo ai pazienti con tumore alla prostata localizzato.”
Il finanziamento royalty per il lancio commerciale sarà disponibile al momento dell’approvazione FDA di aglatimagene e del soddisfacimento di altre condizioni consuete. Secondo i termini dell’accordo, RTW riceverà una percentuale a scaglioni in cifra singola sulle vendite nette annuali di aglatimagene negli Stati Uniti, soggetta a un tetto massimo.
Informazioni su Candel Therapeutics
Candel è una società biofarmaceutica in fase clinica focalizzata sullo sviluppo di immunoterapie biologiche multimodali pronte all’uso, che suscitano una risposta immunitaria antitumorale individualizzata e sistemica per aiutare i pazienti a combattere il cancro. Candel ha istituito due piattaforme di immunoterapia biologica multimodale in fase clinica, basate rispettivamente su nuovi costrutti genetici di adenovirus e virus herpes simplex (HSV). Aglatimagene besadenovec (CAN-2409 o aglatimagene) è il principale candidato della piattaforma adenovirus. L’azienda ha recentemente concluso con successo studi clinici di fase 2a su aglatimagene nel tumore polmonare non a piccole cellule (NSCLC) e nell’adenocarcinoma duttale pancreatico (PDAC), oltre a uno studio clinico pivotale, controllato con placebo, di fase 3 su aglatimagene nel tumore alla prostata localizzato, condotto sotto una Special Protocol Assessment concordata con la U.S. Food and Drug Administration (FDA). La FDA ha inoltre concesso la Fast Track Designation e la Regenerative Medicine Advanced Therapy Designation ad aglatimagene per il trattamento di tumore alla prostata localizzato di nuova diagnosi in pazienti con malattia a rischio intermedio-alto, la Fast Track Designation nel NSCLC, e sia la Fast Track Designation sia la Orphan Drug Designation per il trattamento del PDAC.
Linoserpaturev (CAN-3110) è il principale candidato della piattaforma HSV ed è attualmente oggetto di uno studio clinico di fase 1b in corso su glioma recidivante ad alto grado, valutando gli effetti di ripetute iniezioni di linoserpaturev. I risultati iniziali sono stati pubblicati su Nature e Science Translational Medicine e linoserpaturev ha ricevuto la Fast Track Designation e la Orphan Drug Designation dalla FDA. Infine, la piattaforma enLIGHTEN™ Discovery di Candel è una piattaforma di scoperta sistematica e iterativa basata su HSV, che sfrutta la biologia umana e l’analisi avanzata per creare nuove immunoterapie virali per i tumori solidi.
Dichiarazioni previsionali
Contatto per gli investitori
Theodore Jenkins
Vicepresidente, Relazioni con gli investitori e Sviluppo Business
Candel Therapeutics, Inc.
Contatto per i media
Ben Shannon
ICR Healthcare
Esclusione di responsabilità: il contenuto di questo articolo riflette esclusivamente l’opinione dell’autore e non rappresenta in alcun modo la piattaforma. Questo articolo non deve essere utilizzato come riferimento per prendere decisioni di investimento.
Ti potrebbe interessare anche
BlackRock sotto pressione: Il gigante della finanza limita i prelievi

Ripple: Utilizziamo XRP per generare liquidità per i flussi di pagamento
Un "bull trap" di Bitcoin si sta formando mentre il mercato ribassista entra nella fase centrale: Willy Woo
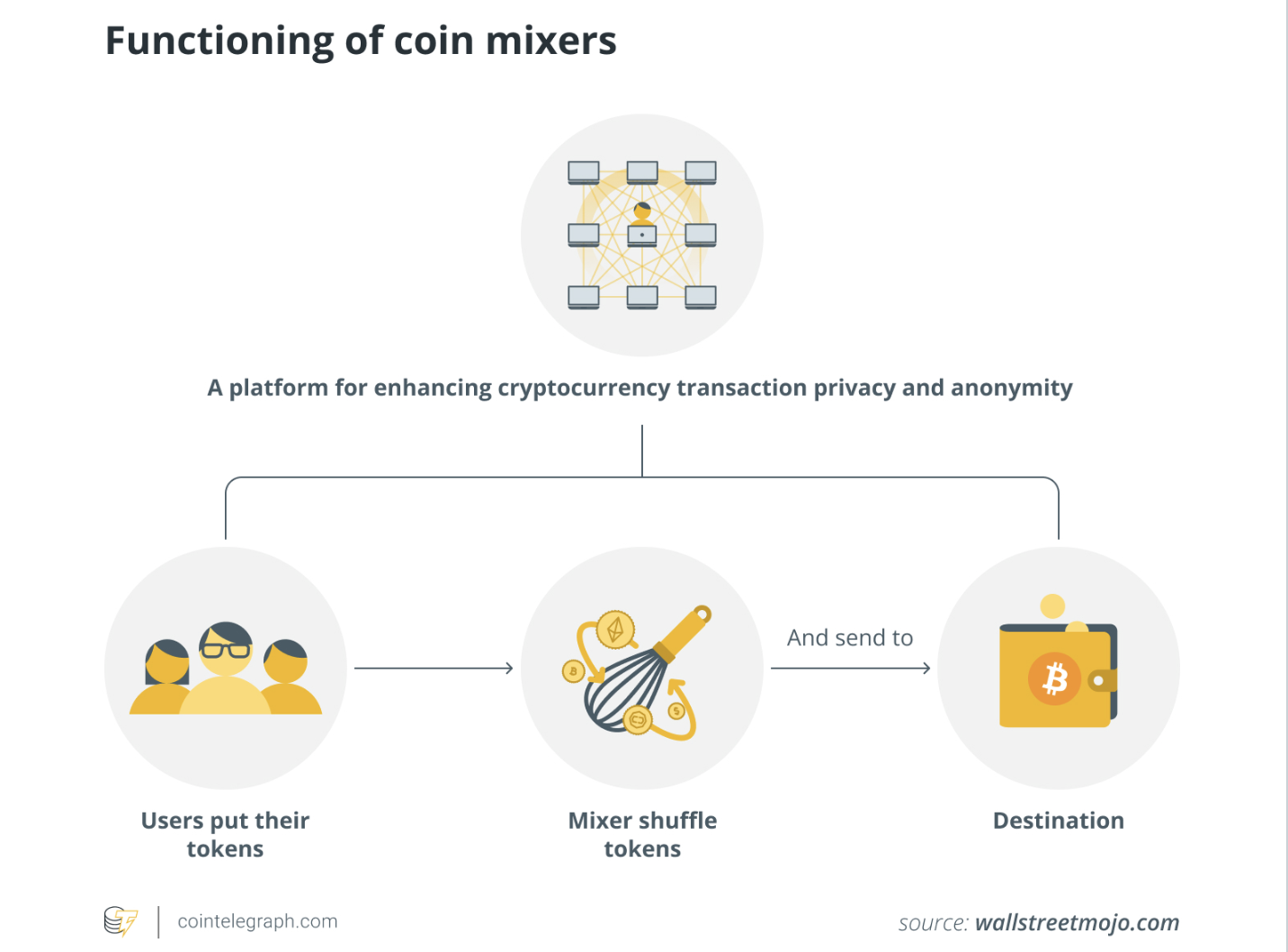
Il rapporto del Tesoro degli Stati Uniti riconosce gli usi legittimi dei crypto mixer