Mappatura della curva S: la partnership di INOVIO in GBM come mossa strategica per avanzare nelle piattaforme di immunoterapia a DNA
Glioblastoma: una frontiera ad alto rischio nel trattamento del cancro al cervello
Il glioblastoma (GBM) rappresenta la forma più temibile di cancro al cervello, noto per la sua progressione aggressiva. I pazienti affrontano una sopravvivenza mediana di circa 15 mesi e le probabilità di sopravvivere cinque anni sono inferiori al tre percento. Questa previsione cupa evidenzia l’urgente necessità di nuove terapie e alimenta gli sforzi di ricerca in corso. INOVIO ha collaborato con Regeneron per sviluppare INO-5401, con l’obiettivo di creare una nuova base per il trattamento di questi tumori così difficili. Tuttavia, questa iniziativa è ancora agli stadi iniziali e incerti, dove i rischi sono elevati e il successo è tutt’altro che garantito.
I risultati clinici attuali mostrano la difficoltà della sfida. INO-5401 è in fase di sperimentazione clinica di Fase II per il GBM, ma solo il 23% dei farmaci in questa categoria avanza con successo a questo stadio. Questo tasso è inferiore alla media dei trattamenti simili, indicando che INO-5401 deve affrontare un percorso particolarmente difficile. Il farmaco si trova ancora nella fase sperimentale, in cui i contrattempi sono comuni e l’efficacia dimostrata deve ancora essere raggiunta. Di fatto, INOVIO sta puntando su una svolta trasformativa prima che la tecnologia si sia affermata su larga scala.
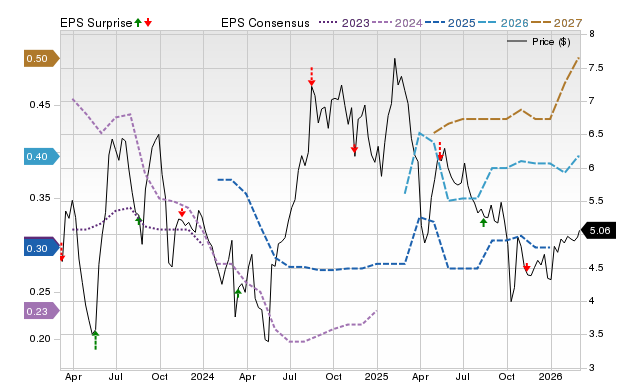
La fiducia degli investitori si riflette nell’andamento del titolo INOVIO, che recentemente è sceso a 1,68 dollari per azione. Questo prezzo segnala scetticismo sia sulle prospettive cliniche che sulla sostenibilità finanziaria del portfolio aziendale. Tale volatilità è tipica per le aziende che operano all’avanguardia dell’innovazione, dove la probabilità di fallimento è elevata. La collaborazione rappresenta una scommessa audace sul fatto che l’immunoterapia basata sul DNA possa diventare una pietra miliare dei futuri trattamenti oncologici, ma per ora il mercato attende risultati concreti.
Approcci innovativi: gettare le basi per l’immunoterapia di nuova generazione
L’alleanza tra INOVIO e Akeso è una mossa calcolata per far progredire l’infrastruttura dell’immunoterapia. La strategia consiste nel combinare la tecnologia DNA di INOVIO con un inibitore di checkpoint innovativo per colpire più efficacemente la capacità del cancro di eludere il sistema immunitario. La sperimentazione clinica abbinerà INO-5412—un vaccino DNA progettato per colpire antigeni specifici del tumore—con il cadonilimab di Akeso, un anticorpo bispecifico che blocca sia i checkpoint PD-1 che CTLA-4. Questo approccio duale è pensato per stimolare una più forte risposta delle cellule T, trasformando l’ambiente tumorale tipicamente “freddo” del GBM in uno più suscettibile agli attacchi immunitari.
La sperimentazione INSIGhT adaptive platform, che valuterà questa combinazione, è strutturata per testare più terapie in modo efficiente utilizzando un gruppo di controllo condiviso. Questo design può accelerare notevolmente lo sviluppo e ridurre i costi, fattore cruciale quando si sperimentano nuovi modelli di trattamento. La motivazione scientifica è convincente: l’immunoterapia DNA prepara il sistema immunitario, mentre gli inibitori dei checkpoint rimuovono i segnali inibitori. Insieme, potrebbero superare i limiti di ciascun approccio preso singolarmente. In precedenti risultati di Fase II con INO-5401 e un inibitore PD-1 sono state osservate risposte immunitarie promettenti e potenziali benefici in termini di sopravvivenza, fornendo una solida base per questo prossimo passo.
Tuttavia, rimane una sfida importante. Sebbene cadonilimab abbia dimostrato efficacia in altri tumori ed è stato approvato in Cina per i tumori dello stomaco e della cervice, il suo impatto sul GBM—un cancro con un microambiente immunitario altamente soppressivo—resta non testato. Questo studio sarà una prova cruciale per capire se la combinazione può avere successo in uno dei tumori più difficili. Un risultato positivo potrebbe stabilire un nuovo standard per le immunoterapie di combinazione, mentre un fallimento metterebbe in luce la complessità biologica del GBM e i rischi degli approcci innovativi. Per ora, INOVIO sta sfruttando una piattaforma ad alta efficienza per valutare rigorosamente questa tecnologia promettente ma ancora indimostrata.
Sfide finanziarie e rischi operativi
Le prospettive finanziarie del programma GBM di INOVIO sono strettamente legate alla capacità di assicurare finanziamenti e realizzare traguardi clinici significativi. I precedenti dati di Fase II che combinavano INO-5401 con cemiplimab hanno mostrato una sopravvivenza globale mediana di 32,5 mesi nei pazienti MGMT-metilati, un miglioramento notevole rispetto agli esiti storici. Questo pone un obiettivo elevato per la nuova combinazione con cadonilimab, che dovrà produrre un beneficio di sopravvivenza statisticamente significativo superiore a questo benchmark per giustificare ulteriori investimenti e adozione.
Questo scenario comporta un significativo rischio esecutivo. La partnership con Akeso è un’attività ad alta richiesta di risorse, poiché le sperimentazioni di Fase II richiedono finanziamenti consistenti per l’arruolamento dei pazienti, il monitoraggio e l’analisi dei dati. La capacità di INOVIO di proseguire la sperimentazione dipende dalle sue riserve finanziarie e dai futuri sforzi di fundraising. Senza capitale sufficiente, lo studio potrebbe subire ritardi o riduzioni di portata, compromettendo l’intera strategia di costruzione delle infrastrutture. La cautela del mercato, visibile nel prezzo depresso delle azioni, riflette queste preoccupazioni.
La concorrenza aggiunge un ulteriore livello di complessità. Ivonescimab di Akeso, ad esempio, ha mostrato solo miglioramenti modesti rispetto a Keytruda e non ha raggiunto un beneficio di sopravvivenza statisticamente significativo nell’analisi ad interim. Ciò sottolinea l’alto standard richiesto per dimostrare che una nuova terapia sia superiore ai trattamenti consolidati. Per INOVIO, la nuova combinazione non solo deve funzionare, ma deve anche superare chiaramente i propri risultati precedenti. Un fallimento rafforzerebbe la cautela degli investitori e metterebbe in dubbio il potenziale a breve termine dell’immunoterapia DNA.
In definitiva, la sostenibilità finanziaria di questo progetto ad alto rischio dipende da due fattori: assicurare abbastanza finanziamenti per avanzare nello studio e generare dati clinici trasformativi. Fino a quando entrambi non saranno raggiunti, la collaborazione rimane uno sforzo audace ma non ancora comprovato, esposto agli stessi rischi che hanno sfidato molti innovatori biotech.
Mile-stone chiave e rischi futuri
Il futuro di questa collaborazione è determinato da vari eventi e incertezze fondamentali. L’imminente catalizzatore sono i risultati intermedi della sperimentazione INSIGhT, che offriranno i primi spunti sulla sicurezza e sull’efficacia della terapia. Questa sperimentazione adattiva è pensata per una valutazione rapida, e i risultati iniziali saranno cruciali per determinare se l’approccio infrastrutturale sia valido. Un esito positivo potrebbe accelerare lo sviluppo, mentre risultati deludenti potrebbero bloccare ulteriori investimenti in questa combinazione.
Un altro fattore importante è il progresso di Akeso con gli altri programmi di anticorpi bispecifici. L’azienda ha recentemente ricevuto la quinta Breakthrough Therapy Designation per ivonescimab nel tumore delle vie biliari, a testimonianza dell’impegno nell’avanzamento di diverse risorse. Questo slancio potrebbe rafforzare il supporto di Akeso per il programma cadonilimab, ma significa anche che le risorse potrebbero essere suddivise tra priorità concorrenti. Eventuali contrattempi in pipeline più ampia di Akeso potrebbero influire indirettamente sul ritmo e sull’attenzione per la collaborazione GBM.
La sfida più grande rimane la validazione clinica. La nuova terapia deve dimostrare un chiaro vantaggio in termini di sopravvivenza rispetto allo standard attuale, che include i dati precedenti di INOVIO di una sopravvivenza mediana di 32,5 mesi in certi pazienti. Con solo il 23% di successo per i farmaci GBM nelle fasi cliniche, la soglia è estremamente alta. Il mancato raggiungimento di un beneficio significativo potrebbe determinare la fine dello sviluppo e nutrire dubbi sulla validità a breve termine dell’immunoterapia DNA.
L’arruolamento dei pazienti per il trial di terapia combinata dovrebbe iniziare nella seconda metà del 2026, fissando una tempistica chiara per la prossima importante pubblicazione di dati. Per gli investitori, si tratta di uno scenario ad alta posta in gioco: la collaborazione sta costruendo le fondamenta per un nuovo approccio al trattamento del cancro, ma il suo futuro dipenderà dal successo dei risultati iniziali. I prossimi mesi sveleranno se questo sarà l’inizio di una nuova era nelle cure oncologiche o una costosa deviazione.
Esclusione di responsabilità: il contenuto di questo articolo riflette esclusivamente l’opinione dell’autore e non rappresenta in alcun modo la piattaforma. Questo articolo non deve essere utilizzato come riferimento per prendere decisioni di investimento.
Ti potrebbe interessare anche
ETF Aerei: Una scommessa tattica su un crollo temporaneo dello spazio aereo
Scott Bessent prevede che Trump aumenterà le tariffe al 15% nel prossimo futuro
CI&T Inc. (CINT) prevede un aumento degli utili: informazioni chiave prima del rapporto della prossima settimana