Sカーブのマッピング:INOVIOのGBMパートナーシップはDNA免疫療法プラットフォーム推進への戦略的な一手
膠芽腫:脳腫瘍治療のハイリスク最前線
膠芽腫(GBM)は、最も強力な脳腫瘍として知られており、その進行は非常に急速です。患者の生存中央値は約15ヶ月であり、5年生存率は3%未満です。この厳しい見通しは、新たな治療法の切迫した必要性を浮き彫りにしており、継続的な研究を促進しています。INOVIOはRegeneronと提携し、INO-5401を開発することで、これら困難な腫瘍治療の新しい基盤構築を目指しています。しかし、この取り組みはまだ初期段階にあり、リスクが高く、成功は保証されていません。
現在の臨床結果は、険しい戦いを示しています。INO-5401はGBMの第II相臨床試験中ですが、このカテゴリーの薬剤が成功裏に進む割合はわずか23%です。この成功率は同分野平均より低く、INO-5401が特に厳しい道をたどることを示しています。薬剤は依然として実験段階にあり、失敗も多く、効果の実証はまだありません。INOVIOは、技術が大規模に実証される前に変革的なブレークスルーに賭けている状況です。
投資家の信頼は、INOVIO株価の動向に反映されています。最近は1株1.68ドルまで下落し、同社の臨床見通しやパイプライン財務の持続可能性に懐疑的な姿勢を示しています。このようなボラティリティは、イノベーション最前線の企業に典型的であり、失敗の可能性が高いです。この協力は、DNAベース免疫療法が未来の癌治療の基盤となり得るという大胆な賭けですが、現時点では市場は具体的な成果を期待して待機しています。
革新的アプローチ:次世代免疫療法の基礎構築
INOVIOとAkesoの提携は、免疫療法インフラの進化を狙った計算された一手です。INOVIOのDNA技術と先進的なチェックポイント阻害薬を組み合わせることで、癌が免疫系を回避する能力により効果的に対処する戦略です。臨床試験では、腫瘍特異的抗原を標的とするDNAワクチンINO-5412と、PD-1およびCTLA-4の両チェックポイントを阻害するAkesoの二重特異抗体cadonilimabを組み合わせます。この二重アプローチにより、より強力なT細胞応答を誘発し、GBMの「冷たい」腫瘍環境を免疫攻撃に適した状態へ転換することを目指しています。
この組み合わせを評価するINSIGhTアダプティブプラットフォーム試験は、複数の治療法を効率的に検証するため、共通の対照群を用いる構造です。この設計は開発を加速し、コストを大幅に削減でき、新しい治療モデルを開拓する上で特に重要です。科学的根拠も説得力があります。DNA免疫療法は免疫系を活性化し、チェックポイント阻害薬は抑制信号を解除します。この組み合わせにより、それぞれの限界を乗り越えられる可能性があります。以前のINO-5401とPD-1阻害薬の第II相試験では、有望な免疫応答と生存利益が確認されており、この次のステップの基盤となっています。
しかし、一つ大きな課題が残されています。cadonilimabは他の癌種では効果が証明され、中国では胃癌や子宮頸癌で承認されていますが、免疫抑制の強いGBMではその効果は未検証です。本試験は、この組み合わせが難治性癌の中でも成功するかどうかの重要な検証となります。良好な結果は、免疫療法の新しい標準を確立する可能性がありますが、失敗すればGBMの生物学的複雑さや革新的アプローチのリスクを浮き彫りにします。現時点では、INOVIOは高効率プラットフォームを活用し、有望だが未証明な技術を徹底的に評価しています。
財務的課題と実行リスク
INOVIOのGBMプログラムの財務見通しは、資金確保と重要な臨床マイルストーン達成能力に密接に結び付いています。INO-5401とcemiplimabを組み合わせた過去の第II相データでは、MGMTメチル化患者で全生存期間中央値32.5ヶ月と従来より大幅な改善が示されました。これはcadonilimabとの新組み合わせにとって高い基準となり、更なる投資や普及にはこの基準を上回る統計的有意差が求められます。
この状況は実行リスクを大きくします。Akesoとの提携はリソース集約型で、第II相試験は患者登録、モニタリング、データ解析に多額の資金を要します。INOVIOが試験を継続するには財務体力と今後の資金調達が必要ですが、充分な資本がなければ、研究遅延や規模縮小などでインフラ構築戦略が危ぶまれます。株価が停滞しているのは市場の警戒感の現れです。
競争もさらに複雑化させています。AkesoのivonescimabはKeytrudaに比べて改善は限定的で、中間解析で統計的有意な生存利益は得られませんでした。これは新規治療が既存治療より優れていることを証明するためには、非常に高い基準が必要なことを示しています。INOVIOにとって、新たな組み合わせ治療は、実際に効果を発揮するだけでなく、過去の自社データに対して明確に優れた成果を示さなければなりません。もしこれに達しなければ、投資家の懸念が強まり、DNA免疫療法の短期的な可能性に疑念が生じます。
最終的に、このハイリスクの取り組みの財務的持続性は、試験を進めるための十分な資金確保と変革的な臨床データの創出の二つにかかっています。どちらも達成されるまでは、協力体制は大胆ながら未証明の取り組みにとどまり、多くのバイオテクノロジー革新者が直面した障害と同様のリスクに晒されています。
主要マイルストーンと今後のリスク
この協力の未来は、いくつかの重要なイベントと不確定要素によって左右されます。最も直近の推進力はINSIGhT試験の中間結果であり、治療の安全性と有効性について早期の洞察を提供します。このアダプティブ試験は迅速な評価を目的としており、初期結果がインフラアプローチの実現可能性を判定する鍵となります。良好な結果なら開発が加速し、期待はずれであればこの組み合わせへの投資が停止する可能性があります。
もう一つの重要な要因は、Akesoが進める他の二重特異抗体プログラムの進展です。同社は最近、胆道癌でivonescimabの5回目のBreakthrough Therapy Designationを取得し、複数アセットの開発推進を示しています。この勢いはcadonilimabプログラムの支援強化にもつながりますが、リソースが競合する優先事業に分割される可能性もあります。Akesoのパイプライン全体が遅延すれば、GBM協力の進捗や焦点にも間接的な影響が及ぶでしょう。
最大の課題は臨床的な証明です。新たな治療法は、既存標準、すなわちINOVIO自身の32.5ヶ月という生存中央値データを上回る明確な生存利益を示さなければなりません。GBM薬剤が臨床フェーズを進む成功率はわずか23%なので、基準は非常に高く設定されています。もし十分な効果が示せなければ、開発継続は打ち切られ、DNA免疫療法の近い将来の実現性にも疑念が生じます。
組み合わせ治療の臨床試験への患者登録は2026年後半に始まる予定であり、次の主要データ公開タイミングが明確になっています。投資家にとっては典型的なハイリスクシナリオですが、この協力体制は新たな癌治療アプローチの基盤を築いており、その未来は初期成果の成否にかかっています。今後数ヶ月で、これが癌ケアの新時代の始まりなのか、それとも高くつく回り道なのかが明らかになるでしょう。
免責事項:本記事の内容はあくまでも筆者の意見を反映したものであり、いかなる立場においても当プラットフォームを代表するものではありません。また、本記事は投資判断の参考となることを目的としたものではありません。
こちらもいかがですか?
トランスコンチネンタルの新任CEOは、主要な印刷効率に注力する戦略的な方向転換を示唆
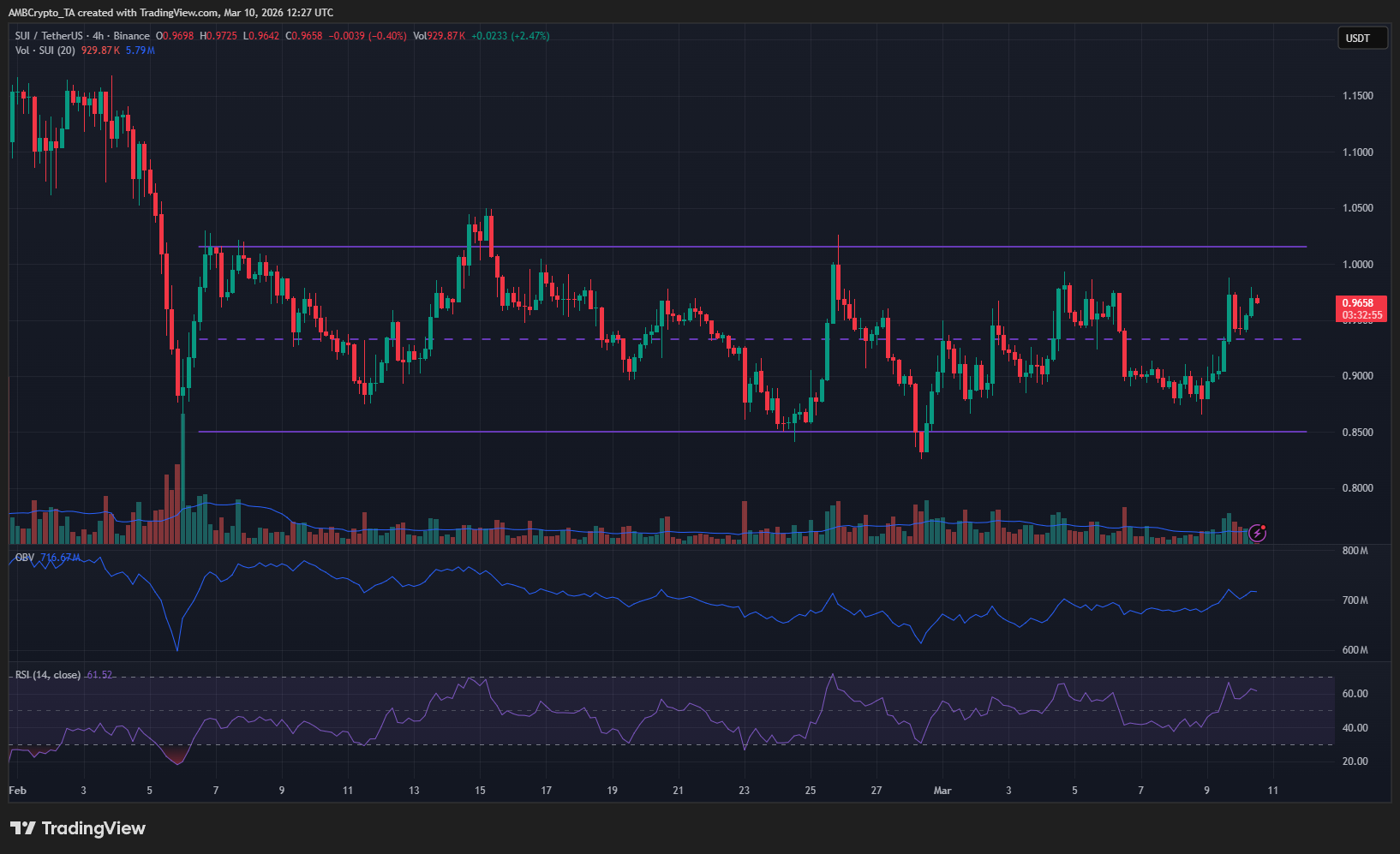
altcoinの最新7%上昇後のSUIの次なる課題についてすべて解説
Micronの勢い:40万ドルの強気な賭けと高まるAI需要
バンク・オブ・アメリカの取引急増、ボラティリティ減少とマージン精査で試練
