NovaBridge podaje pierwszemu pacjentowi lek w globalnym, randomizowanym badaniu fazy 2 oceniającym Givastomig w połączeniu z immunochemioterapią u pacjentów z przerzutowym rakiem żołądka w 1. linii leczenia
- Globalne, randomizowane badanie fazy 2 mające na celu ocenę dodania givastomig, bispecyficznego przeciwciała CLDN18.2 x 4-1BB (8 mg/kg i 12 mg/kg), do standardowej immunochemioterapii u pacjentów z przerzutowym rakiem żołądka w pierwszej linii (1L)
- Kluczowy kamień milowy opiera się na pozytywnych danych z fazy 1b, wykazujących, że givastomig zapewniał najlepszą w swojej klasie potencjalną skuteczność u pacjentów z przerzutowym rakiem żołądka HER2-ujemnym w pierwszej linii w połączeniu z nivolumabem i chemioterapią (mFOLFOX6)
- Wyniki fazy 1b pokazały, że pacjenci leczeni givastomigiem osiągnęli obiektywny wskaźnik odpowiedzi (ORR) na poziomie 75%, medianę czasu wolnego od progresji choroby (mPFS) wynoszącą 16,9 miesiąca oraz 82% sześciomiesięczny wskaźnik PFS
- Rak żołądka stanowi okazję rynkową wartą 12 miliardów dolarów do 2030 roku
- Oczekuje się, że najważniejsze wyniki z fazy 2 będą dostępne w 2027 roku
ROCKVILLE, Md., 17 lutego 2026 r. (GLOBE NEWSWIRE) -- NovaBridge Biosciences (Nasdaq: NBP) (NovaBridge lub Spółka), globalna platforma biotechnologiczna zaangażowana w przyspieszanie dostępu do innowacyjnych leków, ogłosiła dziś rozpoczęcie rekrutacji pierwszego pacjenta do globalnego, randomizowanego badania fazy 2 oceniającego givastomig, bispecyficzne przeciwciało Claudin 18.2 (CLDN18.2) x 4-1BB, w połączeniu z nivolumabem i chemioterapią (mFOLFOX6) u pacjentów z HER2-ujemnym, przerzutowym rakiem żołądka w pierwszej linii. Pozytywne dane z fazy 1b pozycjonują givastomig jako potencjalną terapię CLDN18.2 o najlepszej skuteczności w leczeniu raka żołądka, z przewidywaną wartością rynkową 12 miliardów dolarów do 2030 roku
„Z przyjemnością informujemy o kolejnym kroku w kierunku komercjalizacji givastomig, poprzez rozpoczęcie globalnego, randomizowanego badania fazy 2. Badanie to opiera się na przekonujących wynikach fazy 1b givastomig, wykazujących silną skuteczność i korzystny ogólny profil tolerancji, a także potencjalną znaczącą poprawę w stosunku do historycznych standardów leczenia. Faza 2 została zaprojektowana, aby potwierdzić te wyniki w szerszym zakresie i zwalidować givastomig jako potencjalnie najlepszą terapię w swojej klasie dla przerzutowego raka żołądka w pierwszej linii, z potencjałem szerokiego zastosowania wśród pacjentów z CLDN18.2 o różnym poziomie ekspresji i dodatnim PD-L1,” powiedział Phillip Dennis, MD, PhD, Dyrektor Medyczny NovaBridge. „Oczekujemy, że wyniki tego badania zostaną zaprezentowane w 2027 roku. Ponadto spodziewamy się przedstawić zaktualizowane wyniki z badania rozszerzenia dawki fazy 1b w drugiej połowie tego roku.”
„Nadal jesteśmy zachęceni wysokim wskaźnikiem odpowiedzi givastomig w szerokim zakresie ekspresji Claudin 18.2 i PD-L1. Głębokość i długość odpowiedzi osiągniętych w terapii skojarzonej wraz z dobrą tolerancją umożliwiły szybkie włączenie pacjentów do badania fazy 1b i stanowią solidną podstawę do przejścia do następnego etapu rozwoju,” powiedział Samuel J. Klempner, MD, profesor nadzwyczajny medycyny w Mass General Brigham Cancer Institute. „Mamy nadzieję, że, przy dalszych pozytywnych wynikach klinicznych, givastomig ostatecznie stanie się standardem leczenia raka żołądka i przełyku.”
„Rozpoczęcie badania fazy 2 stanowi kluczowy moment dla NovaBridge, ponieważ przechodzimy do etapu średniozaawansowanej spółki klinicznej. Przekonujące dane dotyczące skuteczności i bezpieczeństwa fazy 1b potwierdzają potencjał givastomig jako wiodącej terapii skierowanej na CLDN18.2 dla raka żołądka i nie tylko. Silne i trwałe odpowiedzi podkreślają nasze przekonanie o istotnym potencjale komercyjnym givastomig,” powiedział Sean Fu, PhD, MBA, Prezes NovaBridge. „Pozostajemy skoncentrowani na opracowywaniu nowatorskich, zróżnicowanych terapii, które mogą zrewolucjonizować leczenie pacjentów na całym świecie i wierzymy, że givastomig będzie kamieniem węgielnym naszego przyszłego rozwoju.”
O badaniu fazy 1b eskalacji i rozszerzenia dawki givastomig w 1L raku żołądka
Dane z fazy 1b (zgodnie z komunikatem prasowym i prezentacją korporacyjną z 6 stycznia 2026 r.) wykazały, że givastomig, podawany w dawkach 8 mg/kg co dwa tygodnie (Q2W) i 12 mg/kg Q2W, zapewniał:
- Silną skuteczność, z 75% ORR (77% ORR obserwowane przy 8 mg/kg, 73% ORR obserwowane przy 12 mg/kg, n=52 ocenianych)
- Odpowiedzi zaobserwowane w szerokim zakresie ekspresji PD-L1 i CLDN18.2
- Trwałe odpowiedzi z 16,9-miesięcznym mPFS i 82% 6-miesięcznym wskaźnikiem PFS (n=53 ocenianych)
- Dobry ogólny profil tolerancji w połączeniu z immunochemioterapią, bez toksyczności zależnej od dawki
Szczegółowe dane z fazy 1b rozszerzenia zostaną przedstawione podczas ważnej konferencji medycznej w drugiej połowie 2026 roku
O globalnym, randomizowanym badaniu fazy 2 givastomig w leczeniu 1L raka żołądka
Globalne, randomizowane badanie fazy 2 ocenia bezpieczeństwo i skuteczność givastomig stosowanego w połączeniu z nivolumabem i mFOLFOX6 jako terapii 1L u pacjentów z rakiem żołądka CLDN18.2-dodatnim, w tym rakiem żołądkowo-przełykowym (GEC), rakiem połączenia żołądkowo-przełykowego (GEJ), gruczolakorakiem żołądkowo-przełykowym (GEA), z poziomem CLDN18.2 ≥1+ w intensywności immunohistochemicznej (IHC) na ≥1% komórek oraz ekspresją PD-L1 ≥1. Oczekuje się, że do badania zostanie włączonych około 180 pacjentów (randomizowanych równomiernie do 8 mg/kg givastomig, 12 mg/kg givastomig lub nivolumab+mFOLFOX6). Głównym punktem końcowym jest czas wolny od progresji (PFS); drugorzędowe punkty końcowe obejmują obiektywny wskaźnik odpowiedzi (ORR), całkowite przeżycie (OS), czas trwania odpowiedzi (DoR) i wskaźnik kontroli choroby (DCR). Badanie będzie obejmować pacjentów na całym świecie.
Źródła:
- Rynki obejmują USA, pięć krajów UE oraz Japonię do 2030 roku dla potencjalnej sprzedaży na podstawie Data Monitor Biomed Tracker
O givastomig
Givastomig (TJ033721 / ABL111) to bispecyficzne przeciwciało skierowane przeciwko komórkom nowotworowym z dodatnim Claudin 18.2 (CLDN18.2). Warunkowo aktywuje komórki T poprzez szlak sygnalizacyjny 4-1BB w mikrośrodowisku guza, gdzie wyrażany jest CLDN18.2. Givastomig jest rozwijany jako potencjalne leczenie raka żołądka oraz innych nowotworów przewodu pokarmowego wykazujących ekspresję Claudin 18.2. W badaniach fazy 1 givastomig wykazał obiecującą aktywność przeciwnowotworową, przypisywaną synergistycznemu efektowi bliskiej interakcji między CLDN18.2 na komórkach nowotworowych i 4-1BB na komórkach T w mikrośrodowisku guza, jednocześnie minimalizując toksyczności często obserwowane w przypadku innych agonistów 4-1BB.
Givastomig jest rozwijany wspólnie w ramach globalnej współpracy z ABL Bio, w której NovaBridge jest stroną wiodącą i dzieli globalne prawa, z wyłączeniem Wielkich Chin i Korei Południowej, po równo z ABL Bio.
O NovaBridge
NovaBridge to globalna platforma biotechnologiczna zaangażowana w przyspieszanie dostępu do innowacyjnych leków. Firma łączy głęboką ekspertyzę w rozwoju biznesu z elastycznym rozwojem klinicznym, aby identyfikować, przyspieszać i rozwijać przełomowe rozwiązania. Dzięki połączeniu nauki, strategii i realizacji NovaBridge umożliwia szybki postęp terapii transformacyjnych od etapu odkrycia do pacjentów w potrzebie.
Różnicowana linia rozwojowa firmy jest prowadzona przez givastomig, potencjalnie najlepsze w swojej klasie bispecyficzne przeciwciało Claudin 18.2 x 4-1BB oraz VIS-101, bifunkcyjny biologiczny lek drugiej generacji, potencjalnie najlepszy w swojej klasie, ukierunkowany na VEGF-A i ANG2.
Givastomig warunkowo aktywuje komórki T poprzez szlak sygnalizacyjny 4-1BB w mikrośrodowisku guza, gdzie wyrażany jest Claudin 18.2. Givastomig jest rozwijany w celu leczenia raka żołądka z dodatnim Claudin 18.2 oraz innych nowotworów przewodu pokarmowego. Produkt jest oceniany w globalnym, randomizowanym badaniu fazy 2, po niedawnym ogłoszeniu pozytywnych wyników fazy 1b, wieloośrodkowego, otwartego badania w raku żołądka w pierwszej linii. Firma współpracuje również z partnerem, ABL Bio, nad rozwojem ragistomig, bispecyficznego przeciwciała integrującego PD-L1 jako łącznika guza i 4-1BB jako warunkowego aktywatora komórek T w guzach litych. Dodatkowo, NovaBridge posiada globalne prawa poza Chinami do uliledlimab, przeciwciała anty-CD73, które celuje w immunosupresję napędzaną przez adenozynę w nowotworach.
VIS-101 celuje w VEGF-A i ANG-2, aby zapewnić silniejsze i trwalsze korzyści terapeutyczne dla pacjentów z wysiękową postacią zwyrodnienia plamki związaną z wiekiem (wet AMD) oraz cukrzycowym obrzękiem plamki żółtej (DME). VIS-101 jest obecnie w fazie randomizowanego, wielodawkowego badania fazy 2a dla wet AMD. NovaBridge jest większościowym udziałowcem Visara, a Visara posiada globalne prawa do VIS-101 poza Wielkimi Chinami i wybranymi krajami Azji.
Zastrzeżenie: Treść tego artykułu odzwierciedla wyłącznie opinię autora i nie reprezentuje platformy w żadnym charakterze. Niniejszy artykuł nie ma służyć jako punkt odniesienia przy podejmowaniu decyzji inwestycyjnych.
Może Ci się również spodobać
Google niedawno przyznał Sundarowi Pichaiemu pakiet wynagrodzenia o wartości 692 milionów dolarów

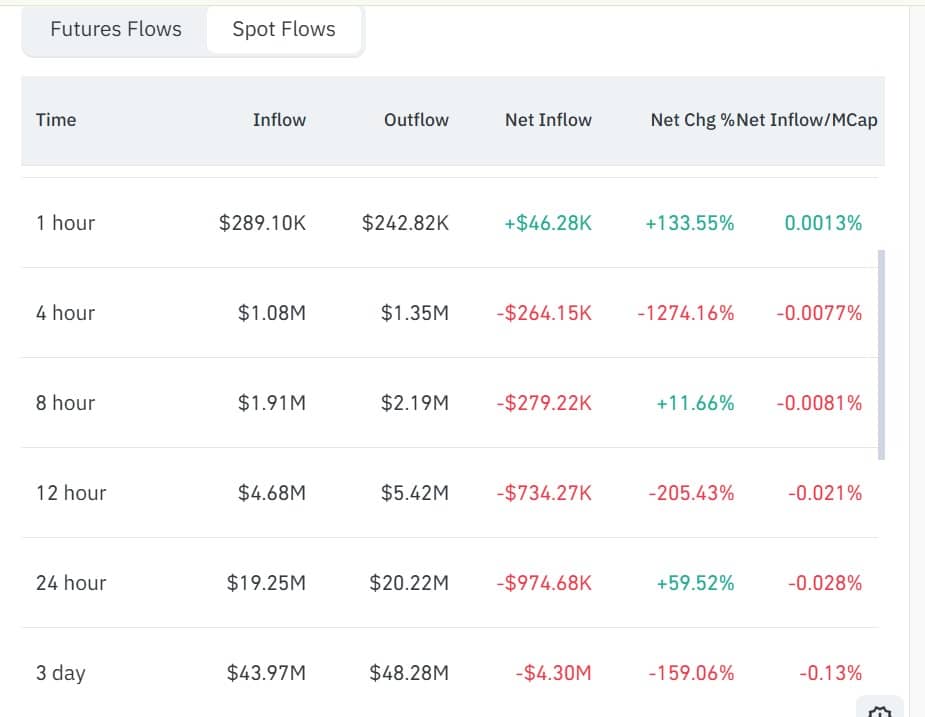
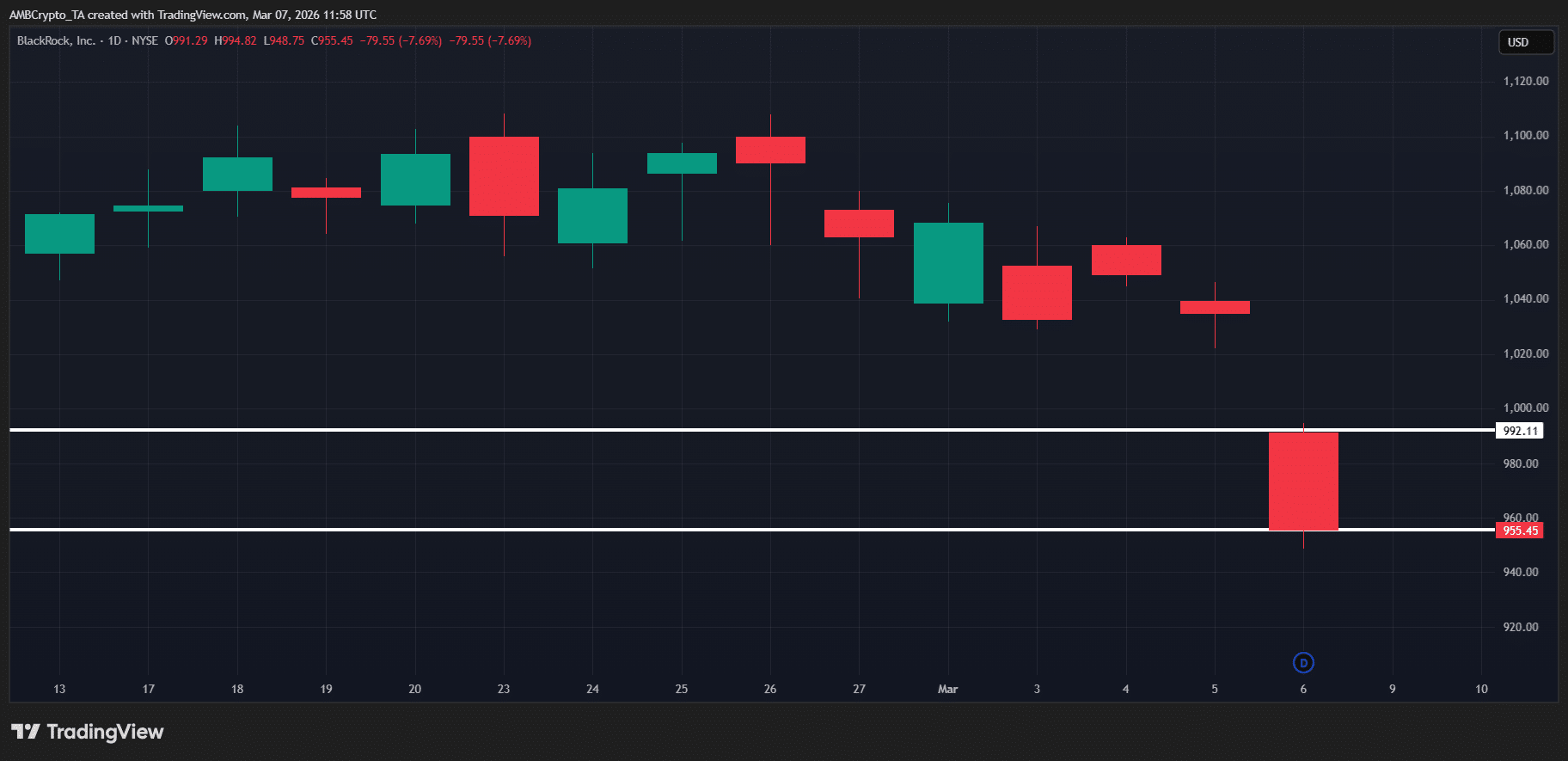
Ostrzeżenie o płynności na 1,2 mld dolarów – Jak BlackRock może wstrząsnąć rynkiem kryptowalut
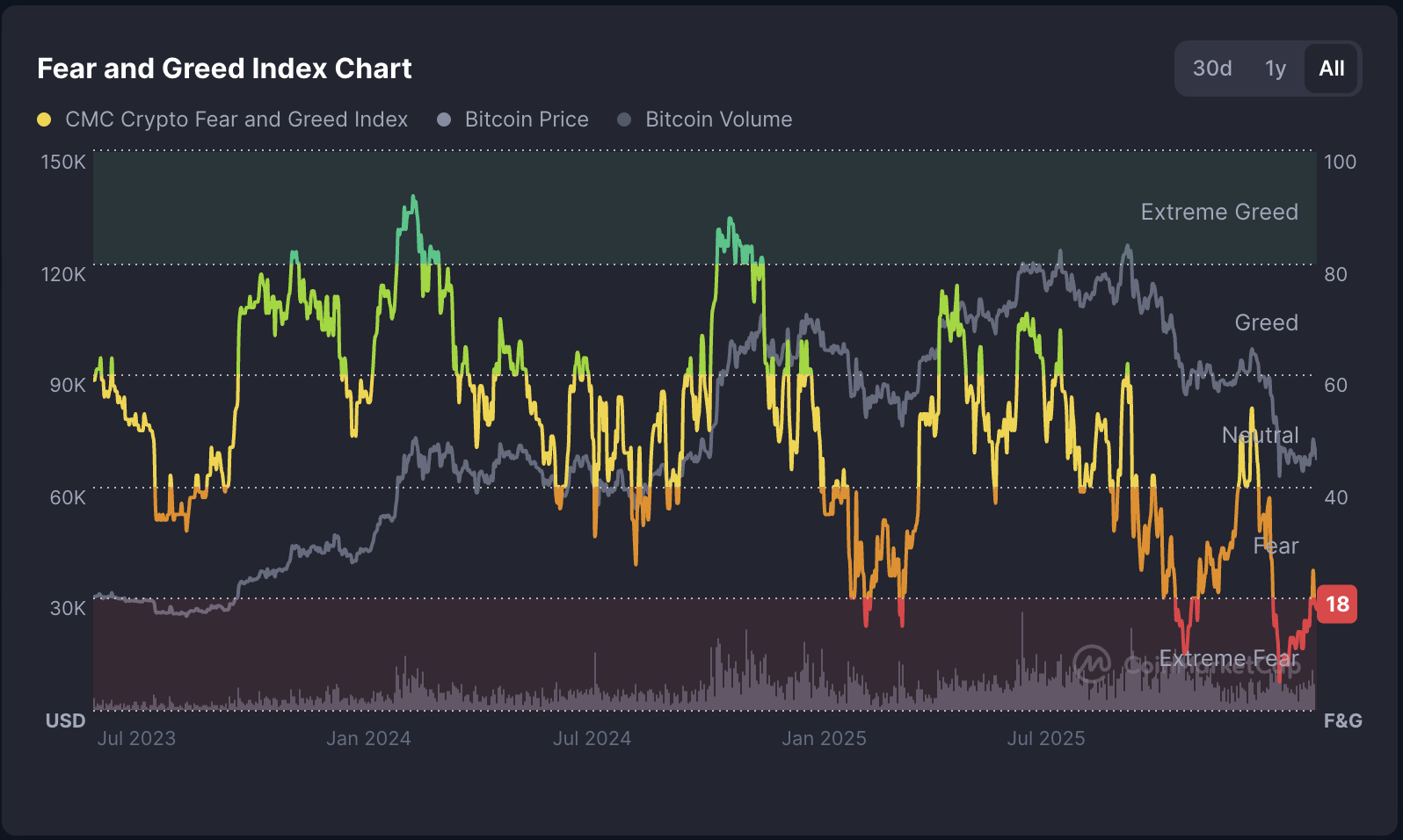
Indeks Strachu i Chciwości Kryptowalut spada z powrotem do poziomów "skrajnego strachu"
Ocena, czy wsparcie Zcash na poziomie 200 dolarów jest zagrożone po spadku ZEC o 8%