Amerykańska Agencja ds. Żywności i Leków (FDA) przyjmuje wniosek o dopuszczenie do obrotu nowego leku (NDA) firmy Teva dotyczący olanzapiny w postaci przedłużonego uwalniania w zawiesinie do wstrzykiwań (TEV-'749) do comiesięcznego leczenia schizofrenii u dorosłych
- Olanzapina o przedłużonym działaniu w postaci zawiesiny do wstrzykiwań (TEV-'749) ma potencjał, by zapewnić skuteczność olanzapiny w comiesięcznej, podskórnej formulacji 1
- Jeśli zostanie zatwierdzony, TEV-'749 może pomóc w zaspokojeniu istotnej niezrealizowanej potrzeby w zakresie dostępnych opcji leczenia schizofrenii poprzez rozwiązanie problemu braku dostępnych formulacji olanzapiny o przedłużonym działaniu 1
- Teva jest zaangażowana w rozwijanie tej innowacyjnej opcji terapeutycznej oraz dalsze budowanie swojej wyróżniającej się linii LAI i przewodnictwa naukowego w złożonych chorobach neurologicznych, realizując swoją strategię Pivot to Growth
PARSIPPANY, N.J. oraz TEL AWIW, Izrael i PARYŻ, 20 lutego 2026 r. (GLOBE NEWSWIRE) -- Teva Pharmaceuticals, amerykańska spółka zależna Teva Pharmaceutical Industries Ltd. (NYSE i TASE: TEVA), oraz Medincell (Euronext: MEDCL), ogłosiły dziś, że Amerykańska Agencja ds. Żywności i Leków (FDA) zaakceptowała ich wniosek o rejestrację nowego leku (NDA) dla olanzapiny o przedłużonym uwalnianiu w postaci zawiesiny do wstrzykiwań (TEV-'749) w leczeniu schizofrenii u dorosłych. TEV-'749 został zaprojektowany w celu poprawy rzeczywistej zgodności z leczeniem i pomocy pacjentom w utrzymaniu długoterminowej stabilności, mając na celu wypełnienie krytycznej luki terapeutycznej dla osób żyjących ze schizofrenią.
Obecnie nie istnieje żadna formulacja olanzapiny o przedłużonym działaniu, która nie wymagałaby od FDA programu oceny i strategii ograniczającej ryzyko (REMS), nakazującej podanie leku w certyfikowanej placówce medycznej oraz trzygodzinny okres obserwacji po wstrzyknięciu. W badaniu fazy 3 SOLARIS, TEV-'749 podawany jako comiesięczny podskórny zastrzyk wykazał profil skuteczności i bezpieczeństwa zgodny z obecnie dostępnymi formulacjami olanzapiny i nie wykazał potrzeby monitorowania po wstrzyknięciu.
„Zgodność z leczeniem pozostaje poważnym wyzwaniem i niezaspokojoną potrzebą wśród osób żyjących ze schizofrenią, w tym wielu korzystających z doustnych form olanzapiny. TEV-'749, nasza eksperymentalna, podskórna olanzapina LAI, może pomóc zapewnić stabilność, oferując sprawdzoną skuteczność i bezpieczeństwo olanzapiny w postaci comiesięcznego leczenia” – powiedział Eric Hughes, MD, PhD, Wiceprezes ds. Globalnych Badań i Rozwoju oraz Dyrektor Medyczny w Teva. „Zbyt długo brak dostępnej formulacji olanzapiny o przedłużonym działaniu ograniczał opcje leczenia dla tych osób i cieszymy się na współpracę z FDA podczas oceny NDA dla TEV-'749, aby pomóc wypełnić tę lukę terapeutyczną.”
„Doustna olanzapina jest jednym z najczęściej przepisywanych leków przeciwpsychotycznych dla osób ze schizofrenią, a ta formulacja o przedłużonym działaniu może lepiej dopasować się do ich życia” – powiedział Christophe Douat, CEO Medincell. „Wraz ze wzrostem doświadczenia z lekami o przedłużonym działaniu, są one coraz częściej uznawane za ważną opcję terapeutyczną w poważnych zaburzeniach psychiatrycznych. Potencjalny zasięg praktycznej opcji o przedłużonym działaniu jest znaczący.”
NDA dla TEV-'749 opiera się na wynikach badania fazy 3 SOLARIS, w tym wynikach z 56. tygodnia oceniających skuteczność, bezpieczeństwo i tolerancję u uczestników w wieku od 18 do 64 lat żyjących ze schizofrenią.
TEV-'749 to badana, comiesięczna podskórna LAI z olanzapiną drugiej generacji – atypowym lekiem przeciwpsychotycznym. Obecnie nie jest zatwierdzony przez żadną instytucję regulacyjną do żadnego zastosowania.
TEV-'749 wykorzystuje SteadyTeq™, technologię kopolimerową zastrzeżoną przez Medincell, która zapewnia kontrolowane, stałe i długotrwałe uwalnianie olanzapiny.
O badaniu podskórnej olanzapiny o przedłużonym działaniu (SOLARIS)
SOLARIS to wielonarodowe, wieloośrodkowe, randomizowane, podwójnie zaślepione, równoległogrupowe, kontrolowane placebo badanie mające na celu ocenę skuteczności, bezpieczeństwa i tolerancji olanzapiny w postaci zawiesiny do wstrzykiwań o przedłużonym uwalnianiu do podskórnego stosowania jako leczenia u pacjentów (w wieku 18–64 lat) ze schizofrenią.
O schizofrenii
Schizofrenia to przewlekłe, postępujące i poważnie wyniszczające zaburzenie psychiczne, które wpływa na sposób myślenia, odczuwania i zachowania.
O Teva
Teva Pharmaceutical Industries Ltd. (NYSE i TASE: TEVA) przekształca się w wiodącą innowacyjną firmę biofarmaceutyczną, wspieraną przez światowej klasy biznes generyczny. Od ponad 120 lat zaangażowanie Teva w poprawę zdrowia nie słabnie. Od innowacji w dziedzinie neurologii i immunologii po dostarczanie złożonych leków generycznych, biopodobnych i marek aptecznych na całym świecie, Teva jest oddana zaspokajaniu potrzeb pacjentów, teraz i w przyszłości. W Teva wszyscy jesteśmy za lepszym zdrowiem. Aby dowiedzieć się więcej, odwiedź
Ostrzeżenie dotyczące oświadczeń dotyczących przyszłości
- Dane w aktach. Parsippany, NJ: Teva Neuroscience, Inc.
- Substance Abuse and Mental Health Services Administration. Schizofrenia. . Dostęp: luty 2026.
- Velligan DI, Rao S. The Epidemiology and Global Burden of Schizophrenia. J Clin Psychiatry. 2023;84(1):MS21078COM5.
- Wander C. (2020). Schizophrenia: Opportunities to Improve Outcomes and Reduce Economic Burden Through Managed Care. The Am J Manag Care. 26(3 Suppl), S62–S68.
- Emsley, R., & Kilian, S. (2018). Efficacy and safety profile of paliperidone palmitate injections in the management of patients with schizophrenia: an evidence-based review. Neuropsychiatric Dis. Treat., 14, 205–223.
- Emsley, R., Chiliza, B., Asmal, L. et al. (2013) The nature of relapse in schizophrenia. BMC Psychiatry 13, 50.
- Andreasen, N. C., et al. (2013). Relapse duration, treatment intensity, and brain tissue loss in schizophrenia: a prospective longitudinal MRI study. The Am J Psychiatry, 170(6), 609–615.
Zapytania medialne Teva:
[email protected]
Zapytania inwestorskie Teva
O Medincell
Medincell jest firmą licencyjną biofarmaceutyczną na etapie badań klinicznych i komercjalizacji, rozwijającą leki o przedłużonym działaniu do wstrzykiwań w wielu obszarach terapeutycznych. Nasze innowacyjne terapie mają na celu zagwarantowanie zgodności z zaleceniami lekarskimi, poprawę skuteczności i dostępności leków oraz zmniejszenie ich śladu środowiskowego. Łączą one substancje czynne z naszą zastrzeżoną technologią BEPO®, która kontroluje dostarczanie leku na poziomie terapeutycznym przez kilka dni, tygodni lub miesięcy po podskórnym lub miejscowym wstrzyknięciu prostego, kilku milimetrowego depozytu, całkowicie bioresorbowalnego. Pierwsze leczenie oparte na technologii BEPO®, przeznaczone do leczenia schizofrenii, zostało zatwierdzone przez FDA w kwietniu 2023 r. i jest obecnie dystrybuowane w Stanach Zjednoczonych przez Teva pod nazwą UZEDY® (technologia BEPO® jest licencjonowana przez Teva pod nazwą SteadyTeq™). Współpracujemy z wiodącymi firmami farmaceutycznymi i fundacjami, aby poprawiać zdrowie na całym świecie poprzez nowe opcje leczenia. Siedziba firmy znajduje się w Montpellier, a Medincell zatrudnia obecnie ponad 140 osób reprezentujących ponad 25 różnych narodowości.
Zastrzeżenie: Treść tego artykułu odzwierciedla wyłącznie opinię autora i nie reprezentuje platformy w żadnym charakterze. Niniejszy artykuł nie ma służyć jako punkt odniesienia przy podejmowaniu decyzji inwestycyjnych.
Może Ci się również spodobać
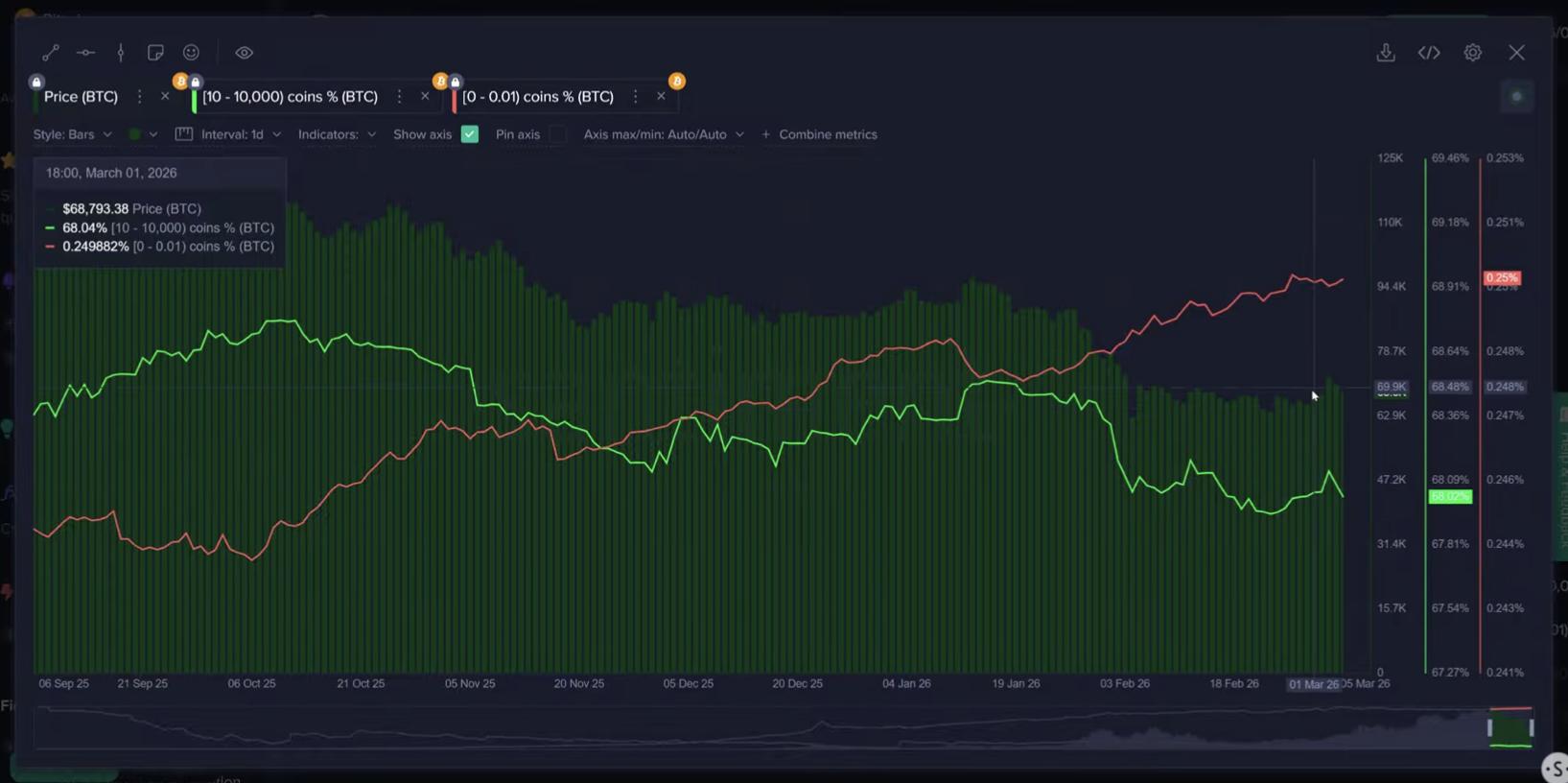
Spadek Bitcoin może się jeszcze nie skończyć, podczas gdy detaliści zwiększają zakupy poniżej 70 tys. dolarów: Santiment
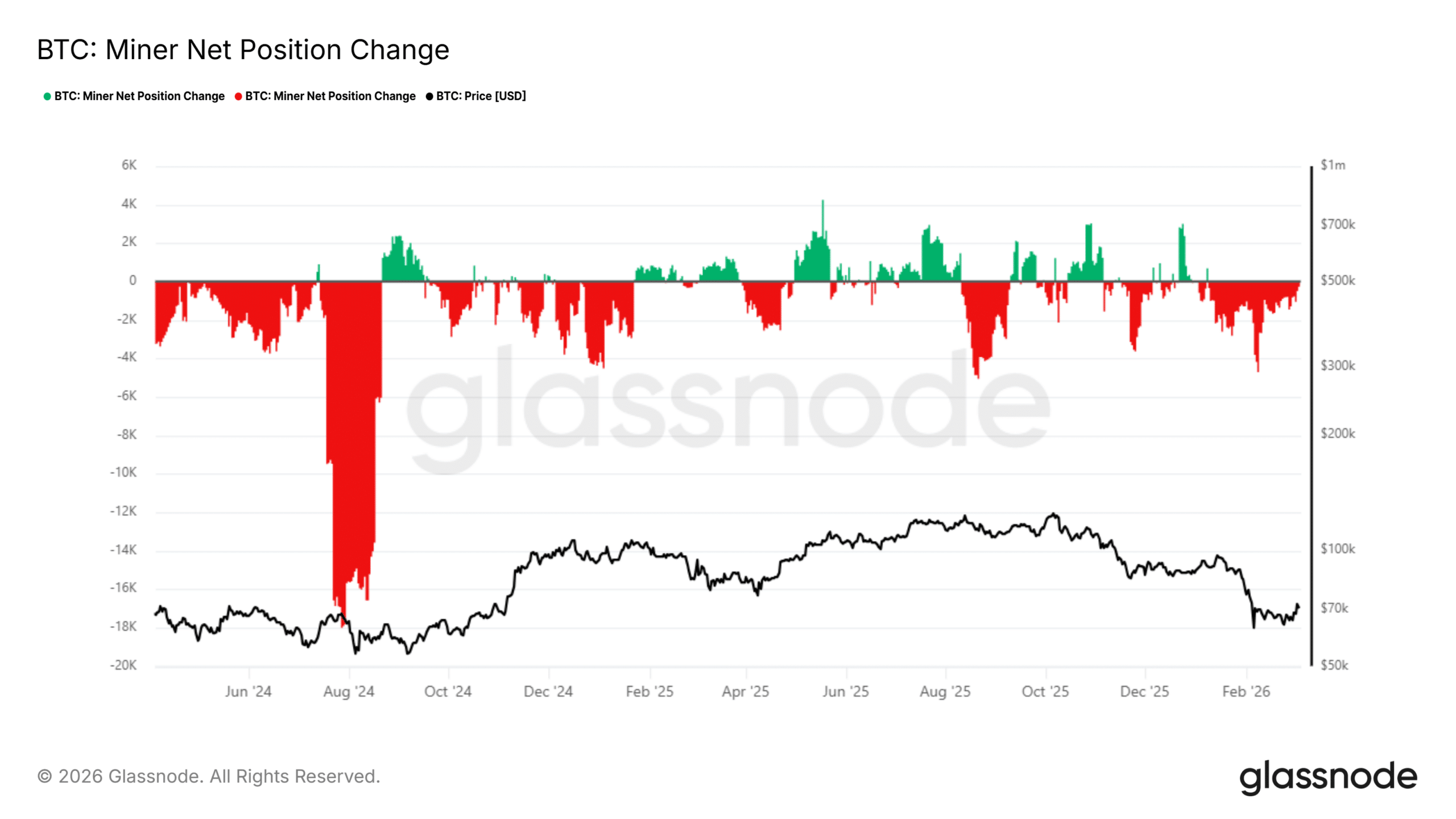
Sprzedaż CleanSpark i Bitcoin miners – czy era HODL wśród górników się kończy?
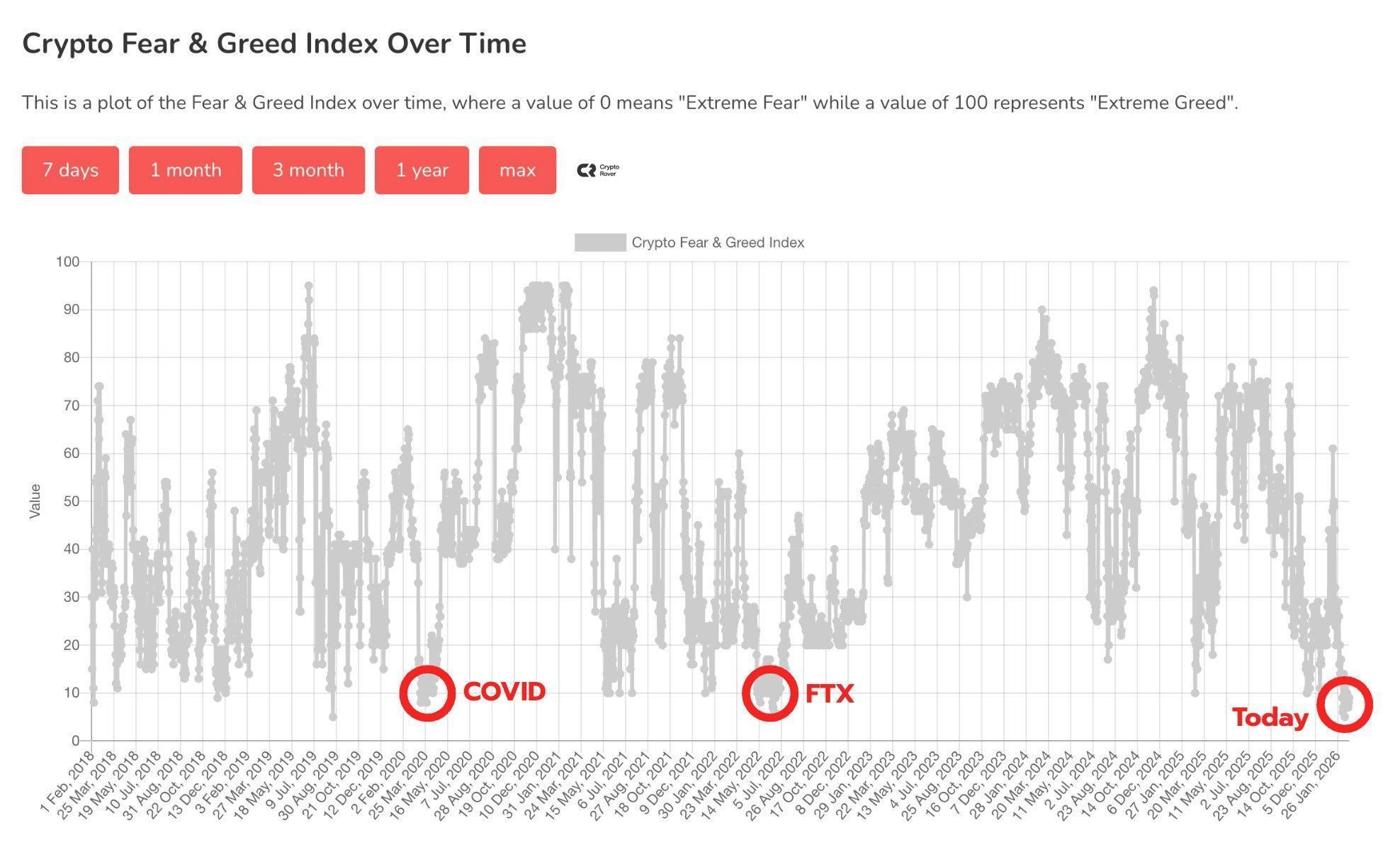
Bitwa byków i niedźwiedzi o 70 tys. dolarów na bitcoinie: jak FOMO może przechylić szalę BTC
Edge AI przedsięwzięcie Lantronix z MediaTek czeka na dowód podczas Embedded World 2026 Challenge

