IBRX firmy ImmunityBio zajmuje 398. miejsce pod względem aktywności handlowej, osiągając wzrost o 0,10%, podczas gdy kluczowe badanie zwiększa optymizm
Przegląd wydajności rynku
26 lutego 2026 roku ImmunityBio (NASDAQ: IBRX) odnotowało spadek wolumenu obrotu do 350 milionów dolarów, co stanowi niemal 59% mniej w porównaniu z poprzednim dniem. Pomimo tak znacznego spadku aktywności, akcje wzrosły o 0,10%, przewyższając szerokie ruchy rynkowe. ImmunityBio zajęło 398. miejsce pod względem wolumenu obrotu wśród notowanych akcji, co wskazuje na nieregularne zaangażowanie inwestorów. Niewielki wzrost ceny akcji nastąpił w warunkach zmiennego nastroju rynkowego – wstępny obrót przed otwarciem giełdy wykazał początkowo silniejsze wzrosty, które później odwróciły się do 3% straty w ciągu dnia.
Główne katalizatory
Kluczowym momentem dla ImmunityBio było zakończenie rekrutacji pacjentów do fazy 2 badania klinicznego QUILT 2.005. Badanie to ocenia skuteczność połączenia ANKTIVA® (nogapendekin alfa inbakicept-pmln) z Bacillus Calmette-Guérin (BCG) w leczeniu raka pęcherza moczowego nieinwazyjnego mięśniowo (NMIBC). Wszyscy z 366 uczestników bez wcześniejszego leczenia BCG zostali zrekrutowani przed planowanym terminem. Analiza pośrednia, na wniosek FDA, wykazała znaczną poprawę: 85% pacjentów otrzymujących połączenie ANKTIVA-BCG utrzymało całkowitą odpowiedź po sześciu miesiącach w porównaniu z 57% w grupie leczonej samym BCG. Po dziewięciu miesiącach wskaźniki odpowiedzi wynosiły odpowiednio 84% i 52%, z istotnością statystyczną (p=0,0455). Nie zidentyfikowano nowych obaw dotyczących bezpieczeństwa, co czyni terapię obiecującą alternatywą dla standardowego leczenia BCG.
Dodatkowo, plan ImmunityBio dotyczący złożenia wniosku o licencję biologiczną (BLA) do FDA w czwartym kwartale 2026 roku jeszcze bardziej zwiększył optymizm. Postępy regulacyjne są kluczowe, ponieważ ANKTIVA posiada już zatwierdzenie w 33 krajach dla NMIBC niewrażliwego na BCG. Wyniki pośrednie wspierają rozszerzenie zastosowania leku na pacjentów bez wcześniejszego leczenia BCG, czyli większą i wcześniejszą grupę. Analitycy uważają, że zatwierdzenie przez organy regulacyjne może uczynić ANKTIVA kluczowym graczem w rozwijającym się leczeniu raka pęcherza moczowego, zwłaszcza biorąc pod uwagę ograniczenia BCG, takie jak oporność i zwiększone ryzyko przerzutów w przypadku opóźnienia cystektomii.
Ponadto ImmunityBio zajmuje się niedoborami BCG poprzez swój Program Rozszerzonego Dostępu (EAP) dla rekombinowanego BCG. Z 580 pacjentami zarejestrowanymi w całych Stanach Zjednoczonych, EAP ma na celu rozwiązanie trwającego niedoboru TICE® BCG. Firma prowadzi również rozmowy z FDA na temat zatwierdzenia rekombinowanego BCG jako alternatywy, co mogłoby złagodzić ograniczenia podaży i wesprzeć szersze przyjęcie terapii skojarzonej. Podejście to podkreśla zaangażowanie ImmunityBio zarówno w innowacje medyczne, jak i stabilność łańcucha dostaw.
Stonowany ruch cen akcji, pomimo zachęcających wyników klinicznych, może sygnalizować ostrożność inwestorów wobec danych pośrednich i barier regulacyjnych. Chociaż analiza FDA potwierdza skuteczność terapii, ostateczne wyniki – spodziewane pod koniec 2026 roku – pozostają kluczowym czynnikiem. Spadek o 3% na rynku przed otwarciem sugeruje, że inwestorzy obawiają się, iż wyniki pośrednie nie gwarantują trwałego sukcesu. Niemniej jednak, ostatnie wyniki finansowe ImmunityBio, w tym 431% wzrost sprzedaży ANKTIVA rok do roku do 38,3 mln dolarów, zapewniają impet. Warunkowe zatwierdzenie przez Komisję Europejską dla NMIBC niewrażliwego na BCG dodatkowo wzmacnia pozycję firmy.
Perspektywy inwestorów i przyszłe możliwości
Kombinacja osiągnięć klinicznych, inicjatyw regulacyjnych i strategii łańcucha dostaw wpływa na nastroje inwestorów. Chociaż zmniejszony wolumen obrotu wskazuje na krótkoterminową zmienność, postępy w badaniu QUILT 2.005 i nadchodzące złożenie BLA wyznaczają jasną ścieżkę wzrostu. Analitycy nadal rekomendują „Kupuj”, a docelowe ceny akcji wahają się od 12,60 do 23,00 dolarów, co odzwierciedla zaufanie do platformy BioShield ImmunityBio oraz jej potencjału do zaspokojenia niezaspokojonych potrzeb w leczeniu raka pęcherza moczowego. Wraz ze zbliżającym się złożeniem BLA inwestorzy będą uważnie obserwować reakcję FDA i ostateczne wyniki badań, aby ocenić komercyjną opłacalność terapii.
Zastrzeżenie: Treść tego artykułu odzwierciedla wyłącznie opinię autora i nie reprezentuje platformy w żadnym charakterze. Niniejszy artykuł nie ma służyć jako punkt odniesienia przy podejmowaniu decyzji inwestycyjnych.
Może Ci się również spodobać
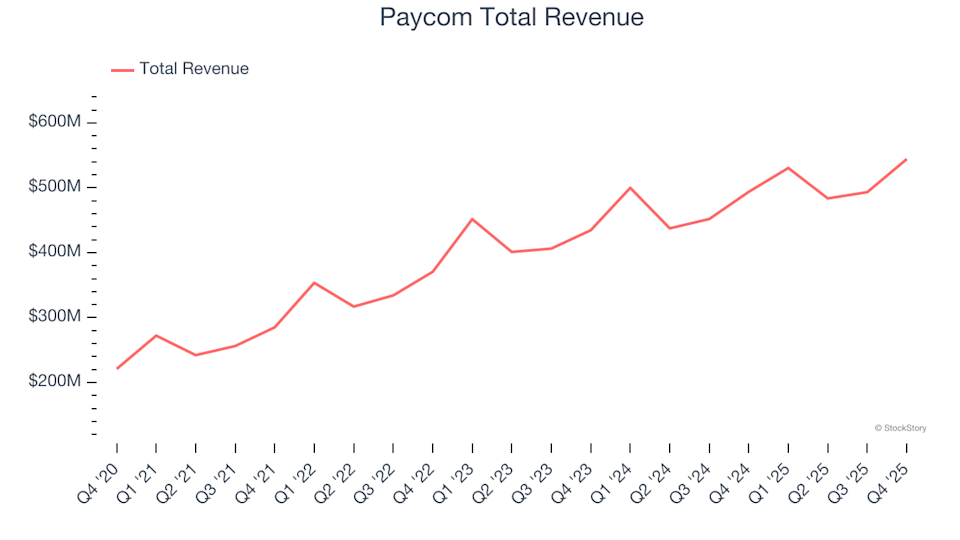
Przegląd wyników za IV kwartał spółek z branży oprogramowania HR: porównanie Paycom (NYSE:PAYC) z konkurentami
Podział sektorowy Wedbush: arbitraż oczekiwań w AppLovin, Unity i Playtika