DNLI odnotowuje w IV kwartale mniejszą niż oczekiwano stratę, uwaga skupiona na leczeniu zespołu Huntera
Przegląd finansowy Denali Therapeutics za IV kwartał 2025 r.
Denali Therapeutics (DNLI) odnotowało w czwartym kwartale 2025 roku stratę netto na akcję w wysokości 0,73 USD, co było nieco lepszym wynikiem od konsensusu zakładającego stratę na poziomie 0,75 USD. Dla porównania, w analogicznym okresie ubiegłego roku strata wyniosła 0,67 USD na akcję.
Roczny wzrost straty na akcję był przede wszystkim spowodowany wyższymi kosztami operacyjnymi.
Ponieważ Denali nie posiada jeszcze produktów na rynku, jej przychody ograniczają się do środków pozyskiwanych w ramach trwających partnerstw. W raportowanym kwartale spółka nie odnotowała żadnych przychodów z tytułu współpracy, co było poniżej oczekiwanych 18 milionów dolarów.
W ciągu ostatniego roku akcje DNLI wzrosły o 13,4%, przewyższając sektor medyczny, biomedyczny i genetyczny, który odnotował wzrost o 11,5%.
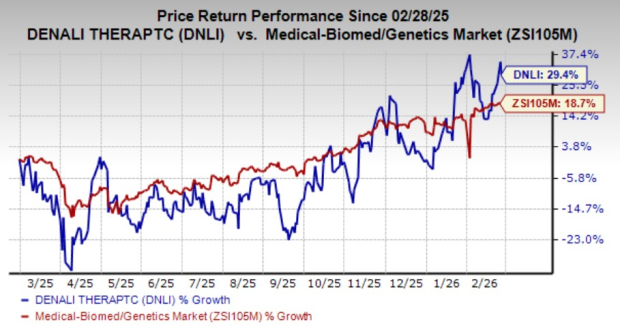
Źródło: Zacks Investment Research
Kluczowe punkty z wyników za IV kwartał
- Koszty badań i rozwoju spadły o 1,9% do 97,9 mln USD, głównie ze względu na niższe wydatki na projekty dotyczące małych cząsteczek.
- Koszty ogólne i administracyjne wzrosły o 31,3% do 39,5 mln USD, co odzwierciedla przygotowania do planowanego wprowadzenia tividenofusp alfa na rynek.
- Na dzień 31 grudnia 2025 r. Denali posiadała około 966,2 mln USD w gotówce, ekwiwalentach gotówki i papierach wartościowych.
Podsumowanie roku 2025
- W 2025 roku nie wygenerowano żadnych przychodów.
- Roczna strata na akcję wzrosła do 2,97 USD w porównaniu do 2,57 USD w 2024 roku.
Postępy w zakresie wiodącego kandydata na lek
Denali aktywnie przygotowuje się do komercyjnego wprowadzenia swojego głównego produktu, tividenofusp alfa.
Wniosek o pozwolenie na dopuszczenie do obrotu produktów biologicznych (BLA) dla tividenofusp alfa, mający na celu leczenie mukopolisacharydozy typu II (zespół Huntera), jest obecnie rozpatrywany przez amerykańskich regulatorów.
FDA przedłużyła termin rozpatrzenia wniosku z 5 stycznia 2026 r. na 5 kwietnia 2026 r.
Tividenofusp alfa uzyskał od FDA kilka oznaczeń, w tym Breakthrough Therapy, Fast Track, Orphan Drug oraz status leku na rzadkie choroby pediatryczne.
Ta eksperymentalna terapia została zaprojektowana w celu dostarczenia enzymu iduronate-2-sulfatase (IDS) przez barierę krew-mózg, docierając zarówno do ciała, jak i mózgu.
Okres analizy BLA został wydłużony po tym, jak Denali dostarczyło zaktualizowane dane z zakresu farmakologii klinicznej na żądanie FDA. Firma wyjaśniła, że aktualizacja ta nie dotyczyła skuteczności, bezpieczeństwa ani biomarkerów.
FDA zakwalifikowała zgłoszenie jako istotną poprawkę, co skutkowało przedłużeniem terminu rozpatrzenia.
Trwające globalne badanie fazy II/III COMPASS ma dostarczyć dodatkowych dowodów dla zgłoszeń regulacyjnych na całym świecie; rekrutacja do kohorty neuronopatycznej (Kohorta A) zakończyła się w grudniu 2025 r.
Rozwój portfolio badawczego
- Denali bada DNL126 w leczeniu zespołu Sanfilippo typu A (MPS IIIA). Wstępne wyniki fazy I/II zaprezentowane podczas WORLDSymposium wykazały znaczące obniżenie kluczowych biomarkerów choroby oraz profil bezpieczeństwa zbliżony do istniejących terapii enzymatycznych. Wyniki te mogą wspierać przyspieszoną ścieżkę zatwierdzenia, a planowane jest badanie potwierdzające fazy III.
- Inni kandydaci z portfolio są rozwijani we współpracy z Takeda (TAK), Biogen (BIIB) i Sanofi (SNY).
- Denali i Takeda rozwijają DNL593 jako potencjalne leczenie otępienia czołowo-skroniowego związanego z mutacją granulinową (FTD-GRN). Zakończono rekrutację do badania fazy I/II, w którym uczestniczy 40 osób. Początkowe dane kliniczne spodziewane są w 2026 roku.
- Denali niedawno otrzymała zgodę na badanie fazy Ib DNL628, a przygotowania są w toku.
- Denali i Biogen wspólnie rozwijają BIIB122. Biogen prowadzi globalne badanie fazy IIb LUMA dla wczesnego stadium choroby Parkinsona – wyniki spodziewane są w połowie 2026 roku. Denali prowadzi badanie fazy IIa BEACON oceniające inhibicję LRRK2 w chorobie Parkinsona związanej z mutacją LRRK2.
- W październiku Denali złożyła IND dla DNL952 (ETV:GAA) w celu rozpoczęcia badań klinicznych w chorobie Pompego. FDA zniosła tymczasowe wstrzymanie badań klinicznych, a przygotowania do badania fazy I są kontynuowane.
- Sanofi rozwija eclitasertib w leczeniu umiarkowanego do ciężkiego wrzodziejącego zapalenia jelita grubego, a wyniki fazy II spodziewane są w pierwszej połowie roku.
Analiza perspektyw Denali
Zatwierdzenie tividenofusp alfa mogłoby znacząco poprawić trajektorię wzrostu Denali. Obiecujące są również postępy z DNL126.
Silne rezerwy gotówkowe firmy podkreślają jej zdolność do wspierania dalszych prac badawczo-rozwojowych.
Zastrzeżenie: Treść tego artykułu odzwierciedla wyłącznie opinię autora i nie reprezentuje platformy w żadnym charakterze. Niniejszy artykuł nie ma służyć jako punkt odniesienia przy podejmowaniu decyzji inwestycyjnych.
Może Ci się również spodobać
XRP osiąga kluczowy poziom po raz trzeci w ciągu 10 lat. Oto, na co zwrócić uwagę
Właściciel Daily Mirror ponosi największą stratę od dziesięciu lat w związku ze spadkiem ruchu z Google

Nowo mianowany CEO Target ujawnia swoją strategię ożywienia firmy

Opcje Dochód Dzienny: MU, SOFI, CRWV i więcej

