Cyclerion Therapeutics объявляет о прогрессе в подготовке к исследованию доказательства концепции CYC-126 фазы 2 с учетом отзывов FDA и формированием клинического консультативного совета
–Получен положительный письменный отзыв по предварительной заявке на исследование нового лекарственного препарата (“IND”) от Управления по санитарному надзору за качеством пищевых продуктов и медикаментов США (“FDA”)–
–В Клинико-совещательный совет (“CAB”) входят ключевые лидеры в области нейропсихиатрии, анестезиологии и клинической разработки–
–Остаемся на пути к запуску исследования доказательства концепции (“POC”) II фазы CYC-126 при лечении депрессии, устойчивой к терапии (“TRD”), во втором полугодии 2026 года–
КЕМБРИДЖ, штат Массачусетс, 17 февраля 2026 г. (GLOBE NEWSWIRE) -- Cyclerion Therapeutics, Inc. (Nasdaq: CYCN) (“Cyclerion” или "Компания"), биофармацевтическая компания, занимающаяся разработкой инновационных нейропсихиатрических терапий, сегодня объявила о получении положительного письменного регуляторного отзыва и ответов от FDA относительно исследования II фазы POC CYC-126 при TRD и пути к потенциальному утверждению препарата. CYC-126 — это потенциально новый исследуемый препарат на основе анестетика, который включает в себя обратную связь в реальном времени по данным электроэнцефалограммы (“EEG”) и разрабатывается для лечения TRD. CYC-126 разработан как индивидуализированный, точно дозируемый подход, сочетающий хорошо изученные анестетики с мониторингом EEG в реальном времени и алгоритмически управляемым дозированием. Cyclerion считает, что такая стратегия может позволить врачам более точно направлять пациентов к целевым состояниям мозга, ассоциированным с антидепрессивным эффектом, что позволит восполнить значительный неудовлетворенный спрос среди пациентов с TRD, нуждающихся в альтернативных терапевтических вариантах.
Планируемое исследование — это рандомизированное, двойное слепое, двухчастное (Часть A и Часть B) клиническое исследование оценки CYC-126 у взрослых с TRD, которые являются кандидатами на контролируемую анестезию. Участники будут рандомизированы в группы активного лечения или фиктивного контроля для оценки безопасности, антидепрессивной эффективности и долгосрочности ответа. В исследовании будут использоваться клинические конечные точки, принятые FDA, включая шкалу оценки депрессии Монтгомери – Асберг (MADRS).
CYC-126 будет регулироваться Центром оценки и исследования лекарственных средств FDA (“CDER”), при этом Центр по устройствам и радиологическому здоровью (“CDRH”) FDA будет предоставлять консультации и рецензирование по мере необходимости. Отзыв FDA дал четкие инструкции, которые, по мнению Компании, помогут обеспечить успешную подачу IND в FDA. FDA поддержало продолжение разработки запланированного дизайна исследования II фазы с использованием одобренных FDA анестетиков и их хорошо изученных доклинических и клинических данных по безопасности. В результате Компания сохраняет планы начать исследование II фазы во втором полугодии 2026 года, при этом первый пациент будет набран в Австралии, а набор в США начнется в первой половине 2027 года.
«Мы довольны конструктивным отзывом, полученным от FDA, который дает дополнительную ясность в отношении регуляторной юрисдикции и пути разработки CYC-126», — сказала Регина Граул, Ph.D., президент и главный исполнительный директор Cyclerion. — «Это согласование поддерживает наши планы подачи IND и подтверждает ключевые элементы предлагаемого дизайна исследования II фазы. Мы ценим продолжающееся взаимодействие с соответствующими подразделениями FDA и считаем, что эти рекомендации станут важной основой для продвижения CYC-126 с целью удовлетворения значительных неудовлетворенных потребностей пациентов с TRD».
Cyclerion также объявила о формировании Клинико-совещательного совета с назначением пяти всемирно признанных лидеров в области нейропсихиатрии, анестезиологии, клинической практики и клинической разработки. CAB будет оказывать стратегическую поддержку и помогать в ключевых решениях по клинической разработке по мере продвижения CYC-126 для TRD и формирования портфеля исследований по нейропсихиатрическим заболеваниям. Пять членов CAB:
- Доктор Хуссейни Манджи, M.D., FRCPC: всемирно признанный лидер в области нейронауки и инноваций в психическом здоровье. В его выдающуюся карьеру входят руководящие должности в Национальных институтах здоровья США, где он продвигал фундаментальные исследования синаптической пластичности, и в Janssen/Johnson & Johnson, где он был глобальным главой по нейронауке, возглавляя разработку новых методов лечения расстройств настроения. В настоящее время он является профессором Оксфордского и Йельского университетов, специализируется на тяжелых нейропсихиатрических расстройствах, и членом Национальной академии медицины. Доктор Манджи широко признан лидером мнений в области политики и инноваций психического здоровья, имеет сотни рецензируемых публикаций и значительный опыт внедрения научных достижений в трансформационные терапии. Доктор Манджи получил степень бакалавра биохимии и M.D. в Университете Британской Колумбии. После ординатуры прошел стажировку в Национальном институте психического здоровья и получил дополнительное образование по клеточной и молекулярной биологии в Национальном институте диабета, болезней органов пищеварения и почек.
- Доктор Линда Карпентер, M.D.: профессор психиатрии и поведения человека Медицинской школы Альперта при Университете Брауна и медицинский директор программы исследований мозга и интервенционной нейротерапии (BRaIN) в больнице Батлер. Она основала клинику TMS Батлер и исследовательскую лабораторию нейромодуляции, где проводит клинические испытания и механистические исследования при расстройствах настроения и тревожности. Ее работа поддержана множеством грантов промышленности и федеральных структур. Она опубликовала более 200 научных статей, включая отчеты клинических испытаний по стимуляции блуждающего нерва, глубокой стимуляции мозга, транскраниальной магнитной стимуляции (“TMS”) и других устройствах нейростимуляции. Доктор Карпентер занимала руководящие и наставнические должности в ряде национальных научных и профессиональных организаций, включая Общество клинической TMS, Американскую психиатрическую ассоциацию, Американский колледж нейропсихофармакологии и Общество биологической психиатрии. Доктор Карпентер получила степень M.D. в Университете Пенсильвании, прошла стажировку по внутренним болезням, ординатуру по психиатрии и исследовательскую клиническую стипендию по нейронаукам в Йельском университете.
- Доктор Лоренс Оланофф, M.D., Ph.D.: адъюнкт-профессор Медицинского университета Южной Каролины и партнер Good Life Sciences Ventures. С 2006 по 2010 годы был президентом и главным операционным директором Forest Laboratories, Inc. С 2005 по 2006 годы доктор Оланофф занимал пост генерального директора Celsion Corporation. До 2005 года он был исполнительным вице-президентом по исследованиям и разработкам и главным научным сотрудником Forest Laboratories, а также занимал руководящие должности в клинических исследованиях Sandoz Pharmaceutical Corporation и Upjohn Company. За свою карьеру в фармацевтической разработке доктор Оланофф внес значительный вклад в получение тридцати новых одобрений лекарств, как новых химических соединений, так и дополнительных показаний, в различных терапевтических областях. Он является членом советов директоров Ichnos Glenmark Innovation, Tevard Biosciences и Leukogene Therapeutics, а также ряда некоммерческих организаций. Ранее входил в советы директоров Forest Laboratories, Ironwood Pharmaceuticals, Axovant Sciences Ltd. и Celsion Corporation. Доктор Оланофф получил степень Ph.D. по биомедицинской инженерии и M.D. в Университете Кейс Вестерн Резерв, проходил ординатуру по внутренним болезням и стипендию по клинической фармакологии в Медицинском университете Южной Каролины и автор более 40 научных публикаций по контролируемой доставке лекарств, фармакокинетике, метаболизму лекарств и клинической токсикологии.
- Доктор Юрий Бронштейн, M.D.: врач-реаниматолог (интенсивист) и анестезиолог в системе здравоохранения Университета Дьюка, а также доцент Медицинской школы Университета Дьюка. Получил степень M.D. в Медицинской школе Университета Вандербильта и прошел интернатуру и ординатуру по анестезиологии в Массачусетской общей больнице (MGH) / Гарвардской медицинской школе (HMS). Затем прошел стажировку по медицине критических состояний в MGH/HMS. Обладает шестью действующими сертификатами совета по трем различным клиническим направлениям — медицине критических состояний, анестезиологии и эхокардиографии, а также является членом Американского общества эхокардиографии. Доктор Бронштейн также занимал несколько руководящих должностей местного, национального и международного уровня, связанных с диагностическим ультразвуком.
- Доктор Лейбен С. Лестер, M.D.: кардиолог-анестезиолог и врач неотложной медицины в Johns Hopkins Medicine, а также ассистент-профессор анестезиологии и медицины критических состояний в Медицинской школе Университета Джонса Хопкинса. Доктор Лестер получил степень M.D. в Медицинской школе Калифорнийского университета в Сан-Франциско, прошел ординатуру по неотложной медицине в Центре медицинских наук Университета Нью-Мексико и ординатуру (где был старшим ординатором) и стажировку по анестезиологии и медицине критических состояний и кардиологической анестезиологии в Johns Hopkins. Сертифицирован по анестезиологии, взрослой кардиологической анестезиологии, неотложной медицине и периоперационной чреспищеводной эхокардиографии. Его академические интересы включают управление дыхательными путями, седацию процедур у пациентов высокого риска и фармакологию анестетиков, а также ультразвук и 3D-эхокардиографию. Он активно участвует в разработке медицинских устройств и имеет несколько патентов в процессе рассмотрения или уже выданных. В настоящее время он получает грант NIH R61/R33 на разработку фотоакустических игл для ультразвукового контроля сосудистого доступа со своей исследовательской командой.
«Для нас большая честь принять в свой Клинико-совещательный совет такую выдающуюся группу клинических экспертов», — сказала Регина Граул. — «Эти выдающиеся лидеры приносят мощное сочетание экспертизы в области нейропсихиатрии, анестезиологии и клинической разработки, что поможет направлять продвижение CYC-126 и информировать о дальнейшем расширении нашего исследовательского портфеля. Их взгляды и рекомендации сыграют критическую роль в формировании нашей клинической стратегии и обеспечат самые высокие стандарты научной строгости на этом важнейшем этапе развития Компании, направленном на предоставление инновационных терапевтических решений пациентам с депрессией, устойчивой к лечению, и в других сферах с высоким неудовлетворенным спросом».
В дополнение к получению ценных отзывов от FDA и формированию CAB, Cyclerion продолжила продвижение своих клинических разработок, включая выбор контрактной исследовательской организации для поддержки проведения планируемого многонационального исследования. Компания сохраняет планы по запуску исследования доказательства концепции II фазы CYC-126 при депрессии, устойчивой к терапии, во втором полугодии 2026 года.
О компании Cyclerion Therapeutics
Cyclerion — биофармацевтическая компания, ориентированная на разработку терапии для нейропсихиатрических заболеваний. Основной продукт Компании — индивидуализированная терапия CYC-126 для TRD, состояния с существенными неудовлетворенными медицинскими потребностями и значительным коммерческим потенциалом. Компания считает, что эта программа может стать краеугольным камнем ее будущего роста.
Источник: Cyclerion Therapeutics, Inc.
Дисклеймер: содержание этой статьи отражает исключительно мнение автора и не представляет платформу в каком-либо качестве. Данная статья не должна являться ориентиром при принятии инвестиционных решений.
Вам также может понравиться
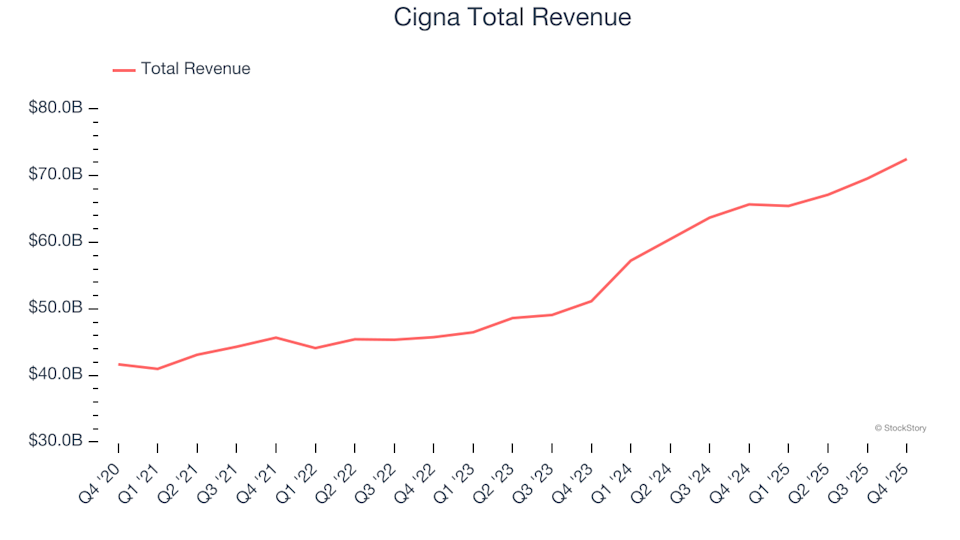
Обзор акций поставщиков медицинского страхования за 4 квартал: сравнение Cigna (NYSE:CI)
Восстановления Bitcoin пока недостаточно для крупных майнинговых компаний

Криптовалютные фонды получили 619 млн долларов на фоне стабильности рынков несмотря на опасения из-за нефти и войны