Telix reicht europäischen Zulassungsantrag für TLX101-Px zur Bildgebung bei Hirntumoren ein
MELBOURNE, Australien und INDIANAPOLIS, 18. Februar 2026 (GLOBE NEWSWIRE) -- Telix Pharmaceuticals Limited (ASX: TLX, NASDAQ: TLX, „Telix“) gibt heute bekannt, dass es einen Antrag auf Marktzulassung (MAA) in Europa für TLX101-Px (O-(2-[
Telix hat die europäischen und US-amerikanischen Zulassungspakete für TLX101-Px parallel vorbereitet, um die europäische Einreichung zu einem vereinbarten Termin vorzuziehen und dabei Aspekte des US-amerikanischen Food and Drug Administration (FDA)-Pakets zur Unterstützung des zusätzlichen Antrags abzustimmen. Die Einreichung umfasst die wichtigsten europäischen Märkte
In Europa wird die Positronen-Emissions-Tomographie (PET) von Gliomen mit
Philipp Lohmann, Gruppenleiter Digitale Translationale Neurobildgebung am Forschungszentrum Jülich in Deutschland, kommentierte: „FET-PET-Bildgebung wird bereits in der klinischen Praxis in Europa zur Beurteilung von Gliomen eingesetzt und spielt eine entscheidende Rolle bei der Therapieentscheidung. Dies gilt insbesondere im posttherapeutischen Setting, wo die konventionelle MRT
Kevin Richardson, Chief Executive Officer, Telix Precision Medicine, ergänzte: „Wir sehen in Europa eine überzeugende Chance, den Zugang zu zugelassenen, zielgerichteten Radiopharmazeutika für die Bildgebung und Therapie von Hirntumoren zu erweitern. Somit ist diese Einreichung ein wichtiger Meilenstein für Telix. Der strategische Wert dieser Einreichung ist besonders relevant, um eine weit verbreitete Gliom-Bildgebung als Teil unseres entsprechenden therapeutischen Entwicklungsprogramms zu etablieren. Wir konnten Aspekte unseres FDA-Pakets nutzen, um die europäische Einreichung zu beschleunigen, die gemäß eines mit der Aufsichtsbehörde vereinbarten Termins eingereicht wurde, wobei die US-amerikanische Einreichung folgen wird.“
Über Gliome in Europa
In Europa werden jedes Jahr etwa 67.500 Tumoren des Gehirns und des zentralen Nervensystems diagnostiziert
Über TLX101-Px
TLX101-Px (O-(2-[
Über Telix Pharmaceuticals Limited
Telix ist ein biopharmazeutisches Unternehmen, das sich auf die Entwicklung und Vermarktung von therapeutischen und diagnostischen Radiopharmazeutika sowie zugehörigen Medizintechnologien konzentriert. Telix hat seinen Hauptsitz in Melbourne, Australien, mit internationalen Niederlassungen in den Vereinigten Staaten, Großbritannien, Brasilien, Kanada, Europa (Belgien und Schweiz) und Japan. Telix entwickelt ein Portfolio von Produkten in klinischer und kommerzieller Phase, das darauf abzielt, signifikante ungedeckte medizinische Bedürfnisse in der Onkologie und bei seltenen Krankheiten zu adressieren. Telix ist an der Australian Securities Exchange (ASX: TLX) und am Nasdaq Global Select Market (NASDAQ: TLX) notiert.
Telix Investor Relations (Global)
Frau Kyahn Williamson
Telix Pharmaceuticals Limited
SVP Investor Relations and Corporate Communications
E-Mail: [email protected]
Diese Mitteilung wurde zur Veröffentlichung durch das Disclosure Committee von Telix Pharmaceuticals Limited im Namen des Vorstands genehmigt.
Rechtliche Hinweise
Haftungsausschluss: Der Inhalt dieses Artikels gibt ausschließlich die Meinung des Autors wieder und repräsentiert nicht die Plattform in irgendeiner Form. Dieser Artikel ist nicht dazu gedacht, als Referenz für Investitionsentscheidungen zu dienen.
Das könnte Ihnen auch gefallen
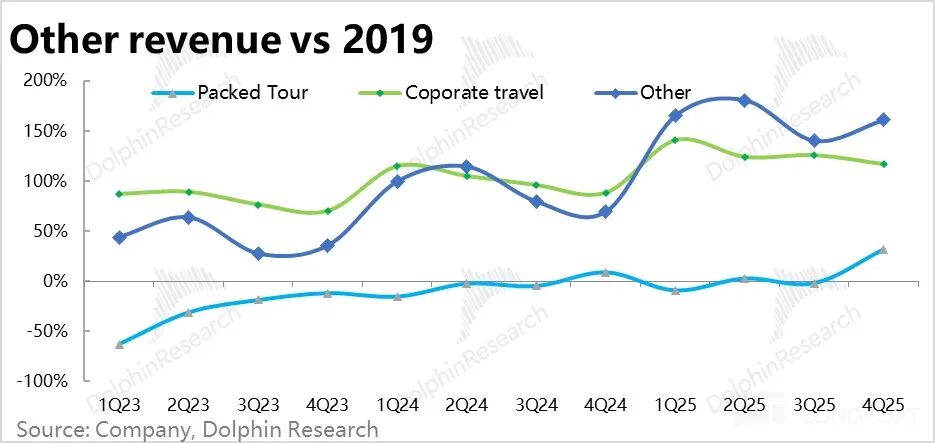
Trip.com: Kann es nach dem „harten Regulierungsschlag“ noch „klein, aber fein“ sein?

Die Haushaltsverschuldung überwältigt die Menschen in den USA. So können Sie darauf reagieren
Händler, LayerZero wird bullisch – ZRO visiert 2,00 $ an, aber DIESE Risiken bleiben