Humacyte kündigt Präsentation der langfristigen Sicherheits- und Wirksamkeitsergebnisse von Symvess auf dem VESS-Treffen an
- Daten präsentiert auf dem Annual Winter Meeting 2026 der Vascular & Endovascular Surgery Society -
- Nach bis zu 36 Monaten Nachbeobachtung zeigten Patienten mit arteriellen Extremitätenverletzungen hohe Raten an Gliedmaßenerhalt, niedrige Infektionsraten und keine unbegründeten strukturellen Ausfälle -
- Langzeitergebnisse zur Haltbarkeit zeigten weder Dilatation noch Verengung des Symvess-Durchmessers bis zu 36 Monaten -
DURHAM, N.C., 18. Februar 2026 (GLOBE NEWSWIRE) -- Humacyte, Inc. (Nasdaq: HUMA), ein biotechnologisches Plattformunternehmen im kommerziellen Stadium, das universell implantierbare, bioengineerte menschliche Gewebe im industriellen Maßstab entwickelt, gab heute die Präsentation von Langzeitdaten zur Haltbarkeit von Symvess bei Patienten mit arteriellen Extremitätenverletzungen auf dem Annual Winter Meeting 2026 der Vascular & Endovascular Surgery Society (VESS) in Olympic Valley, Kalifornien, bekannt.
Die Präsentation mit dem Titel „Langzeitergebnisse des azellulären, gewebetechnisch hergestellten Gefäßes bei der Reparatur arterieller Extremitätenverletzungen: Ergebnisse der V005-Studie“ wurde von Michael Curi, MD, MPA, Leiter der Gefäßchirurgie, stellvertretender Vorsitzender der Chirurgieabteilung und außerordentlicher Professor für Chirurgie an der Rutgers – New Jersey Medical School gehalten. In der V005-Studie bewahrte Symvess seine langfristige strukturelle Integrität, zeigte niedrige Infektionsraten und ermöglichte hohe Raten an Gliedmaßenerhalt bei Patienten, die bis zu 36 Monate nachbeobachtet wurden.
„Diese Langzeitergebnisse belegen das Potenzial von Symvess, den Bedürfnissen von Traumapatienten gerecht zu werden, wenn die Verwendung einer autologen Vene nicht möglich oder praktikabel ist“, sagte Dr. Curi. „Während der V005-Studie gab es anhaltend niedrige Infektionsraten, keine conduit-bedingten Todesfälle und eine ausgezeichnete Haltbarkeit von Symvess über drei Jahre – Ergebnisse, die sich in bedeutenden Vorteilen für Patienten niederschlagen, die mit lebens- oder gliedmaßengefährdenden Verletzungen konfrontiert sind, bei denen eine autologe Rekonstruktion keine Option ist.“
Unter den im Rahmen der V005 Phase 2/3 Studie behandelten Patienten waren 54, bei denen eine gefäßchirurgische Reparatur der Extremitäten mit Symvess durchgeführt wurde, weil eine Behandlung mit einer autologen Vene, dem Behandlungsstandard, nicht möglich war. In dieser Patientengruppe blieben nach Abklingen der frühen Komplikationen durch die traumatischen Verletzungen die Raten von conduit-Infektionen, Gliedmaßenerhalt sowie das Überleben der Patienten während der dreijährigen Nachbeobachtung relativ konstant. Symvess hielt von Monat 3 bis 36 eine infektionsfreie Rate von 92,9 %, es traten nach Tag 37 keine Infektionen mehr auf und insgesamt wurden nur drei conduit-Infektionen festgestellt. Die Raten des Gliedmaßenerhalts lagen bei 87,3 % nach 12 Monaten und 82,5 % nach 24 Monaten, und das trotz einer schwer verletzten Traumakohorte.
Die langfristige mechanische Haltbarkeit wurde in der V005-Studie ebenfalls nachgewiesen. Mithilfe von Duplex-Ultraschall wurden die Durchgängigkeit und der mittlere Gefäßdurchmesser bei jeder Nachuntersuchung bis Monat 36 überprüft. Der durchschnittliche mittlere Transplantatdurchmesser wich über 36 Monate nicht wesentlich vom Ausgangswert von 6 mm ab. Darüber hinaus gab es keine Hinweise auf Tendenzen zu Dilatation oder Verengung des Symvess-Durchmessers bis zu 36 Monaten. Unerwünschte Ereignisse und schwerwiegende unerwünschte Ereignisse gingen im Zeitverlauf zurück, was die langfristige Haltbarkeit dieser Gefäßreparatur unterstützt. Entscheidend ist, dass keine Todesfälle, Amputationen oder mechanischen Ausfälle auf Symvess zurückgeführt wurden. Ebenso gab es während der gesamten Nachbeobachtungszeit keine Hinweise auf spontane Rupturen oder strukturelle Ausfälle bei irgendeinem Patienten.
Gefäßverletzungen stellen für Chirurgen eine besondere Herausforderung dar, und autologe Venen-Transplantate galten traditionell als Goldstandard aufgrund ihrer Haltbarkeit und niedrigen Infektionsraten. Allerdings sind autologe Transplantate bei Verletzungen, bei denen die Venen beschädigt sind oder wenig Zeit zur Entnahme bleibt, nicht immer praktikabel. Symvess (azelluläres, gewebetechnisch hergestelltes Gefäß (ATEV)) wurde entwickelt, um sofort einsatzbereit zu sein – was in Notfallsituationen wertvolle Operationszeit spart – und hat ebenfalls konstant niedrige Infektionsraten gezeigt.
INFORMATIONEN ZUR INDIKATION
Symvess ist ein azelluläres, gewebetechnisch hergestelltes Gefäß, das bei Erwachsenen als vaskulärer Ersatz für arterielle Extremitätenverletzungen indiziert ist, wenn eine dringende Revaskularisierung zur Vermeidung eines drohenden Gliedmaßenverlusts erforderlich ist und ein autologes Venentransplantat nicht möglich ist.
WICHTIGE SICHERHEITSINFORMATIONEN
GEKENNZEICHNETE WARNUNG: TRANSPLANTATAUSFALL
Der Verlust der Integrität von Symvess durch eine Ruptur im mittleren Transplantatbereich oder ein Anastomoseversagen kann zu lebensbedrohlichen Blutungen führen.
KONTRAINDIKATIONEN
Symvess darf NICHT bei Patienten angewendet werden, die eine Erkrankung haben, die eine langfristige Behandlung mit Thrombozytenaggregationshemmern (wie Aspirin oder Clopidogrel) nach Abklingen der akuten Verletzungen ausschließt.
WARNHINWEISE UND VORSICHTSMASSNAHMEN
- Transplantatruptur
Gefäßtransplantatrupturen sind bei mit Symvess behandelten Patienten vorgekommen. Patienten sollten darüber informiert werden, dass arterielle Blutungen lebensbedrohlich sein können, und bei Anzeichen oder Symptomen einer Transplantatruptur wie Blutungen, Schmerzen und Schwellungen an der Extremität oder Anzeichen einer Extremitätenischämie sofort medizinische Hilfe suchen.
- Anastomoseversagen
Anastomoseversagen sind bei mit Symvess behandelten Patienten aufgetreten. In klinischen Studien mit Symvess trat Anastomoseversagen innerhalb der ersten 36 Tage nach der Implantation auf. Patienten sollten auf Anzeichen eines Anastomoseversagens wie Schmerzen und Schwellungen an der Operationsstelle, fallenden Hämoglobinwerten oder andere Anzeichen und Symptome von Blutungen überwacht werden. Patienten sollten angewiesen werden, bei jeglichen Anzeichen oder Symptomen, die auf ein Anastomoseversagen hindeuten könnten, wie Blutungen, Schwellungen oder zunehmende Schmerzen an der Operationsstelle oder Veränderungen der Hautfarbe, unverzüglich medizinische Hilfe in Anspruch zu nehmen.
- Thrombose
Thrombosen sind bei mit Symvess behandelten Patienten aufgetreten. In klinischen Studien mit Symvess erhielten Patienten nach der Implantation eine antithrombozytäre Therapie, um das Thromboserisiko zu senken. Das Risiko einer Thrombose kann bei Patienten steigen, die die Therapie abbrechen. Eine antithrombozytäre Therapie wird nach einer Behandlung mit Symvess empfohlen.
- Übertragung von Infektionskrankheiten
Symvess wird unter Verwendung von Zellen und Reagenzien hergestellt, die Infektionskrankheiten oder infektiöse Erreger übertragen können. Die zur Herstellung von Symvess verwendeten Zellen stammen von einem Spender, der die Eignungskriterien für übertragbare Infektionskrankheiten erfüllte, einschließlich eines Screenings und Tests auf Risiken im Zusammenhang mit dem humanen Immundefizienzvirus 1 (HIV-1), humanen Immundefizienzvirus 2 (HIV-2), Hepatitis-B-Virus (HBV), Hepatitis-C-Virus (HCV) und Syphilis (Treponema pallidum). Die Zellbanken wurden negativ auf humane und tierische Viren, Retroviren, Bakterien, Pilze, Hefen und Mykoplasmen getestet. Während alle tierischen Reagenzien vor der Verwendung auf tierische Viren, Bakterien, Pilze und Mykoplasmen getestet werden, eliminieren diese Maßnahmen das Risiko der Übertragung dieser oder anderer infektiöser Krankheiten und Krankheitserreger nicht vollständig. Fetales Kälberserum wird so bezogen, dass das Risiko einer Übertragung eines Prionproteins, das die bovine spongiforme Enzephalopathie verursacht und der Auslöser einer seltenen tödlichen Erkrankung des Menschen namens Variante Creutzfeldt-Jakob-Krankheit ist, minimiert wird. Während der klinischen Erprobung wurden keine Infektionen mit übertragbaren Erregern berichtet.
NEBENWIRKUNGEN
Die häufigsten Nebenwirkungen (≥ 10 %) waren Thrombosen im Transplantat, Fieber (Pyrexie) und Schmerzen.
Über Humacyte
Humacyte, Inc. (Nasdaq: HUMA) entwickelt eine bahnbrechende Biotechnologie-Plattform zur Herstellung universell implantierbarer bioengineerter menschlicher Gewebe, fortschrittlicher Gewebekonstrukte und Organsysteme, die das Leben von Patienten verbessern und die medizinische Praxis revolutionieren sollen. Das Unternehmen entwickelt und produziert azelluläre Gewebe für die Behandlung eines breiten Spektrums von Erkrankungen, Verletzungen und chronischen Leiden. Der Biologics License Application von Humacyte für das azelluläre, gewebetechnisch hergestellte Gefäß (ATEV) bei der Indikation vaskuläres Trauma wurde im Dezember 2024 von der FDA genehmigt. ATEVs befinden sich zudem in fortgeschrittenen klinischen Studien für andere vaskuläre Anwendungen, darunter arteriovenöser (AV) Zugang für Hämodialyse und periphere arterielle Verschlusskrankheit (PAD). In der präklinischen Entwicklung befinden sich außerdem Koronararterien-Bypässe, pädiatrische Herzchirurgie, die Behandlung von Typ-1-Diabetes und mehrere neuartige Zell- und Gewebeanwendungen. Das 6mm-ATEV von Humacyte für AV-Zugang in der Hämodialyse war das erste Produkt, das mit der RMAT-Designation („Regenerative Medicine Advanced Therapy“) der FDA ausgezeichnet wurde, und erhielt auch die Fast Track-Designation der FDA. Die 6mm-ATEV von Humacyte für die dringende arterielle Reparatur nach Extremitäten-Gefäßtrauma und für fortgeschrittene PAD haben ebenfalls RMAT-Designation erhalten. Das ATEV erhielt die Prioritätsbezeichnung für die Behandlung von Gefäßtrauma vom US-Verteidigungsminister.
Für andere Anwendungen als die von der FDA zugelassene Indikation „vaskuläres Trauma der Extremitäten“ ist das ATEV ein Prüfpräparat und wurde weder von der FDA noch von einer anderen Aufsichtsbehörde zum Verkauf zugelassen.
Haftungsausschluss: Der Inhalt dieses Artikels gibt ausschließlich die Meinung des Autors wieder und repräsentiert nicht die Plattform in irgendeiner Form. Dieser Artikel ist nicht dazu gedacht, als Referenz für Investitionsentscheidungen zu dienen.
Das könnte Ihnen auch gefallen
NFLX am 5. März: Aufwärtspotenzial nach geplatztem Deal oder Falle?
Ein Vorstandsmitglied einer Gemeinschaftsbank tritt zurück und äußert scharfe Kritik.
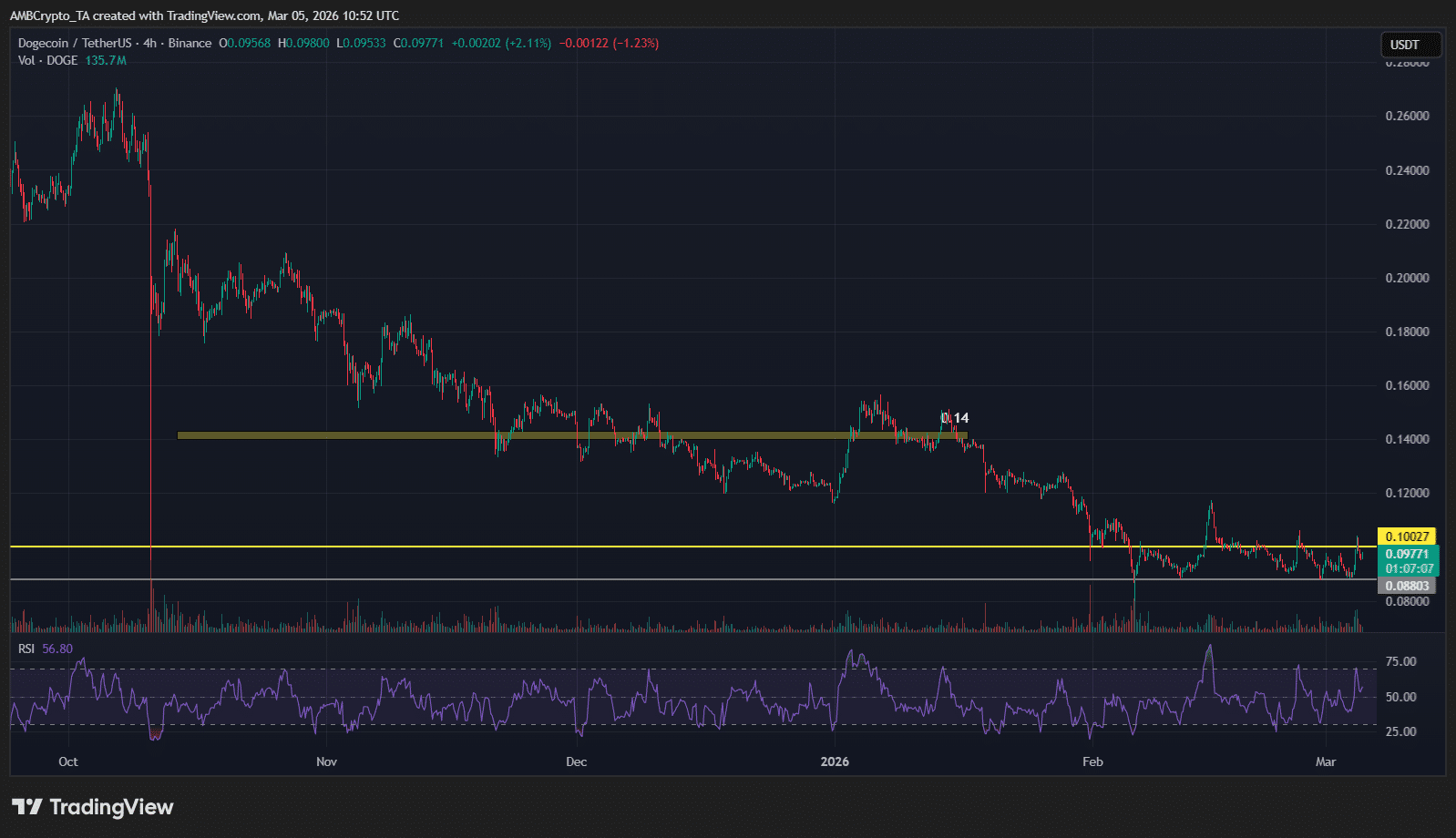
Dogecoin-Volumen steigt um 60 % – aber DOGE kann $0,10 NUR zurückerobern, wenn…