Moleculin MIRACLE-Studie liefert vorläufige verblindete CRc-Rate von 40 % (n=30)
Zusätzlich berichtet das Unternehmen über eine vorläufige zusammengesetzte vollständige Remissionsrate (CRc) von 40% bei den ersten 30 behandelten Probanden der MIRACLE-Studie und mit verblindeten, vorläufigen Wirksamkeitsdaten. Diese CRc-Rate setzt sich zusammen aus einer vollständigen Remissionsrate (CR) von 30% sowie einer vollständigen Remission mit partieller hämatologischer Erholung (CRh) von 10%.
„Die verblindeten Wirksamkeitsraten, die wir in MIRACLE sehen, sind außergewöhnlich ermutigend“, sagte Walter Klemp, Vorstandsvorsitzender und CEO von Moleculin. „Und natürlich beinhaltet dies auch den Kontrollarm aus Cytarabin plus Placebo, was darauf hindeutet, dass die Ergebnisse mit Annamycin besser sein sollten. Selbst mit dem Kontrollarm übertreffen diese vorläufigen verblindeten Ergebnisse die historischen Ergebnisse für CR mit Cytarabin allein deutlich und unterstreichen unsere Erwartungen, was Annamycin in der Behandlung von R/R AML werden kann. Besonders bemerkenswert ist, dass etwa 35% der bisher behandelten Probanden Rückfälle oder refraktär (R/R) nach einem Venetoclax-Regime sind – eine Patientengruppe, die allgemein als besonders schwer zu behandeln gilt mit 2
Dr. Mohamad Cherry, ein führender Meinungsbildner in der hämatologischen Onkologie, bemerkte: „Solche verblindeten Wirksamkeitsraten im MIRACLE-Trial zu sehen, ist ermutigend für die Robustheit der gesamten Studie und lässt auf eine vielversprechende klinische Zukunft für Annamycin als nicht-kardiotoxisches Anthrazyklin hoffen. Dies könnte einen bedeutenden Fortschritt im Behandlungsumfeld für rezidivierende/refraktäre AML darstellen.“
„Ein weiteres ermutigendes Zeichen ist, dass die bisher behandelten Probanden eine hohe Anzahl genetischer Marker aufwiesen, die als prädiktiv für eine schlechte Behandlungsantwort gelten, was diese Ergebnisse noch beeindruckender macht. Die Wirksamkeitsraten, die bislang in sechs Ländern im MIRACLE-Trial beobachtet wurden, bilden die Grundlage für unseren Optimismus hinsichtlich unserer Aussichten für 2026“, fuhr Herr Klemp fort. „Unsere aktuelle verblindete CR-Rate liegt 67% über den historischen Ansprechraten aus zwei aktuellen HiDAC-Studien mit Cytarabin allein, die etwa 17-18% CR zeigten, und auch 50% über der mittleren CR-Rate, die für die Zulassung aller derzeit verschriebenen Therapien für AML-Patienten in der Zweitlinie verwendet wurde. Zudem gehen wir davon aus, dass etwa ein Drittel der bisher behandelten Probanden kein Annamycin erhalten hat. Wir glauben daher, dass Annamycin vermutlich auf dem beeindruckenden Niveau unseres letzten Phase-2-Trials liegt oder diesem nahekommt. In Kombination mit den jüngst veröffentlichten Sicherheitsdaten aus insgesamt 90 Probanden aus früheren klinischen Studien, die das Fehlen einer Kardiotoxizität von Annamycin zeigen, glauben wir, dass Annamycin Patienten mit dieser herausfordernden Erkrankung eine neue Behandlungsmöglichkeit bieten kann. Wir freuen uns auf den bevorstehenden wichtigen Meilenstein für das Unternehmen und den MIRACLE-Trial: die Entblindung der Wirksamkeit jeder Studiengruppe bei den ersten 45 Probanden.“
Herr Klemp schloss: „Angesichts der Bedeutung dieser Studie und ihres Potenzials, zukünftige Partnerschaften und Wertsteigerungen zu fördern, wissen wir, wie wichtig der Zeitpunkt der Daten-Entblindung ist. Wir verpflichten uns zu häufigen Markt-Updates, um Investoren zu informieren, sobald die Sichtbarkeit in Bezug auf einen genaueren Entblindungszeitpunkt zunimmt.“
Die MIRACLE-Studie (abgeleitet von Moleculin R/R AML AnnAraC Clinical Evaluation) ist eine globale, multizentrische, randomisierte, doppelblinde, placebokontrollierte Phase-2B/3-Studie mit adaptivem Design, bei der die Daten aus dem 2B-Teil (Teil A) mit dem Phase-3-Teil (Teil B) zur Messung des primären Wirksamkeitsendpunkts kombiniert werden. Teil A des MIRACLE-Trials ist darauf ausgelegt, die Wirksamkeit von Annamycin in zwei Dosierungsarmen (190 mg/m
Der MIRACLE-Trial richtet sich ausschließlich an AML-Patienten, die eine einzige vorherige Induktionstherapie erhalten haben (2
Die derzeit eingeschlossenen Probanden, einschließlich derjenigen, die bereits behandelt, aber noch nicht auf Wirksamkeit beurteilt wurden, stammen von Standorten in sieben Ländern und bieten so eine vielfältige Probandenbasis. 24 Standorte haben bereits Site Initiation Visits erhalten, das Unternehmen strebt mindestens 30 Standorte für Teil B an. Der Fokus liegt auf der verbesserten Rekrutierung in den USA, da die Rekrutierung in Europa bislang robust war.
Das Unternehmen erwartet, im ersten Quartal 2026 die Rekrutierung und Behandlung der ersten 45 Probanden abzuschließen. Die Entblindung der ersten 45 Probanden mit Wirksamkeitsdaten sollte gegen Ende des zweiten Quartals 2026 erfolgen, da die Daten zunächst endgültig eingetragen, geprüft und anschließend gesperrt werden müssen. Daher können diese vorläufigen Daten von den endgültigen, gesperrten Wirksamkeits- und Sicherheitsdaten abweichen. Die zweite Gruppe von 45 Probanden in Teil A soll im dritten Quartal 2026 vollständig rekrutiert sein, mit Entblindung in der zweiten Jahreshälfte 2026. Die Rekrutierung der zweiten Gruppe von 45 Probanden in Teil A wird fortgesetzt, während die Wirksamkeitsdaten der ersten 45 Probanden entblindet werden. Die Entblindung aller 90 Probanden in Teil A kann mehr Zeit in Anspruch nehmen als die der ersten 45, da mehr Daten für den Übergang von Teil A zu Teil B benötigt werden.
Annamycin, auch bekannt unter dem nicht-proprietären Namen Naxtarubicin, hat derzeit den Fast-Track-Status und die Orphan-Drug-Designation der FDA für die Behandlung von rezidivierter oder refraktärer akuter myeloischer Leukämie, zusätzlich zur Orphan-Drug-Designation für die Behandlung von Weichteilsarkomen. Annamycin profitiert zudem von einem Patentschutz bis 2040 mit der Möglichkeit, diesen Schutz bis 2045 zu verlängern. Darüber hinaus hat Annamycin auch von der EMA die Orphan-Drug-Designation für die Behandlung von rezidivierter oder refraktärer akuter myeloischer Leukämie erhalten.
Moleculin Biotech, Inc. ist ein pharmazeutisches Unternehmen im klinischen Stadium der Phase 3, das eine Pipeline therapeutischer Kandidaten für schwer zu behandelnde Tumore und Viren entwickelt. Das Leitprogramm des Unternehmens, Annamycin, ist ein hochwirksames und gut verträgliches Anthrazyklin der nächsten Generation, das darauf ausgelegt ist, Mechanismen der Multidrug-Resistenz zu umgehen und keine der bei aktuell verschriebenen Anthrazyklinen üblichen Kardiotoxizitäten aufzuweisen. Annamycin befindet sich derzeit in der Entwicklung zur Behandlung von rezidivierter oder refraktärer akuter myeloischer Leukämie (AML) sowie Lungenmetastasen von Weichteilsarkomen (STS).
Das Unternehmen hat die MIRACLE (
Darüber hinaus entwickelt das Unternehmen WP1066, einen Immun-/Transkriptionsmodulator, der p-STAT3 und andere onkogene Transkriptionsfaktoren hemmen und gleichzeitig eine natürliche Immunantwort stimulieren kann, mit dem Ziel, Hirntumore, Pankreaskarzinome und andere Krebsarten zu behandeln. Moleculin hat außerdem eine Pipeline von Antimetaboliten, darunter WP1122 zur potenziellen Behandlung pathogener Viren sowie bestimmter Krebsindikationen.
Haftungsausschluss: Der Inhalt dieses Artikels gibt ausschließlich die Meinung des Autors wieder und repräsentiert nicht die Plattform in irgendeiner Form. Dieser Artikel ist nicht dazu gedacht, als Referenz für Investitionsentscheidungen zu dienen.
Das könnte Ihnen auch gefallen
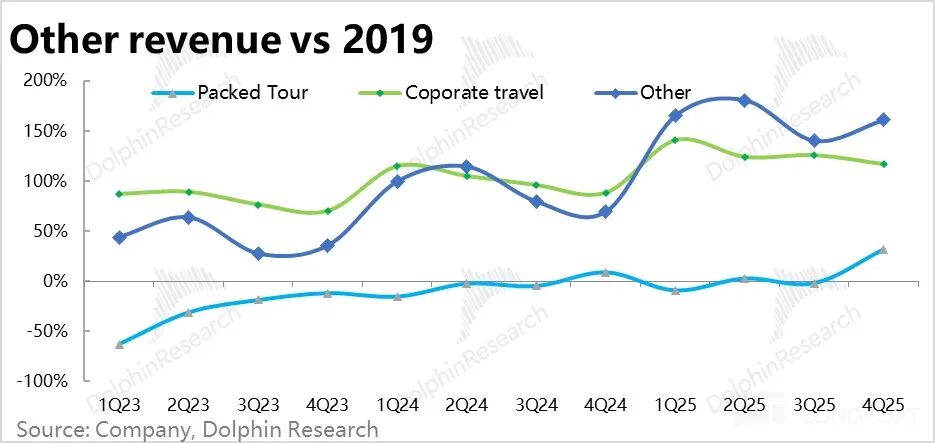
Trip.com: Kann es nach dem „harten Regulierungsschlag“ noch „klein, aber fein“ sein?

Die Haushaltsverschuldung überwältigt die Menschen in den USA. So können Sie darauf reagieren

