Edesa Biotech berichtet über weitere positive Ergebnisse aus der Phase-3-Studie zu Paridiprubart
- Ergebnisse in einer Population von 278 Patienten bestätigen statistisch signifikante Reduktionen der Sterblichkeit
- Vorteile wurden über alle Schweregrade hinweg und bei Patienten mit schweren Begleiterkrankungen beobachtet
- Das Unternehmen hat vorläufige Patentanmeldungen für Sepsis, akutes Nierenversagen und Pneumonie eingereicht
- Strategische Kooperationen zur Unterstützung der späten Entwicklungsphase und Kommerzialisierung werden geprüft
- Studienergebnisse für mündlichen Vortrag auf der ATS 2026-Konferenz ausgewählt
TORONTO, 24. Februar 2026 (GLOBE NEWSWIRE) -- Edesa Biotech, Inc. (Nasdaq:EDSA), ein biopharmazeutisches Unternehmen in der klinischen Phase mit Fokus auf die Entwicklung von hostgerichteten Therapeutika für immun-inflammatorische Erkrankungen, gab heute positive zusätzliche Daten aus einer Phase-3-Studie mit paridiprubart bekannt.
Die Ergebnisse betreffen eine größere Population von 278 Patienten, darunter sowohl die zuvor berichteten 104 Patienten, die eine invasive mechanische Beatmung (IMV) benötigten, als auch 174 Patienten ohne IMV. In dieser Gesamtpopulation zeigte der neuartige Anti-TLR4-Antikörper des Unternehmens eine statistisch signifikante Reduktion der 28-Tage-Sterblichkeit. Die Behandlungsvorteile waren über alle Schweregrade und bei Patienten mit schweren Begleiterkrankungen konsistent.
Zentrale Ergebnisse
Der primäre Endpunkt wurde für die gesamte behandelte Population von 278 randomisierten Probanden erreicht. Paridiprubart senkte die adjustierte 28-Tage-Sterblichkeit von 33% auf 24%, was einer relativen Risikoreduktion des Todes von 27% entspricht (p<0,001). Darüber hinaus zeigten Probanden, die Paridiprubart erhielten, eine höhere relative Rate klinischer Verbesserung bis Tag 28. Paridiprubart oder Placebo wurden zusätzlich zu den Standardbehandlungen (SOC) verabreicht.
In einer explorativen Analyse einer milderen Population von 174 randomisierten Patienten, die die IMV-basierten Einschlusskriterien der Studie nicht erfüllten, reduzierte Paridiprubart + SOC die adjustierte 28-Tage-Sterblichkeit von 23% (Placebo + SOC) auf 15%, was einer relativen Risikoreduktion des Todes von 35% entspricht (p<0,05).
Edesa berichtete außerdem, dass explorative Analysen in einer Patientengruppe von bis zu 108 randomisierten Probanden durchgängig eine reduzierte adjustierte Sterblichkeit für Paridiprubart + SOC im Vergleich zu Placebo + SOC nach 28 Tagen bei Probanden mit klinisch relevanten Begleiterkrankungen zeigten:
- Akutes Nierenversagen: 35% relative Reduktion (35% Paridiprubart vs. 53% Placebo; p<0,05, n=48)
- Sepsis: 36% relative Reduktion (40% Paridiprubart vs. 63% Placebo; p<0,05, n=41)
- Pneumonie: 30% relative Reduktion (35% Paridiprubart vs. 49% Placebo; p<0,05, n=108)
Die Gesamtraten an Nebenwirkungen, schwerwiegenden Nebenwirkungen, Infektionen und Therapieabbrüchen waren gering und zwischen der Paridiprubart- und der Placebo-Gruppe ähnlich. Das Sicherheitsprofil entsprach früheren klinischen Erfahrungen, wobei inzwischen mehr als 400 Patienten Paridiprubart erhalten haben.
Basierend auf diesen positiven Ergebnissen hat Edesa vorläufige Patentanmeldungen beim US-Patent- und Markenamt für die Verwendung von Paridiprubart bei der Behandlung von Sepsis, akutem Nierenversagen und Pneumonie eingereicht. Die grundlegenden Stoffschutzpatente des Unternehmens reichen bis in die 2030er Jahre.
Par Nijhawan, MD, Chief Executive Officer von Edesa Biotech, erklärte, dass die heute bekannt gegebenen Ergebnisse mit der zentralen Rolle von TLR4 beim hyperinflammatorischen ARDS (Akutes Lungenversagen) übereinstimmen und einen konsistenten Nutzen bei Ursachen mit hoher Sterblichkeit aufzeigen.
„Die Konsistenz der Sterblichkeitsreduktion und der klinischen Verbesserung bei allen 278 randomisierten Patienten, einschließlich weniger schwerer Patienten sowie solcher mit ARDS, das durch akutes Nierenversagen, Sepsis und Pneumonie kompliziert ist, unterstreicht die Vielseitigkeit und das transformative Potenzial von Paridiprubart, um mehrere kritische ungedeckte medizinische Bedürfnisse zu adressieren“, sagte Dr. Nijhawan. „Wir führen regulatorische Gespräche und prüfen strategische Kooperationen sowie Partnerschaftsmöglichkeiten, die die Entwicklung beschleunigen und den globalen Zugang erweitern könnten.“ Er merkte an, dass die Planung zum Ausbau der Produktion bereits läuft.
Paridiprubart wird derzeit in einer separaten, von der US-Regierung finanzierten Studie an ARDS-Patienten evaluiert. Die Rekrutierung läuft für bis zu etwa 200 randomisierte Probanden für die Edesa-Kohorte. Das Entwicklungsprogramm für Paridiprubart, einschließlich Produktionserweiterung, späte Entwicklungsphase und Marktreife, erhält ebenfalls Unterstützung von der Regierung Kanadas.
Edesa wurde für eine mündliche Präsentation auf der American Thoracic Society (ATS) 2026 International Conference (15.-20. Mai 2026) ausgewählt und plant, weitere Ergebnisse aus der Phase-3-Studie auf weiteren medizinischen und wissenschaftlichen Konferenzen zu präsentieren.
Detaillierte Ergebnisse
Die Daten stammen aus der gesamten Sicherheitsstudienpopulation von 278 Patienten; die zuvor berichtete 104-Personen-IMV-ITT-Kohorte stellt eine vordefinierte Teilmenge dieser Population dar. Patienten in der gesamten 278-Personen-Sicherheitsgruppe wurden zufällig (1:1) zu SOC mit Paridiprubart (n=138) oder SOC mit Placebo (n=140) zugeteilt. Die Ausgangsmerkmale und SOC waren zwischen den Behandlungsgruppen ausgewogen.
Die folgenden Tabellen fassen die wichtigsten zusätzlichen Ergebnisse zusammen:
Primärer Endpunkt: Sterblichkeitsrate nach 28 Tagen
Multivariate logistische Regression, berechnete Risikounterschiede, 95%CI
| Population | Paridiprubart | Placebo | P-Wert |
| Alle (n=278) | 0,24 (0,21, 0,27) | 0,33 (0,29, 0,37) | <0,001 |
| IMV ITT (n=104) | 0,39 (0,35, 0,44) | 0,52 (0,47, 0,58) | <0,001 |
Adjustierte Modell-basierte Mortalitätsschätzungen: Variablen umfassen Alter, Ausgangswert der WHO Covid-19 Severity Scale (WCSS), Ausgangswert antiviraler Einsatz, Ausgangswert Kortikosteroid-Einsatz, Ausgangswert Immunmodulator-Einsatz, gleichzeitiger antiviraler Einsatz, gleichzeitiger Kortikosteroid-Einsatz, gleichzeitiger Immunmodulator-Einsatz. Gesamte Sicherheitsgruppe n=278; Intent-to-treat (ITT) IMV Population n=104
Sekundärer Endpunkt: Erreichen einer Verbesserung von ≥2 Punkten im WCSS nach 28 Tagen
Multivariate logistische Regression, berechnete Risikounterschiede, 95%CI
| Population | Paridiprubart | Placebo | P-Wert |
| Alle (n=278) | 0,52 (0,48, 0,56) | 0,45 (0,41-0,48) | <0,01 |
| IMV ITT (n=104) | 0,38 (0,31, 0,45) | 0,27 (0,21, 0,33) | <0,05 |
Adjustierte Risikoschätzung: Variablen umfassen Alter, Ausgangswert WCSS, Ausgangswert antiviraler Einsatz, Ausgangswert Kortikosteroid-Einsatz, Ausgangswert Immunmodulator-Einsatz, gleichzeitiger antiviraler Einsatz, gleichzeitiger Kortikosteroid-Einsatz, gleichzeitiger Immunmodulator-Einsatz. Sicherheitsgruppe n=278; ITT IMV Population n=104
Explorative Analyse: Sterblichkeitsrate nach 28 Tagen
Multivariate logistische Regression, berechnete Risikounterschiede, 95%CI
| Population | Paridiprubart | Placebo | P-Wert* |
| Nicht-IMV (n=174) | 0,15 (0,12, 0,18) | 0,23 (0,19, 0,26) | <0,05 |
| Pneumonie (n=108) | 0,35 (0,29, 0,41) | 0,49 (0,43, 0,55) | <0,05 |
| Akutes Nierenversagen (n=48) | 0,35 (0,25, 0,44) | 0,53 (0,44, 0,62) | <0,05 |
| Sepsis (n=41) | 0,40 (0,37, 0,43) | 0,63 (0,59, 0,66) | <0,05 |
*Nominaler p-Wert, nicht für Multiplikität adjustiert
Methodik und Hintergrund
In Übereinstimmung mit der ursprünglichen Analyse wurden alle vordefinierten Wirksamkeitsbewertungen gemäß demselben statistischen Analyseplan (SAP) unter Verwendung eines identischen multivariaten logistischen Regressionsmodells und denselben Kovariaten durchgeführt. Der SAP definierte eine hierarchische Teststruktur für die adjustierte 28-Tage-Sterblichkeit sowohl für die gesamte 278-Personen-Population als auch für die 104-Personen-IMV-ITT-Population. Beide Analysen waren vordefiniert und vor Entblindung gesichert. Explorative Analysen wurden anschließend für die 174 nicht-IMV-randomisierten Probanden unter Verwendung desselben Modells und derselben Kovariaten durchgeführt. Weitere explorative Analysen wurden für Probanden mit akutem Nierenversagen, Sepsis oder Pneumonie durchgeführt, wobei dasselbe Modell, aber subgroupenspezifische Kovariaten zur Berücksichtigung klinischer Unterschiede verwendet wurden.
Die Studie wurde von JSS Medical Research, einer internationalen Auftragsforschungsorganisation, geleitet und ausgewertet.
Über Paridiprubart
Paridiprubart repräsentiert eine neue Klasse von hostgerichteten Therapeutika (HDTs), die darauf ausgelegt sind, die körpereigene Immunantwort bei bekannten oder unbekannten Gesundheitsbedrohungen wie neuartigen Infektionskrankheiten sowie chemischen, biologischen, radiologischen und nuklearen Vorfällen zu modulieren. HDTs sind dabei unabhängig vom Auslöser und können vorsorglich eingelagert werden, um auf Notfälle im Bereich der öffentlichen Gesundheit und die Biodefense zu reagieren. Mechanistisch hemmt Paridiprubart den Toll-like-Rezeptor 4 (TLR4), ein zentrales Protein der Immunantwort, das nachweislich durch Viren, Bakterien, Verletzungen/Trauma und bei der Pathogenese chronischer Autoimmunerkrankungen aktiviert wird.
Über ARDS
Das akute Atemnotsyndrom (ARDS) ist durch eine überschießende Immunantwort gekennzeichnet, die zu Entzündungen und Schäden an der Lunge führt, wodurch die Lunge nicht mehr in der Lage ist, das Blut mit Sauerstoff zu versorgen, was letztlich zu Sauerstoffmangel im Körper führt. Für moderate bis schwere Fälle gibt es derzeit nur wenige empfohlene Behandlungen außer zusätzlichem Sauerstoff und mechanischer Beatmung, und die Sterblichkeitsrate ist hoch. Neben virusinduzierter Pneumonie kann ARDS durch Rauch-/Chemikalieninhalation, Sepsis, Thoraxverletzungen und andere Ursachen ausgelöst werden. ARDS verursacht 10% aller Intensivstationsaufenthalte und betrifft weltweit mehr als 3 Millionen Patienten pro Jahr.
Über Edesa Biotech
Edesa Biotech, Inc. (Nasdaq: EDSA) ist ein biopharmazeutisches Unternehmen in der klinischen Phase, das innovative Wege zur Behandlung von entzündlichen und immunbezogenen Erkrankungen entwickelt. Die klinische Pipeline konzentriert sich auf zwei therapeutische Bereiche: medizinische Dermatologie und Atemwege. In der medizinischen Dermatologie entwickelt Edesa EB06, einen anti-CXCL10 monoklonalen Antikörper-Kandidaten, als Therapie für Vitiligo, eine häufige Autoimmunerkrankung, die dazu führt, dass die Haut ihre Farbe in Flecken verliert. Die medizinischen Dermatologieprodukte umfassen außerdem EB01 (1,0% Daniluromer-Creme), eine für die Phase 3 bereitstehende Substanz, die als potenzielle Therapie für mittelgradige bis schwere chronische allergische Kontaktdermatitis (ACD), eine häufige berufliche Hauterkrankung, entwickelt wurde. Der am weitesten fortgeschrittene Atemwegsarzneimittelkandidat des Unternehmens ist EB05 (Paridiprubart), der in einer von der US-Regierung finanzierten Plattformstudie als Behandlung für das akute Atemnotsyndrom, eine lebensbedrohliche Form des Atemversagens, untersucht wird. Das EB05-Programm wurde von der kanadischen Regierung zur weiteren Entwicklung dieses Wirkstoffs mit zwei Förderpreisen ausgezeichnet. Edesa prüft zudem weitere Einsatzmöglichkeiten für Paridiprubart. Melden Sie sich für Nachrichten an. Vernetzen Sie sich mit uns auf X und LinkedIn.
Kontakt:
Gary Koppenjan
Edesa Biotech, Inc.
Haftungsausschluss: Der Inhalt dieses Artikels gibt ausschließlich die Meinung des Autors wieder und repräsentiert nicht die Plattform in irgendeiner Form. Dieser Artikel ist nicht dazu gedacht, als Referenz für Investitionsentscheidungen zu dienen.
Das könnte Ihnen auch gefallen
Das Pfund Sterling schwächt sich auf nahe 1,3300 ab, da geopolitische Risiken den US-Dollar stärken
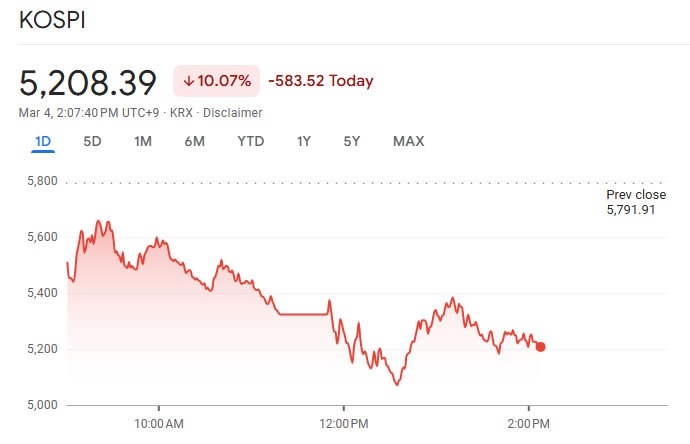
Korea setzt den Handel aus, nachdem wichtige Indizes aufgrund der Nahostkrise um 10 % gefallen sind
Agentic Inference Cloud von DigitalOcean: Schaffung der Infrastruktur für den produktiven Einsatz von KI