DNLI Q4 meldet geringeren als erwarteten Verlust, Fokus auf Behandlung des Hunter-Syndroms
Denali Therapeutics Finanzieller Überblick Q4 2025
Denali Therapeutics (DNLI) verzeichnete im vierten Quartal 2025 einen Nettoverlust von 0,73 $ pro Aktie, was geringfügig besser war als die Konsensschätzung eines Verlusts von 0,75 $. Im Vergleich dazu betrug der Verlust im gleichen Zeitraum des Vorjahres 0,67 $ pro Aktie.
Der Anstieg des Verlusts je Aktie im Jahresvergleich ist in erster Linie auf höhere Betriebsausgaben zurückzuführen.
Da Denali keine Produkte auf dem Markt hat, beschränken sich die Einnahmen auf Erlöse aus laufenden Partnerschaften. Im Berichtsquartal erzielte das Unternehmen keine Einnahmen aus Kooperationen und verfehlte damit die erwarteten 18 Millionen $.
Im vergangenen Jahr stiegen die DNLI-Aktien um 13,4 % und übertrafen damit den Sektor Medizin, Biomedizin und Genetik, der einen Zuwachs von 11,5 % verzeichnete.
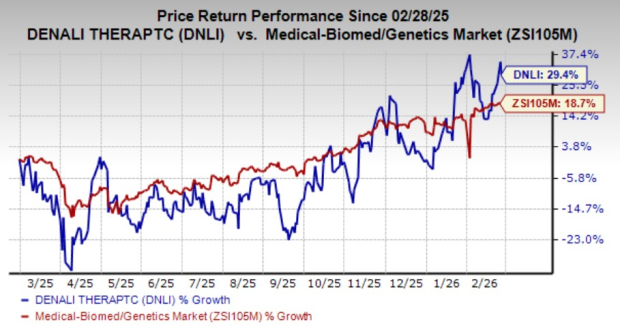
Quelle: Zacks Investment Research
Wichtige Punkte aus den Q4-Ergebnissen
- Die Forschungs- und Entwicklungskosten sanken um 1,9 % auf 97,9 Millionen $, hauptsächlich aufgrund geringerer Ausgaben für Small-Molecule-Projekte.
- Die allgemeinen Verwaltungsaufwendungen stiegen um 31,3 % auf 39,5 Millionen $, was die Vorbereitungen auf die erwartete Markteinführung von tividenofusp alfa widerspiegelt.
- Zum 31. Dezember 2025 verfügte Denali über etwa 966,2 Millionen $ an Barmitteln, Barmitteläquivalenten und marktfähigen Wertpapieren.
Zusammenfassung des Gesamtjahres 2025
- Im Jahr 2025 wurden keine Umsätze erzielt.
- Der Jahresverlust pro Aktie weitete sich auf 2,97 $ aus, verglichen mit 2,57 $ im Jahr 2024.
Fortschritt des führenden Arzneimittelkandidaten
Denali bereitet aktiv die kommerzielle Einführung seines wichtigsten Assets, tividenofusp alfa, vor.
Der Biologics License Application (BLA) für tividenofusp alfa, der zur Behandlung der Mukopolysaccharidose Typ II (Hunter-Syndrom) eingesetzt werden soll, wird derzeit von US-Regulierungsbehörden geprüft.
Die FDA hat die Frist für die Überprüfung vom 5. Januar 2026 auf den 5. April 2026 verlängert.
Tividenofusp alfa hat von der FDA mehrere Designationen erhalten, darunter Breakthrough Therapy, Fast Track, Orphan Drug und Rare Pediatric Disease Status.
Diese experimentelle Therapie ist darauf ausgelegt, das Enzym Iduronat-2-Sulfatase (IDS) über die Blut-Hirn-Schranke zu transportieren und so sowohl den Körper als auch das Gehirn zu erreichen.
Die BLA-Prüfungsfrist wurde verlängert, nachdem Denali aktualisierte klinisch-pharmakologische Daten als Antwort auf eine FDA-Anfrage bereitgestellt hatte. Das Unternehmen stellte klar, dass dieses Update nicht mit Wirksamkeit, Sicherheit oder Biomarkern zusammenhängt.
Die FDA stufte die Einreichung als wesentliche Änderung ein, was zu einer Verlängerung des Prüftermins führte.
Die laufende globale Phase II/III COMPASS-Studie soll unterstützende Nachweise für Zulassungsanträge weltweit liefern; die Rekrutierung der neuronopathischen Teilnehmer (Kohorte A) wurde im Dezember 2025 abgeschlossen.
Entwicklungen in der Pipeline
- Denali untersucht DNL126 zur Behandlung des Sanfilippo-Syndroms Typ A (MPS IIIA). Vorläufige Phase-I/II-Ergebnisse, die auf dem WORLDSymposium präsentiert wurden, zeigten signifikante Reduktionen wichtiger Krankheitsbiomarker und ein Sicherheitsprofil, das bestehenden Enzymersatztherapien ähnelt. Diese Ergebnisse könnten einen beschleunigten Zulassungspfad unterstützen, und eine bestätigende Phase-III-Studie ist geplant.
- Weitere Pipeline-Kandidaten werden in Zusammenarbeit mit Takeda (TAK), Biogen (BIIB) und Sanofi (SNY) entwickelt.
- Denali und Takeda treiben DNL593 als potenzielle Behandlung der mit Granulin-Mutation assoziierten Frontotemporalen Demenz (FTD-GRN) voran. Die Rekrutierung für die Phase-I/II-Studie ist mit 40 Teilnehmern abgeschlossen. Erste Patientendaten werden 2026 erwartet.
- Denali hat kürzlich die Genehmigung für eine Phase-Ib-Studie mit DNL628 erhalten, die Vorbereitungen laufen.
- Denali und Biogen entwickeln gemeinsam BIIB122. Biogen leitet die globale Phase-IIb-LUMA-Studie für die frühe Parkinson-Krankheit, deren Ergebnisse Mitte 2026 erwartet werden. Denali führt die Phase-IIa-BEACON-Studie zur Bewertung der LRRK2-Hemmung bei LRRK2-assoziierter Parkinson-Krankheit durch.
- Im Oktober reichte Denali einen IND-Antrag für DNL952 (ETV:GAA) ein, um klinische Studien bei der Pompe-Krankheit zu beginnen. Die FDA hat die klinische Sperre inzwischen aufgehoben, und die Vorbereitungen für die Phase-I-Studie laufen.
- Sanofi entwickelt eclitasertib für mittelschwere bis schwere Colitis ulcerosa, mit Phase-II-Daten, die in der ersten Jahreshälfte erwartet werden.
Analyse der Aussichten von Denali
Die Zulassung von tividenofusp alfa könnte Denalis Wachstumskurs erheblich stärken. Auch der Fortschritt von DNL126 ist vielversprechend.
Die soliden Barmittelreserven des Unternehmens unterstreichen die Fähigkeit, laufende Forschungs- und Entwicklungsinitiativen zu unterstützen.
Haftungsausschluss: Der Inhalt dieses Artikels gibt ausschließlich die Meinung des Autors wieder und repräsentiert nicht die Plattform in irgendeiner Form. Dieser Artikel ist nicht dazu gedacht, als Referenz für Investitionsentscheidungen zu dienen.
Das könnte Ihnen auch gefallen
Die Renditen von US-Staatsanleihen steigen, da die Ölpreise klettern und die Sorgen über die Inflation zunehmen
Der Token von Hyperliquid steigt, da der Schock am Wochenende im Iran auf wenige offene Märkte trifft
