Capricor Therapeutics annonce une présentation de dernière minute lors de la conférence clinique et scientifique MDA 2026
- Présentation de dernière minute à la MDA mettant en avant les résultats de l’étude HOPE-3 de Phase 3 soutenant Deramiocel dans la dystrophie musculaire de Duchenne
- Le rapport d’étude clinique (CSR) HOPE-3 soumis à la Food and Drug Administration (FDA) des États-Unis en appui à l’examen en cours du dossier BLA
SAN DIEGO, 24 février 2026 (GLOBE NEWSWIRE) -- Capricor Therapeutics (NASDAQ : CAPR), une société de biotechnologie développant des thérapies innovantes à base de cellules et d’exosomes pour le traitement de maladies rares, a annoncé aujourd’hui que les résultats de son étude clinique de Phase 3 HOPE-3 de Deramiocel pour la dystrophie musculaire de Duchenne (DMD) ont été sélectionnés pour une présentation orale de dernière minute lors de la Conférence Clinique et Scientifique de la Muscular Dystrophy Association (MDA) 2026, qui se tiendra du 8 au 11 mars 2026 à Orlando, Floride.
« La sélection de HOPE-3 comme présentation de dernière minute à la conférence MDA témoigne de la solidité et de l’accroissement des preuves cliniques soutenant Deramiocel et son potentiel impact pour les patients atteints de Duchenne », a déclaré Linda Marbán, Ph.D., directrice générale de Capricor. « Nous sommes impatients de partager ces résultats de Phase 3 avec la communauté DMD tout en poursuivant nos efforts réglementaires, incluant la soumission récente du rapport d’étude clinique HOPE-3 à la FDA dans le cadre de notre processus d’examen BLA en cours. Nous restons concentrés sur l’obtention potentielle d’une décision d’approbation et sur la mise à disposition de cette thérapie auprès des patients aussi efficacement que possible. »
Détails de la présentation MDA
| Date et heure : | 11 mars 2026, 14h45 ET |
| Titre de la présentation : | Confirmation du bénéfice musculosquelettique et cardiaque dans la DMD par Deramiocel, une thérapie cellulaire allogénique, dans l’étude HOPE-3 de Phase 3 |
| Présentateur : | Craig McDonald, M.D. (Professeur de Médecine Physique & Réadaptation et Pédiatrie à UC Davis Health et Investigateur Principal National de l’essai HOPE-3) |
| Lieu : | Florida 4 |
La soumission du CSR a été demandée par la FDA à la suite d’échanges réglementaires antérieurs et vise à traiter les points mentionnés dans la lettre de réponse complète (CRL) et à soutenir l’examen en cours de la demande de licence de produits biologiques (BLA) de la société pour Deramiocel dans la dystrophie musculaire de Duchenne, y compris la possibilité que la FDA attribue une nouvelle date cible d’action dans le cadre du Prescription Drug User Fee Act (PDUFA).
À propos de la dystrophie musculaire de Duchenne
La dystrophie musculaire de Duchenne (DMD) est une maladie génétique sévère liée à l’X, caractérisée par une dégénérescence musculaire progressive affectant les muscles squelettiques, respiratoires et cardiaques. Elle est causée par l’absence de dystrophine fonctionnelle, une protéine structurale clé des cellules musculaires. La DMD touche environ 15 000 personnes aux États-Unis et affecte principalement les garçons. Au fil du temps, la dégradation du muscle cardiaque conduit à une cardiomyopathie et à une insuffisance cardiaque, principale cause de décès dans la DMD. Il n’existe pas de remède et les options thérapeutiques demeurent limitées.
À propos de Deramiocel
Deramiocel (CAP-1002) est composé de cellules dérivées de cardiosphères allogéniques (CDCs), une population rare de cellules cardiaques qui ont montré, lors d’études précliniques et cliniques, des actions immunomodulatrices et anti-fibrotiques puissantes pour préserver la fonction musculaire cardiaque et squelettique dans les dystrophies musculaires telles que la DMD. Les CDCs agissent en sécrétant des vésicules extracellulaires appelées exosomes, qui ciblent les macrophages et modifient leur profil d’expression vers un phénotype de réparation plutôt que pro-inflammatoire. Les CDCs ont fait l’objet de plus de 250 publications scientifiques à comité de lecture et ont été administrées à plus de 250 sujets humains dans le cadre de plusieurs essais cliniques.
Deramiocel a reçu la désignation de médicament orphelin pour le traitement de la DMD de la part de la FDA américaine et de l’Agence européenne des médicaments (EMA). Il a également obtenu la désignation Regenerative Medicine Advanced Therapy (RMAT) aux États-Unis, la désignation Advanced Therapy Medicinal Product (ATMP) en Europe, et la désignation Rare Pediatric Disease de la FDA, ce qui pourrait permettre à Capricor d’obtenir un bon de priorité d’examen en cas d’approbation.
À propos de l’essai HOPE-3 de Phase 3
HOPE-3 est un essai clinique de Phase 3, multicentrique, randomisé, en double aveugle et contrôlé par placebo, composé de deux cohortes évaluant la sécurité et l’efficacité de Deramiocel chez des participants atteints de DMD. Des garçons ambulatoires et non-ambulatoires répondant aux critères d’éligibilité ont été répartis de manière aléatoire pour recevoir soit Deramiocel, soit un placebo tous les 3 mois pour un total de quatre doses au cours des 12 premiers mois de l’essai. Au total, 106 sujets ont été randomisés dans cet essai à double cohorte.
À propos de Capricor Therapeutics
Capricor Therapeutics (NASDAQ : CAPR) est une société de biotechnologie dédiée au développement de thérapies innovantes à base de cellules et d’exosomes afin de redéfinir le paysage thérapeutique des maladies rares. Au cœur de notre innovation se trouve notre candidat principal, Deramiocel, une thérapie cellulaire d’origine cardiaque allogénique actuellement en développement avancé pour le traitement de la dystrophie musculaire de Duchenne (DMD). De nombreuses données précliniques et cliniques ont démontré les effets puissants de Deramiocel sur l’immunomodulation et l’anti-fibrose pour préserver la fonction musculaire cardiaque et squelettique dans la DMD. Capricor exploite également la puissance de sa technologie des exosomes, utilisant sa plateforme propriétaire StealthX™ en développement préclinique axée sur la vaccinologie et l’administration ciblée d’oligonucléotides, de protéines et de petites molécules thérapeutiques, avec le potentiel de traiter et prévenir un large éventail de maladies. Chez Capricor, nous nous engageons à repousser les limites du possible et à ouvrir la voie à des traitements transformateurs pour ceux qui en ont besoin.
Note de prudence concernant les déclarations prospectives
Capricor a conclu un accord pour la commercialisation et la distribution exclusive de Deramiocel pour la DMD aux États-Unis et au Japon avec Nippon Shinyaku Co., Ltd. (filiale américaine : NS Pharma, Inc.), sous réserve de l’approbation réglementaire. Deramiocel et le vaccin StealthX™ sont des candidats en phase d’investigation et n’ont été approuvés dans aucune indication à des fins commerciales.
Avertissement : le contenu de cet article reflète uniquement le point de vue de l'auteur et ne représente en aucun cas la plateforme. Cet article n'est pas destiné à servir de référence pour prendre des décisions d'investissement.
Vous pourriez également aimer
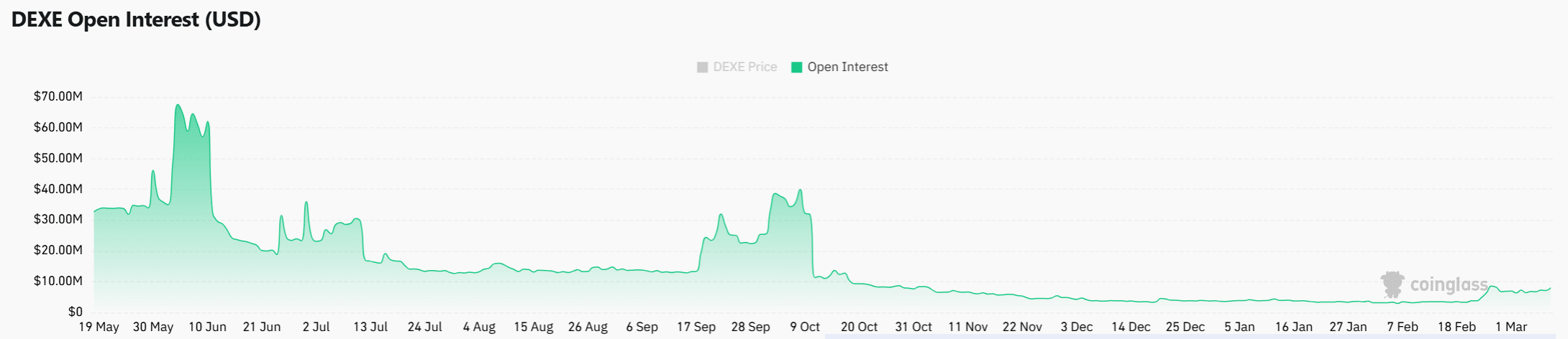
DEXE bondit de 17 % alors que les acheteurs dominent : une cassure poussera-t-elle vers 7 $ ?
Live Nation approche d'un accord avec le DOJ qui n'exigerait pas la vente de Ticketmaster



