BridgeBio riporta risultati positivi di fase 3 per l'infigratinib orale con i primi miglioramenti statisticamente significativi nella proporzionalità corporea nell'acondroplasia
- PROPEL 3 ha raggiunto con successo l’endpoint primario relativo al cambiamento rispetto al basale nella AHV alla Settimana 52 (p<0,0001)
- Il cambiamento rispetto al basale nella AHV è stato superiore al placebo alla Settimana 52 con una differenza media di trattamento rispetto al placebo di +2,10 cm/anno; la LS media è stata di +1,74 cm/anno
- In un’analisi esplorativa pre-specificata dell’endpoint secondario chiave, l’infigratinib orale ha ottenuto il primo miglioramento statisticamente significativo nella proporzionalità corporea rispetto al placebo nell’acondroplasia, dimostrando una differenza media di trattamento LS di -0,05 (p<0,05) rispetto al placebo nei bambini di età inferiore a 8 anni (>50% dei partecipanti)
- PROPEL 3 ha raggiunto con successo l’endpoint secondario chiave relativo al cambiamento rispetto al basale nel punteggio Z dell’altezza (popolazione di riferimento per acondroplasia) alla Settimana 52 (p<0,0001), con un aumento LS medio nel braccio di trattamento di +0,41 SD
- L’infigratinib orale è stato ben tollerato, senza interruzioni o eventi avversi gravi correlati al farmaco in studio, 3 casi (4%) di iperfosfatemia considerati lievi e transitori senza alcun caso che abbia richiesto riduzione della dose o interruzione, e nessun evento avverso associato all’inibizione di FGFR1 o 2 (ad es., retinico o corneale)
- NDA e MAA sono previsti per la seconda metà del 2026 per l’acondroplasia; l’infigratinib orale è l’unica opzione terapeutica in sviluppo per l’acondroplasia ad aver ottenuto la Breakthrough Therapy Designation dalla FDA
- Dato il valore di questi dati, BridgeBio prevede di accelerare lo sviluppo dell’infigratinib orale nell’ipocondroplasia e sta reclutando i partecipanti per la fase osservazionale run-in dello studio di Fase 3
PALO ALTO, Calif., 12 febbraio 2026 (GLOBE NEWSWIRE) -- BridgeBio Pharma, Inc. (Nasdaq: BBIO) (“BridgeBio” o la “Società”), azienda biofarmaceutica focalizzata sullo sviluppo di farmaci per condizioni genetiche, ha annunciato oggi risultati positivi di topline da PROPEL 3, lo studio pivotale globale di Fase 3 dell’infigratinib orale in bambini affetti da acondroplasia. BridgeBio ospiterà una call per gli investitori il 12 febbraio 2026 alle 8:00 ET per discutere questi risultati.
"L’acondroplasia è una condizione genetica guidata da FGFR3 che influisce non solo sulla statura, ma anche su funzioni fisiche e indipendenza con conseguenze che si estendono per tutta la vita di una persona,” ha dichiarato Ravi Savarirayan, M.D., Ph.D. del Murdoch Children’s Research Institute di Melbourne, Australia, e responsabile globale per PROPEL 3. “L’infigratinib è la prima terapia orale progettata per colpire FGFR3 e affrontare direttamente la causa sottostante dell’acondroplasia. Nel più ampio range di età studiato fino a oggi, l’infigratinib orale ha dimostrato il miglioramento più alto e significativo nella velocità di crescita annualizzata, insieme al primo miglioramento statisticamente significativo nella proporzionalità corporea, nei bambini da 3 a 8 anni, riportato per qualsiasi terapia approvata o in sviluppo per questa condizione. Questi risultati best-in-class evidenziano il potenziale trasformativo dell’infigratinib nell’affrontare aspetti dell’acondroplasia oltre l’altezza lineare, con un prodotto somministrato per via orale.”
PROPEL 3 è stato uno studio clinico globale, della durata di un anno, randomizzato 2:1, in doppio cieco e controllato con placebo, che ha valutato l’efficacia e la sicurezza dell’infigratinib in bambini con acondroplasia di età compresa tra 3 e <18 anni con placche di crescita aperte. I principali risultati dello studio fino alla Settimana 52 includono:
- Endpoint primario:
- Cambiamento rispetto al basale nella velocità di crescita annualizzata (AHV) superiore al placebo, con una differenza media di trattamento LS di +1,74 cm/anno (p<0,0001) e una differenza media di trattamento di +2,10 cm/anno
- Endpoint secondari:
- In linea con l’endpoint primario, l’endpoint secondario dell’AHV assoluta alla Settimana 52 ha mostrato un miglioramento significativo con l’infigratinib rispetto al placebo, con il braccio infigratinib che ha raggiunto la più alta LS media assoluta di AHV riportata fino a oggi in uno studio randomizzato sull’acondroplasia (5,96 cm/anno contro 4,22 cm/anno con placebo)
- Cambiamento rispetto al basale nel punteggio Z dell’altezza (popolazione di riferimento per acondroplasia) superiore al placebo, con una differenza media di trattamento LS di +0,32 SD (p<0,0001), la differenza più grande osservata in uno studio randomizzato su acondroplasia; la variazione LS media rispetto al basale nel braccio di trattamento è stata di +0,41 SD, il miglioramento più grande osservato in un braccio di trattamento in uno studio randomizzato per acondroplasia
- In un’analisi esplorativa pre-specificata (bambini di età inferiore a 8 anni; >50% dei partecipanti) dell’endpoint secondario chiave sul cambiamento rispetto al basale nella proporzionalità tra parte superiore e inferiore del corpo alla Settimana 52, l’infigratinib orale è la prima opzione terapeutica a mostrare significatività statistica rispetto al placebo in uno studio randomizzato per acondroplasia, dimostrando una riduzione LS media di -0,05 rispetto al placebo (p<0,05)
- Nella popolazione complessiva, l’infigratinib ha ottenuto una riduzione LS media di -0,05, la riduzione maggiore osservata in un braccio di trattamento in uno studio randomizzato su acondroplasia, con una differenza di trattamento LS favorevole di -0,02 rispetto al placebo alla Settimana 52 (p=0,1849)
- L’infigratinib è stato ben tollerato, con:
- Nessuna interruzione correlata al farmaco in studio
- Nessun evento avverso grave correlato al farmaco in studio
- 3 casi (4%) di iperfosfatemia, tutti lievi, transitori, asintomatici e non richiedenti riduzione della dose o interruzione
- Nessun evento avverso associato all’inibizione di FGFR1 o FGFR2 (ad es., retinico o corneale)
- Nessun evento avverso associato ad analoghi CNP: ipotensione sintomatica, reazioni nel sito di iniezione, o ipertricosi
“Rimane un significativo bisogno insoddisfatto di opzioni terapeutiche efficaci, pratiche e meno invasive per i bambini che vivono con acondroplasia,” ha dichiarato Daniela Rogoff, M.D., Chief Medical Officer, Skeletal Dysplasia di BridgeBio. “I dati di PROPEL 3 supportano il potenziale di un farmaco orale che colpisce direttamente l’iperattività di FGFR3 per rispondere a importanti bisogni clinici, integrandosi nella vita quotidiana delle famiglie che cercano un’opzione non iniettabile. Questi risultati rappresentano un progresso significativo per coloro che attendevano un approccio migliore e non vediamo l’ora di portare avanti questo programma verso le sottomissioni globali. Vorremmo ringraziare i partecipanti allo studio, le loro famiglie, gli investigatori e il personale che ci hanno dato fiducia e ci hanno accompagnato in questo percorso.”
Sulla base di questi risultati, BridgeBio intende incontrare le autorità regolatorie per discutere i piani di sottomissione di una New Drug Application (NDA) e di una Marketing Authorization Application (MAA) per l’infigratinib nella seconda metà del 2026 a supporto dell’approvazione. La Società intende inoltre accelerare lo sviluppo dell’infigratinib per l’ipocondroplasia, e sta reclutando partecipanti nella fase osservazionale run-in dello studio di Fase 3. La Società ha inoltre uno studio clinico in corso sull’infigratinib nei neonati e bambini fino a <3 anni con acondroplasia nello studio PROPEL Infant & Toddler. L’infigratinib ha ricevuto la Breakthrough Designation dalla FDA per l’acondroplasia, così come la Orphan Drug Designation (FDA & EMA), la Fast Track Designation e la Rare Pediatric Disease Designation.
“L’annuncio di oggi rappresenta un’altra pietra miliare nella ricerca sull’acondroplasia e, in attesa della revisione regolatoria, amplia le opzioni di cura disponibili includendo una terapia orale, offrendo a individui e famiglie una scelta aggiuntiva mentre considerano i loro obiettivi e preferenze di salute,” ha dichiarato Michael Hughes, Presidente del Biotech Industry Liaison Committee presso Little People of America. “L’impegno di BridgeBio nel coinvolgere e apprendere dalla comunità delle persone di bassa statura riflette l’attenzione all’ascolto dell’esperienza vissuta e al riconoscimento di priorità diverse nel definire gli sforzi di ricerca. In questo contesto, il miglioramento osservato nella proporzionalità corporea dopo un anno di trattamento nello studio PROPEL 3 è un risultato identificato come significativo da individui e famiglie, potrebbe essere rilevante per la funzione fisica e continua a essere valutato per comprenderne la portata.”
Informazioni sullo studio PROPEL Infant & Toddler (NCT07169279) sono disponibili su clinicaltrials.gov. Informazioni su ACCEL, lo studio osservazionale lead-in dell’azienda per l’infigratinib nello studio di Fase 3 per l’ipocondroplasia, (NCT06410976) sono disponibili , così come informazioni su ACCEL 2/3, lo studio clinico di Fase 2/3 di BridgeBio sull’infigratinib nell’ipocondroplasia, (NCT06873035). BridgeBio si impegna a esplorare il potenziale dell’infigratinib sugli impatti medici e funzionali più ampi di acondroplasia, ipocondroplasia e altre displasie scheletriche, che rappresentano un notevole bisogno insoddisfatto per le famiglie.
Informazioni sul Webcast
BridgeBio ospiterà una call per investitori e un webcast simultaneo per discutere i risultati dello studio di Fase 3 PROPEL 3 dell’infigratinib nei bambini con acondroplasia il 12 febbraio 2026 alle 8:00 ET. Un link al webcast sarà disponibile dalla pagina calendario eventi del sito di BridgeBio. Una registrazione della conference call e del webcast sarà archiviata sul sito della Società e disponibile per almeno 30 giorni dopo l’evento.
Informazioni sull’Acondroplasia
L’acondroplasia è la causa più comune di bassa statura sproporzionata, colpendo circa 55.000 persone negli Stati Uniti e nell’Unione Europea (UE), inclusi fino a 10.000 bambini e adolescenti con placche di crescita aperte. L’acondroplasia influisce sulla salute generale e sulla qualità della vita, portando a complicanze mediche quali apnea ostruttiva del sonno, disfunzione dell’orecchio medio, cifosi e stenosi spinale. La condizione è uniformemente causata da una variante attivante in FGFR3.
Informazioni su BridgeBio Pharma, Inc.
BridgeBio esiste per sviluppare farmaci trasformativi per condizioni genetiche. Milioni di persone nel mondo che vivono con condizioni genetiche non hanno opzioni terapeutiche, spesso perché lo sviluppo di farmaci per popolazioni di pazienti ridotte può essere una sfida commerciale. Il nostro obiettivo è colmare il divario tra i progressi nella scienza genetica e farmaci significativi per popolazioni di pazienti trascurate. Il nostro modello decentralizzato hub-and-spoke è progettato per rapidità, precisione e scalabilità. Team autonomi e responsabilizzati si concentrano su singole condizioni, mentre un hub centrale fornisce le capacità cliniche, regolatorie e commerciali necessarie per portare l’innovazione sul mercato. Per ulteriori informazioni, visitate e seguiteci su , , , , , e .
Esclusione di responsabilità: il contenuto di questo articolo riflette esclusivamente l’opinione dell’autore e non rappresenta in alcun modo la piattaforma. Questo articolo non deve essere utilizzato come riferimento per prendere decisioni di investimento.
Ti potrebbe interessare anche
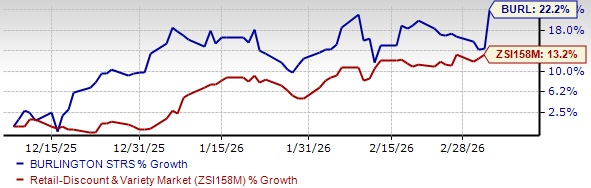
Gap vede un'opportunità di recupero favorita dalle condizioni meteorologiche dopo un calo netto del 10%
La divisione Neuroscienze di AbbVie continuerà a guidare la crescita dei ricavi nel 2026?
Il prezzo di VIA aumenta dell'11,96%: i trader notano un'attività di mercato insolita

