Nature Medicine pubblica lo studio randomizzato, controllato con placebo di fase 2a di Helus Pharma su SPL026 nel disturbo depressivo maggiore
- Lo studio randomizzato, controllato con placebo di Fase 2a su SPL026 ha raggiunto il suo endpoint primario dimostrando una riduzione clinicamente significativa dei sintomi depressivi misurata dal punteggio MADRS (differenza media: -7,35) rispetto al placebo a due settimane
- Gli effetti antidepressivi sono stati osservati entro una settimana e mantenuti fino a tre mesi
- I risultati rafforzano il potenziale terapeutico degli agonisti serotoninergici ad azione breve e informano il programma di sviluppo HLP004 di Helus Pharma, con i dati principali di Fase 2 nel disturbo d’ansia generalizzato (“GAD”) previsti nel Q1 2026
Questo comunicato stampa costituisce una “designated news release” ai fini del supplemento al prospetto della Società datato 30 dicembre 2025, relativo al prospetto base short form datato 17 settembre 2025, come modificato il 19 dicembre 2025.
BOSTON e TORONTO, 17 febbraio 2026 (GLOBE NEWSWIRE) -- Helus Pharma™ (Nasdaq: HELP) (Cboe CA: HELP), azienda farmaceutica in fase clinica che sviluppa nuovi agonisti serotoninergici (“NSA”) per gravi condizioni di salute mentale, ha annunciato oggi la pubblicazione
Lo studio ha raggiunto il suo endpoint primario dimostrando riduzioni statisticamente significative e clinicamente rilevanti dei sintomi depressivi a due settimane, misurate con la Montgomery-Åsberg Depression Rating Scale (“MADRS”) nei partecipanti trattati con SPL026 rispetto al placebo. Riduzioni dei sintomi depressivi sono state osservate già una settimana dopo la somministrazione e mantenute a tre mesi, con effetti che perdurano fino a sei mesi in alcuni partecipanti. Il trattamento è stato generalmente ben tollerato, senza eventi avversi gravi correlati al trattamento segnalati.
“Abbiamo dimostrato che una singola dose di SPL026 è sicura, efficace e duratura, con effetti di trattamento comparabili ad altri trattamenti interventistici promettenti che spesso richiedono sessioni molto più lunghe.” Il Dr. David Erritzoe, del Dipartimento di Scienze del Cervello dell’Imperial College e principale investigatore dello studio, ha continuato: “Sebbene questi risultati iniziali debbano sempre essere interpretati con cautela, questi dati mostrano il potenziale della DMT come trattamento clinico per la depressione potenzialmente più conveniente rispetto ad agonisti serotoninergici correlati con azione psicoattiva più lunga, grazie a sessioni di somministrazione più brevi.”
Questo studio di Fase 2a ha valutato l’efficacia e la sicurezza di SPL026. I partecipanti che hanno ricevuto una singola dose di 21,5 mg di SPL026 (n=17) hanno mostrato una riduzione significativa del punteggio MADRS rispetto al placebo (n=17) a due settimane, raggiungendo l’endpoint primario (differenza media: -7,35; IC 95%, -13,62 a –1,08; p=0,023). L’effetto del trattamento con SPL026 era evidente già a una settimana (differenza media: -10,75; IC 95%, -16,95 a –4,55; p=0,002). I tassi di risposta (≥50% di riduzione MADRS) alla settimana 2 erano del 35% per SPL026 contro il 12% per il placebo, con tassi di remissione (MADRS ≤10) del 29% contro il 12%. Durante la fase open-label dello studio, l’effetto del trattamento è stato mantenuto fino a tre mesi.
“Questa pubblicazione rappresenta una validazione importante degli agonisti serotoninergici ad azione breve come approccio clinicamente rilevante nei trattamenti per la salute mentale,” ha dichiarato Michael Cola, Chief Executive Officer di Helus Pharma. “I risultati forniscono una prova di concetto clinica per la modulazione serotoninergica ad azione breve e sostengono ulteriormente la nostra convinzione che le nostre nuove molecole agoniste serotoninergiche, come HLP004, possano potenzialmente offrire risultati significativi con maggiore coerenza e fattibilità commerciale. Non vediamo l’ora di presentare i dati principali del nostro studio di Fase 2 su HLP004 nel disturbo d’ansia generalizzato nel corso di questo trimestre.”
<pSebbene Helus Pharma non stia portando avanti la forma attuale di SPL026 per via endovenosa, le intuizioni meccanistiche e cliniche generate da questo studio continuano a informare il programma di sviluppo di HLP004 della Società. Helus sta attualmente sviluppando HLP004, un NSA proprietario, progettato per ottimizzare farmacologia, coerenza e scalabilità per il GAD, di cui SPL026 è un analogo non deuterato.
Informazioni sullo studio
Lo studio è stato condotto presso Hammersmith Medicines Research Ltd (Londra), MAC Clinical Research (Liverpool) e Imperial College London. Questo studio è stato condotto da Helus Pharma Corp., una controllata interamente posseduta da Helus Pharma e entità successiva di Small Pharma Inc. Lo studio era uno studio randomizzato di Fase 2a controllato con placebo che valutava la sicurezza e l’efficacia di SPL026 in adulti con disturbo depressivo maggiore da moderato a grave. Sono stati arruolati 34 partecipanti (età media 32,8 anni, 29,4% donne, prevalentemente bianchi) che avevano sperimentato la depressione per una media di 10,5 anni. I partecipanti sono stati randomizzati in doppio cieco per ricevere una singola infusione endovenosa di 21,5 mg di SPL026 per 10 minuti o placebo, combinata con sessioni di psicoterapia di supporto focalizzate su preparazione, integrazione ed elaborazione emotiva.
Nella Fase 1 in cieco, l’endpoint primario era la variazione dei punteggi MADRS dal basale alla settimana 2. La Fase 2 era un’estensione open-label in cui tutti i partecipanti potevano ricevere una seconda dose di SPL026 due settimane dopo; gli effetti antidepressivi sono persistiti fino a tre mesi dalla prima dose.
Informazioni su Helus Pharma
Helus Pharma™, nome commerciale operativo di Cybin Inc. (la “Società” o “Helus Pharma”) è una società farmaceutica in fase clinica impegnata ad aiutare la mente a guarire sviluppando NSA proprietari: molecole sintetiche progettate per attivare i percorsi della serotonina che si ritiene promuovano la neuroplasticità. Gli NSA proprietari della Società sono destinati potenzialmente a rispondere all’ampio bisogno insoddisfatto delle persone che soffrono di depressione, ansia e altre condizioni di salute mentale.
Con dati leader di settore, Helus Pharma mira a migliorare il panorama dei trattamenti attraverso l’introduzione di NSA che puntano a fornire miglioramenti duraturi nella salute mentale. Helus Pharma sta attualmente sviluppando HLP003, un NSA proprietario, in sviluppo clinico di Fase 3 per il trattamento aggiuntivo del disturbo depressivo maggiore che ha ricevuto la Breakthrough Therapy Designation dalla U.S. Food and Drug Administration, e HLP004, anch’esso un NSA proprietario in Fase 2 per il disturbo d’ansia generalizzato. Inoltre, Helus Pharma dispone di un ampio portafoglio di ricerca di NSA sperimentali.
La Società opera in Canada, Stati Uniti, Regno Unito e Irlanda. Per gli aggiornamenti della Società e per saperne di più su Helus Pharma, visita o segui il team su X, LinkedIn, YouTube e Instagram. Helus Pharma™ è un marchio registrato di Cybin Corp.
Esclusione di responsabilità: il contenuto di questo articolo riflette esclusivamente l’opinione dell’autore e non rappresenta in alcun modo la piattaforma. Questo articolo non deve essere utilizzato come riferimento per prendere decisioni di investimento.
Ti potrebbe interessare anche
Ultimi 6 giorni per guadagni 500x nella vendita diretta di BlockDAG mentre Solana e Dogecoin affrontano la pressione del mercato!
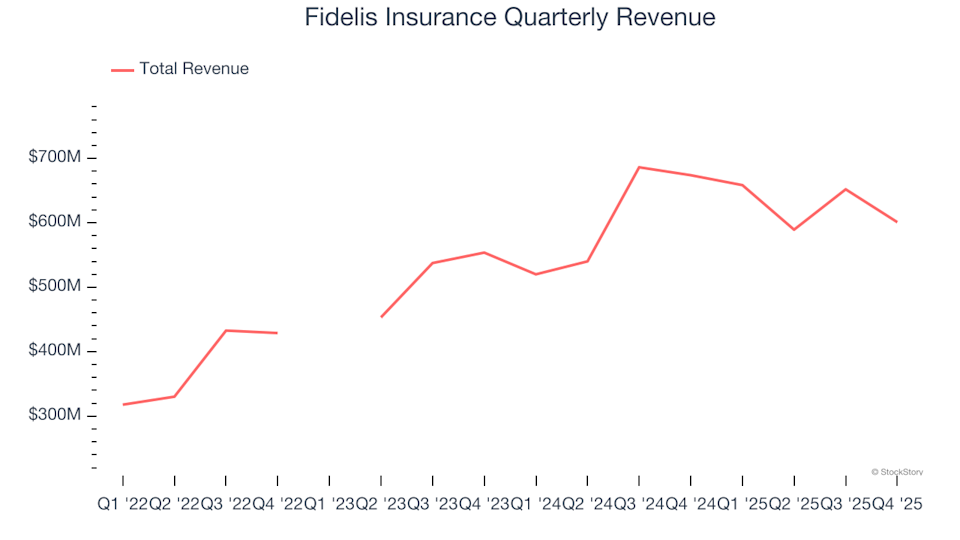
Fidelis Insurance (NYSE:FIHL) registra ricavi del Q4 CY2025 inferiori alle previsioni degli analisti

BJ's Restaurants: Panoramica degli utili del quarto trimestre

