DNLI riporta una perdita nel quarto trimestre inferiore alle attese, attenzione focalizzata sul trattamento della sindrome di Hunter
Denali Therapeutics Panoramica Finanziaria Q4 2025
Denali Therapeutics (DNLI) ha registrato una perdita netta per azione di $0,73 nel quarto trimestre del 2025, leggermente migliore rispetto alla stima di consenso di una perdita di $0,75. Questo dato si confronta con una perdita di $0,67 per azione nello stesso periodo dell'anno precedente.
L'aumento anno su anno della perdita per azione è stato principalmente determinato da maggiori spese operative.
Poiché Denali non ha ancora prodotti sul mercato, i suoi ricavi sono limitati ai proventi delle partnership in corso. Nel trimestre riportato, la società non ha registrato alcun ricavo da collaborazioni, risultando inferiore rispetto agli $18 milioni attesi.
Nell'ultimo anno, le azioni DNLI sono aumentate del 13,4%, sovraperformando il settore medico, biomedico e genetico, che ha registrato un incremento dell'11,5%.
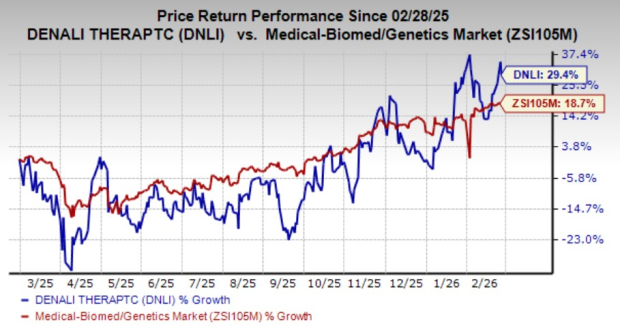
Fonte: Zacks Investment Research
Punti Chiave dai Risultati del Q4
- I costi di ricerca e sviluppo sono diminuiti dell'1,9% a $97,9 milioni, principalmente grazie a una riduzione delle spese nei progetti di piccole molecole.
- Le spese generali e amministrative sono salite del 31,3% a $39,5 milioni, riflettendo i preparativi per il previsto lancio di tividenofusp alfa.
- Al 31 dicembre 2025, Denali deteneva circa $966,2 milioni in contanti, equivalenti di cassa e titoli negoziabili.
Riepilogo dell’Anno Intero 2025
- Nel 2025 non sono stati generati ricavi.
- La perdita annuale per azione si è ampliata a $2,97, rispetto ai $2,57 del 2024.
Progresso sul Principale Farmaco Candidato
Denali sta attivamente preparando l'introduzione commerciale del suo asset principale, tividenofusp alfa.
La domanda di autorizzazione biologica (BLA) per tividenofusp alfa, mirata al trattamento della mucopolisaccaridosi di tipo II (sindrome di Hunter), è attualmente in fase di revisione da parte delle autorità statunitensi.
La FDA ha esteso la scadenza della revisione dal 5 gennaio 2026 al 5 aprile 2026.
Tividenofusp alfa ha ricevuto diverse designazioni dalla FDA, tra cui Breakthrough Therapy, Fast Track, Orphan Drug e Rare Pediatric Disease.
Questa terapia sperimentale è progettata per fornire l’enzima iduronato-2-sulfatasi (IDS) attraverso la barriera emato-encefalica, mirando sia al corpo che al cervello.
Il periodo di revisione della BLA è stato prolungato dopo che Denali ha fornito dati aggiornati di farmacologia clinica in risposta a una richiesta della FDA. L’azienda ha chiarito che questo aggiornamento non era correlato a efficacia, sicurezza o biomarcatori.
La FDA ha classificato la presentazione come una modifica importante, determinando così l'estensione della data di azione.
Il trial globale di fase II/III COMPASS in corso dovrebbe fornire prove a supporto delle richieste regolatorie a livello mondiale, con il completamento dell’arruolamento per i partecipanti neuronopatici (Cohorte A) a dicembre 2025.
Sviluppi della Pipeline
- Denali sta studiando DNL126 per la sindrome di Sanfilippo tipo A (MPS IIIA). I risultati preliminari di fase I/II presentati al WORLDSymposium hanno mostrato significative riduzioni nei principali biomarcatori della malattia e un profilo di sicurezza simile alle attuali terapie di sostituzione enzimatica. Questi risultati potrebbero supportare un percorso di approvazione accelerata, ed è previsto uno studio confermatorio di fase III.
- Altri candidati della pipeline sono sviluppati in collaborazione con Takeda (TAK), Biogen (BIIB) e Sanofi (SNY).
- Denali e Takeda stanno portando avanti DNL593, un potenziale trattamento per la demenza frontotemporale associata a mutazioni del gene granulina (FTD-GRN). L’arruolamento nello studio di fase I/II è completo, con 40 partecipanti. I primi dati sui pazienti sono attesi nel 2026.
- Denali ha recentemente ricevuto l'approvazione per uno studio di fase Ib su DNL628, con i preparativi in corso.
- Denali e Biogen stanno sviluppando congiuntamente BIIB122. Biogen guida lo studio globale di fase IIb LUMA per il morbo di Parkinson in fase iniziale, con risultati attesi a metà 2026. Denali sta conducendo lo studio di fase IIa BEACON per valutare l'inibizione di LRRK2 nel Parkinson associato a LRRK2.
- In ottobre, Denali ha presentato una IND per DNL952 (ETV:GAA) per avviare studi clinici nella malattia di Pompe. La FDA ha successivamente revocato la sospensione clinica e sono in corso i preparativi per lo studio di fase I.
- Sanofi sta sviluppando eclitasertib per la colite ulcerosa da moderata a grave, con dati di fase II attesi nella prima metà dell’anno.
Analisi delle Prospettive di Denali
L’approvazione di tividenofusp alfa potrebbe migliorare sensibilmente la traiettoria di crescita di Denali. Anche i progressi con DNL126 sono promettenti.
Le solide riserve di liquidità dell’azienda evidenziano la sua capacità di sostenere le iniziative di ricerca e sviluppo in corso.
Esclusione di responsabilità: il contenuto di questo articolo riflette esclusivamente l’opinione dell’autore e non rappresenta in alcun modo la piattaforma. Questo articolo non deve essere utilizzato come riferimento per prendere decisioni di investimento.
Ti potrebbe interessare anche

Il debito delle famiglie sta sopraffacendo le persone negli Stati Uniti. Ecco come puoi rispondere
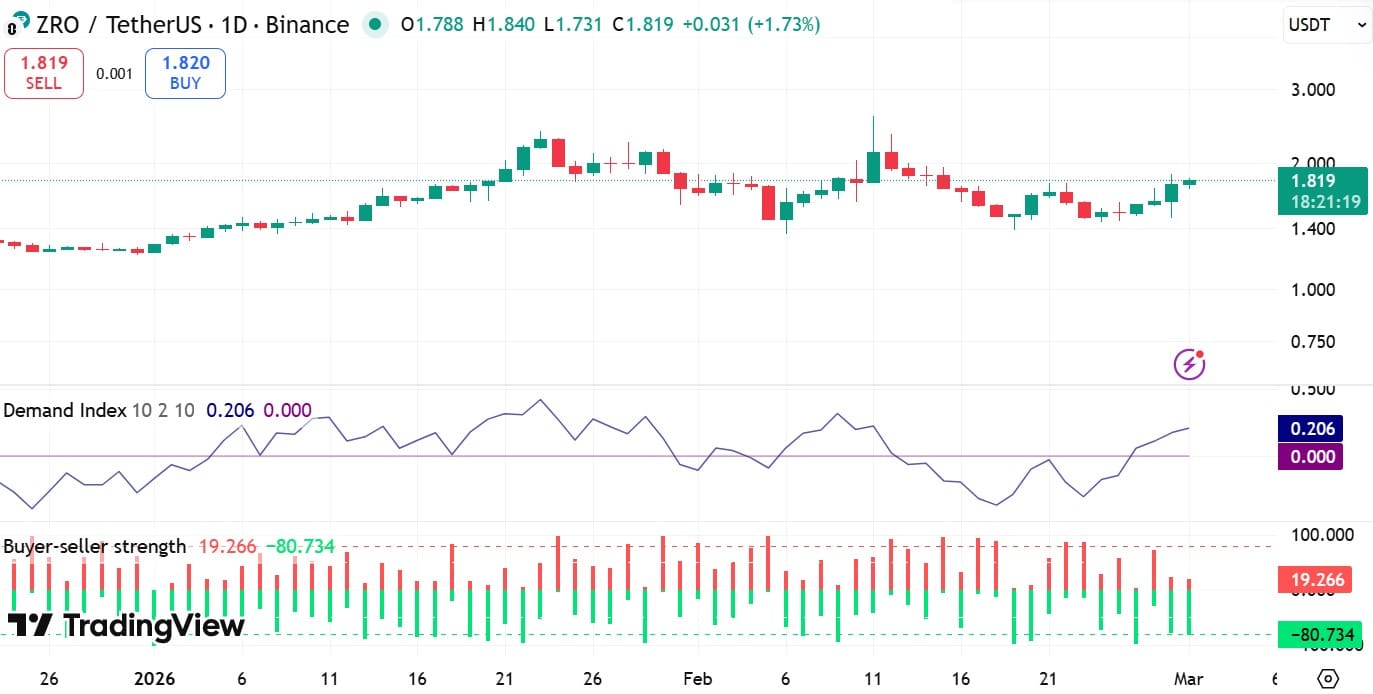
I trader, LayerZero è diventato rialzista – ZRO punta a $2,00, ma rimangono QUESTI rischi