Edesa Biotech Nag-ulat ng Karagdagang Positibong Resulta mula sa Phase 3 Paridiprubart na Pag-aaral
- Ang resulta mula sa populasyon ng 278 pasyente ay nagpapatunay ng estadistikang makabuluhang pagbawas ng mortality
- Ang mga benepisyo ay nakita sa lahat ng antas ng kalubhaan at sa mga pasyenteng may seryosong comorbidities
- Nagsumite ang kumpanya ng mga provisional patent application para sa sepsis, acute kidney injury at pneumonia
- Sinusuri ang mga estratehikong kolaborasyon upang suportahan ang huling yugto ng pag-unlad at komersyalisasyon
- Napili ang resulta ng pag-aaral para sa oral presentation sa ATS 2026 conference
TORONTO, Peb. 24, 2026 (GLOBE NEWSWIRE) -- Inanunsyo ngayon ng Edesa Biotech, Inc. (Nasdaq:EDSA), isang clinical-stage biopharmaceutical company na nakatuon sa pag-develop ng host-directed therapeutics para sa immuno-inflammatory diseases, ang positibong karagdagang datos mula sa Phase 3 na pag-aaral ng paridiprubart.
Ang mga resulta ay nagmumula sa mas malawak na populasyon ng 278 pasyente, na kinabibilangan ng naunang naiulat na 104 pasyente na nangangailangan ng invasive mechanical ventilation (IMV) pati na rin ng 174 non-IMV na pasyente. Sa buong populasyon na ito, ang kauna-unahang anti-TLR4 antibody ng kumpanya ay nagpakita ng estadistikang makabuluhang pagbawas sa 28-araw na mortality. Ang mga benepisyo ng paggamot ay naging konsistente sa lahat ng grupo ng kalubhaan at sa mga pasyenteng may seryosong comorbidities.
Pangunahing Natuklasan
Naabot ang pangunahing endpoint para sa buong populasyon ng paggamot na binubuo ng 278 randomisadong kalahok. Binawasan ng paridiprubart ang adjusted 28-araw na mortality sa 24% mula 33%, isang 27% relative reduction sa panganib ng pagkamatay (p<0.001). Bukod dito, ang mga pasyenteng tumanggap ng paridiprubart ay nagpakita ng mas mataas na relative rate ng klinikal na pagbuti pagsapit ng Araw 28. Ang paridiprubart o placebo ay ibinigay bilang karagdagan sa mga standard na paggamot (SOC).
Sa isang exploratory analysis ng mas magaan na populasyon ng 174 randomisadong pasyente na hindi umabot sa IMV-based inclusion criteria ng pag-aaral, binawasan ng paridiprubart + SOC ang adjusted 28-araw na mortality sa 15% mula 23% (placebo + SOC), isang 35% relative reduction sa panganib ng pagkamatay (p<0.05).
Nag-ulat din ang Edesa na ang exploratory analyses sa populasyon ng hanggang 108 randomisadong pasyente ay palaging nagpakita ng nabawasang adjusted mortality para sa paridiprubart + SOC kumpara sa placebo + SOC pagdating ng 28 araw sa mga pasyenteng may klinikal na mahalagang comorbidities:
- Acute Kidney Injury: 35% relative reduction (35% paridiprubart vs. 53% placebo; p<0.05, n=48)
- Sepsis: 36% relative reduction (40% paridiprubart vs. 63% placebo; p<0.05, n=41)
- Pneumonia: 30% relative reduction (35% paridiprubart vs. 49% placebo; p<0.05, n=108)
Sa pangkalahatan, ang mga antas ng adverse events, seryosong adverse events, impeksyon at pagtigil ng paggamot ay mababa at halos magkapareho sa pagitan ng paridiprubart at placebo na mga grupo. Ang safety profile ay kapareho ng mga naunang clinical exposures, na may higit sa 400 pasyente na nakatanggap na ng paridiprubart.
Batay sa mga positibong resulta na ito, nagsumite ang Edesa ng provisional patent applications sa United States Patent and Trademark Office na sumasaklaw sa paggamit ng paridiprubart sa paggamot ng sepsis, acute kidney injury at pneumonia. Ang pangunahing composition-of-matter patents ng kumpanya ay umaabot hanggang 2030s.
Ipinahayag ni Par Nijhawan, MD, Chief Executive Officer ng Edesa Biotech, na ang mga resultang inanunsyo ngayon ay umaayon sa sentral na papel ng TLR4 sa hyperinflammatory ARDS (Acute Respiratory Distress Syndrome) at nagpapakita ng konsistenteng benepisyo sa iba’t ibang sanhi ng mataas na mortality.
“Ang konsistensya ng pagbawas ng mortality at klinikal na pagpapabuti sa lahat ng 278 randomisadong pasyente, kabilang ang mas hindi malubhang pasyente pati na rin yaong may ARDS na may kasamang acute kidney injury, sepsis at pneumonia, ay higit na nagpapakita ng versatility at transformasyong potensyal ng paridiprubart upang tugunan ang maraming kritikal na hindi natutugunang pangangailangang medikal,” ani Dr. Nijhawan. “Pinapaigting namin ang regulatory discussions at sinusuri ang mga estratehikong kolaborasyon at partnership opportunities na maaaring magpabilis ng pag-unlad at magpalawak ng global access.” Binanggit din niya na isinasagawa na ang manufacturing scale-up planning.
Kasalukuyang sinusuri ang paridiprubart sa isang hiwalay na U.S. government-funded na pag-aaral ng ARDS patients. Tumatanggap pa ng mga kalahok para sa hanggang tinatayang 200 randomisadong kalahok para sa Edesa cohort. Ang paridiprubart development program ng kumpanya, kabilang ang manufacturing scale-up, late-stage development at commercial readiness, ay tumatanggap din ng pondo mula sa Government of Canada.
Napili ang Edesa para sa isang oral presentation sa American Thoracic Society (ATS) 2026 International Conference (Mayo 15-20, 2026) at planong iprisenta ang karagdagang natuklasan mula sa Phase 3 na pag-aaral nito sa iba pang paparating na medikal at siyentipikong mga kumperensya.
Detalyadong Resulta
Ang datos ay nakuha mula sa buong study safety population ng 278 pasyente; ang naunang naiulat na 104-pasyenteng IMV ITT cohort ay kumakatawan sa isang prespecified subset ng populasyong ito. Ang mga pasyente sa buong 278-pasyenteng safety population ay random na itinalaga (1:1) sa SOC na may paridiprubart (n=138), o SOC na may placebo (n=140). Ang baseline characteristics at SOC ay balanse sa pagitan ng treatment groups.
Ang mga sumusunod na talahanayan ay nagbubuod ng mga pangunahing karagdagang resulta:
Pangunahing Endpoint: Antas ng Mortality sa 28 Araw
Multivariate Logistic Regression Derived Risk Differences, 95%CI
| Population | Paridiprubart | Placebo | P-Value |
| Lahat (n=278) | 0.24 (0.21, 0.27) | 0.33 (0.29, 0.37) | <0.001 |
| IMV ITT (n=104) | 0.39 (0.35, 0.44) | 0.52 (0.47, 0.58) | <0.001 |
Adjusted model derived adjusted mortality estimates: mga variable na kasama ay edad, baseline WHO Covid-19 Severity Scale (WCSS), baseline antiviral use, baseline corticosteroid use, baseline immunomodulator use, kasabay na antiviral use, kasabay na corticosteroid use, kasabay na immunomodulator use. Lahat (safety population) n=278; Intent to treat (ITT) IMV population n=104
Sekondaryang Endpoint: Pagkamit ng ≥2-Point Improvement sa WCSS sa 28 Araw
Multivariate Logistic Regression Derived Risk Differences, 95%CI
| Population | Paridiprubart | Placebo | P-Value |
| Lahat (n=278) | 0.52 (0.48, 0.56) | 0.45 (0.41-0.48) | <0.01 |
| IMV ITT (n=104) | 0.38 (0.31, 0.45) | 0.27 (0.21, 0.33) | <0.05 |
Adjusted risk estimate: mga variable na kasama ay edad, baseline WCSS, baseline antiviral use, baseline corticosteroid use, baseline immunomodulator use, kasabay na antiviral use, kasabay na corticosteroid use, kasabay na immunomodulator use. Safety population n=278; ITT IMV population n=104
Exploratory Analysis: Antas ng Mortality sa 28 Araw
Multivariate Logistic Regression Derived Risk Differences, 95%CI
| Population | Paridiprubart | Placebo | P-Value* |
| Non-IMV (n=174) | 0.15 (0.12, 0.18) | 0.23 (0.19, 0.26) | <0.05 |
| Pneumonia (n=108) | 0.35 (0.29, 0.41) | 0.49 (0.43, 0.55) | <0.05 |
| Acute Kidney Injury (n=48) | 0.35 (0.25, 0.44) | 0.53 (0.44, 0.62) | <0.05 |
| Sepsis (n=41) | 0.40 (0.37, 0.43) | 0.63 (0.59, 0.66) | <0.05 |
*Nominal p-value, hindi inangkop para sa multiplicity
Metodolohiya at Background
Konsistent sa orihinal na pagsusuri, lahat ng prespecified efficacy evaluations ay isinagawa sa ilalim ng parehong statistical analysis plan (SAP) gamit ang magkaparehong multivariate logistic regression model at parehong mga covariate. Tinukoy ng SAP ang hierarchical testing structure para sa adjusted 28‑day mortality para sa buong 278‑pasyenteng populasyon pati na rin sa 104‑pasyenteng IMV ITT population. Parehong pagsusuri ay prespecified at na-lock bago ang unblinding. Ang mga exploratory analysis ay isinagawa pagkatapos para sa 174 non‑IMV randomisadong kalahok, gamit ang parehong modelo at mga covariate. Karagdagang exploratory analyses ay isinagawa para sa mga pasyenteng may acute kidney injury, sepsis o pneumonia, gamit ang parehong modelo ngunit may subgroup‑appropriate covariates upang isaalang-alang ang klinikal na pagkakaiba.
Ang pag-aaral ay pinamahalaan at ang mga pagsusuri ay isinagawa ng JSS Medical Research, isang internasyonal na contract research organization.
Tungkol sa Paridiprubart
Ang Paridiprubart ay kumakatawan sa isang bagong klase ng host directed therapeutics (HDTs) na idinisenyo upang i-modulate ang sariling immune response ng katawan kapag nahaharap sa mga kilala o hindi kilalang banta sa pampublikong kalusugan tulad ng mga bagong infectious diseases pati na rin ang chemical, biological, radiological, at nuclear incidents. Mahalaga, ang HDTs ay agnostic sa causal agent at maaaring iimbak nang preemptive upang tumugon sa mga emergency sa pampublikong kalusugan at biodefense. Sa mekanismo, pinipigilan ng paridiprubart ang toll-like receptor 4 (TLR4), isang mahalagang immune signaling protein na napatunayang naa-activate ng mga virus, bacteria, injury/trauma at sa pathogenesis ng mga chronic autoimmune diseases.
Tungkol sa ARDS
Ang Acute Respiratory Distress Syndrome ay kinapapalooban ng pinalalang immune response na humahantong sa pamamaga at pinsala sa baga na pumipigil sa baga na mag-oxygenate ng dugo at sa bandang huli ay nagkukulang ng oxygen ang katawan. Para sa katamtaman hanggang malubhang kaso, kasalukuyang kakaunti ang inirerekomendang paggamot maliban sa supplemental oxygen at mechanical ventilation, at mataas ang mortality rates. Bukod sa virus-induced pneumonia, maaaring sanhi rin ng ARDS ang smoke/chemical inhalation, sepsis, chest injury, at iba pa. Ang ARDS ay bumubuo ng 10% ng intensive care unit admissions, na kumakatawan sa higit sa 3 milyong pasyente sa buong mundo bawat taon.
Tungkol sa Edesa Biotech
Ang Edesa Biotech, Inc. (Nasdaq: EDSA) ay isang clinical-stage biopharmaceutical company na nagde-develop ng mga makabagong paraan upang gamutin ang mga inflammatory at immune-related na sakit. Ang clinical pipeline nito ay nakatuon sa dalawang therapeutic areas: Medical Dermatology at Respiratory. Sa Medical Dermatology, dine-develop ng Edesa ang EB06, isang anti-CXCL10 monoclonal antibody candidate, bilang therapy para sa vitiligo, isang karaniwang autoimmune disorder na nagdudulot ng pagkawala ng kulay ng balat sa ilang bahagi. Kasama rin sa medical dermatology assets nito ang EB01 (1.0% daniluromer cream), isang Phase 3-ready asset na dinevelop bilang potensyal na therapy para sa moderate-to-severe chronic Allergic Contact Dermatitis (ACD), isang karaniwang occupational skin condition. Ang pinaka-advanced na respiratory drug candidate ng kumpanya ay ang EB05 (paridiprubart), na kasalukuyang sinusuri sa isang U.S. government-funded platform study bilang paggamot para sa Acute Respiratory Distress Syndrome, isang nakakamatay na uri ng respiratory failure. Ang EB05 program ay tumanggap ng dalawang pondo mula sa Government of Canada upang suportahan ang karagdagang pag-unlad ng asset na ito. Naghahanap din ang Edesa ng iba pang gamit para sa paridiprubart. Mag-sign up para sa balita s. Kumonekta sa amin sa X at LinkedIn.
Contact:
Gary Koppenjan
Edesa Biotech, Inc.
Disclaimer: Ang nilalaman ng artikulong ito ay sumasalamin lamang sa opinyon ng author at hindi kumakatawan sa platform sa anumang kapasidad. Ang artikulong ito ay hindi nilayon na magsilbi bilang isang sanggunian para sa paggawa ng mga desisyon sa investment.
Baka magustuhan mo rin
Kita-araw-araw mula sa Options Income: MU, SOFI, CRWV at iba pa

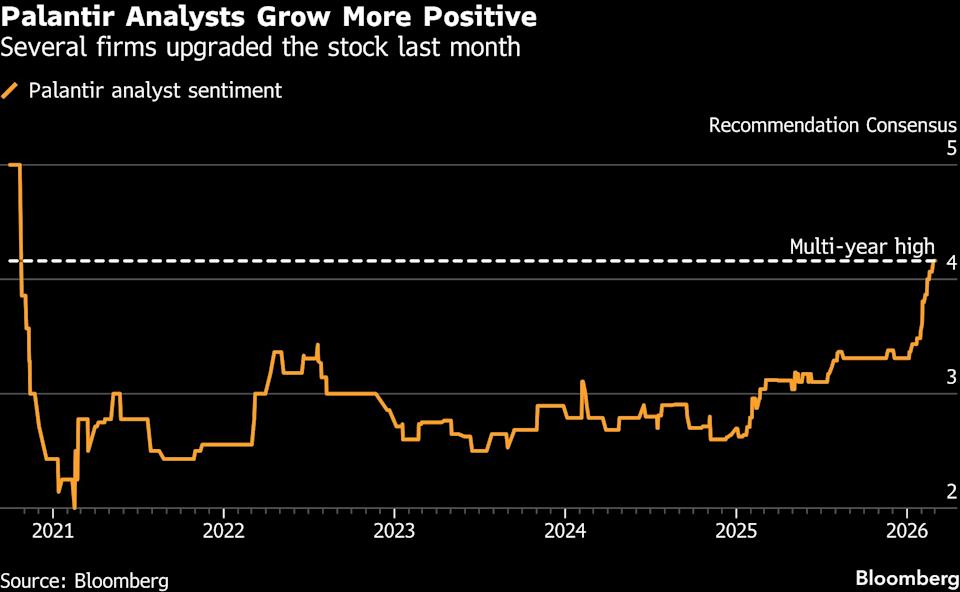
Bumalik ang Palantir sa mga Inirerekomendang Stock ng Wall Street Matapos ang 38% Pagbagsak
Nagpapalipat-lipat ang Bitcoin, Binibigyang pansin ngayon ang Crypto Derivatives
Hong Kong at Shanghai Magpapaunlad ng Blockchain Infrastructure para sa Cross-Border Trade

