BridgeBio zbliża się do 52-tygodniowego maksimum dzięki mocnym wynikom badań nad karłowatością, planuje złożenie wniosku do FDA w 2026 roku
BridgeBio Pharma Inc. (NASDAQ:BBIO) akcje gwałtownie rosną w czwartek i zbliżają się do górnej granicy 52-tygodniowego zakresu $28,33-$84,94, według danych Benzinga Pro.
Firma biofarmaceutyczna skupiająca się na schorzeniach genetycznych, opublikowała pozytywne wyniki badań PROPEL 3 fazy 3, oceniających skuteczność doustnego infigratinibu u dzieci z achondroplazją, najczęstszą postacią dysplazji szkieletowej prowadzącą do nieproporcjonalnego karłowatości kończyn.
PROPEL 3 oceniło infigratinib u dzieci z achondroplazją w wieku od 3 do 18 lat z otwartymi płytkami wzrostu.
Kluczowe Wyniki
Zmiana w stosunku do wartości wyjściowej w rocznej prędkości wzrostu (AHV) była lepsza od placebo, z LS średnią różnicą leczenia wynoszącą +1,74 cm/rok oraz średnią różnicą leczenia +2,10 cm/rok
Drugorzędowy punkt końcowy, czyli absolutna AHV w 52. tygodniu, wykazał znaczącą poprawę przy stosowaniu infigratinibu w porównaniu do placebo; grupa otrzymująca infigratinib osiągnęła najwyższą LS średnią absolutnej AHV odnotowaną do tej pory w randomizowanym badaniu nad achondroplazją (5,96 cm/rok wobec 4,22 cm/rok w placebo).
W predefiniowanej analizie eksploracyjnej (dzieci poniżej 8 roku życia; ponad 50% uczestników) kluczowego drugorzędowego punktu końcowego zmiany w stosunku do wartości początkowej proporcji górnej do dolnej części ciała w 52. tygodniu, doustny infigratinib jest pierwszą opcją terapeutyczną, która wykazała istotność statystyczną w porównaniu do placebo w randomizowanym badaniu nad achondroplazją, wykazując LS średni spadek o -0,05 względem placebo.
W całej populacji, infigratinib osiągnął LS średni spadek o -0,05, największy spadek zaobserwowany w ramieniu leczenia w randomizowanym badaniu nad achondroplazją, z korzystną LS różnicą leczenia -0,02 względem placebo w 52. tygodniu (p=0,1849)
Infigratinib był dobrze tolerowany, nie odnotowano przerwań leczenia związanych z badanym lekiem, ani poważnych zdarzeń niepożądanych związanych z badanym lekiem.
Plany Regulacyjne
BridgeBio zamierza spotkać się z organami regulacyjnymi, aby omówić plany złożenia wniosku o dopuszczenie nowego leku (NDA) oraz wniosku o pozwolenie na dopuszczenie do obrotu (MAA) dla infigratinibu w drugiej połowie 2026 roku, aby wesprzeć proces zatwierdzania.
Inne Rzadkie Wskazania
Firma zamierza również przyspieszyć rozwój infigratinibu dla hipochondroplazji, a obecnie rekrutuje uczestników do obserwacyjnej fazy wstępnej badania fazy 3.
Firma prowadzi także trwające badanie kliniczne infigratinibu u noworodków oraz dzieci w wieku do trzech lat z achondroplazją w ramach badania PROPEL Infant and Toddler.
Krajobraz Konkurencyjny
Dane pojawiają się tuż przed nadchodzącą datą docelową PDUFA, która przypada na 28 lutego, dotyczącą konkurencyjnego wniosku o dopuszczenie nowego leku (NDA) firmy Ascendis Pharma A/S (NASDAQ:ASND) dla TransCon CNP (navepegritide) dla dzieci z achondroplazją.
Voxzogo (vosoritide) firmy BioMarin Pharmaceutical Inc. (NASDAQ: BMRN) był pierwszym zatwierdzonym przez FDA lekiem (listopad 2021) na achondroplazję.
BBIO Cena Akcji: Akcje BridgeBio rosną o 6,92% do poziomu $78,41 w momencie publikacji w czwartek. W dniu publikacji akcje osiągnęły maksimum $84,94 i spadły do minimum $77,45. Według Benzinga Pro, kurs akcji znajduje się około 5,5% poniżej 52-tygodniowego maksimum.
Zdjęcie: Shutterstock
Zastrzeżenie: Treść tego artykułu odzwierciedla wyłącznie opinię autora i nie reprezentuje platformy w żadnym charakterze. Niniejszy artykuł nie ma służyć jako punkt odniesienia przy podejmowaniu decyzji inwestycyjnych.
Może Ci się również spodobać
Impasse ustawy CLARITY: exodus depozytów o wartości 500 miliardów dolarów, który niepokoi banki
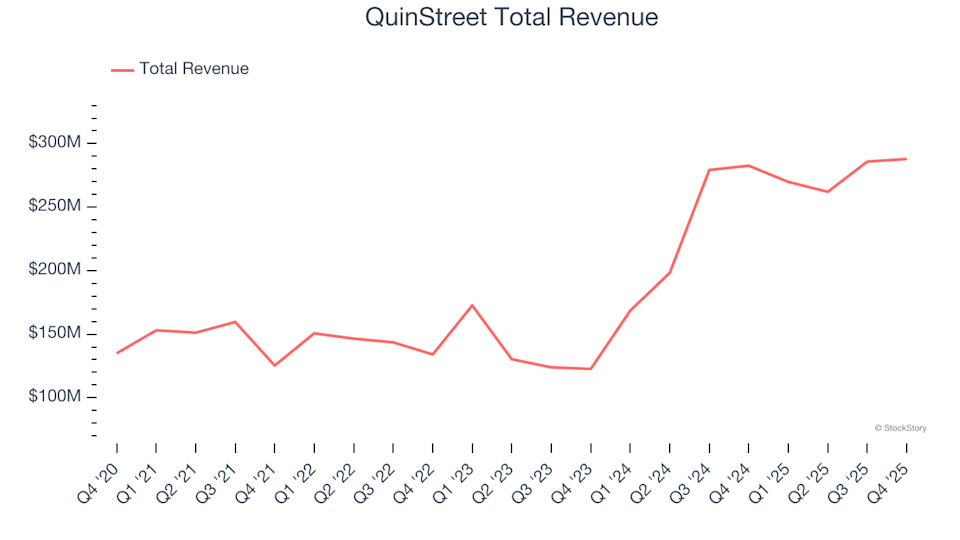
Pełna moc: Wyniki kwartalne QuinStreet (NASDAQ:QNST) nadają tempo
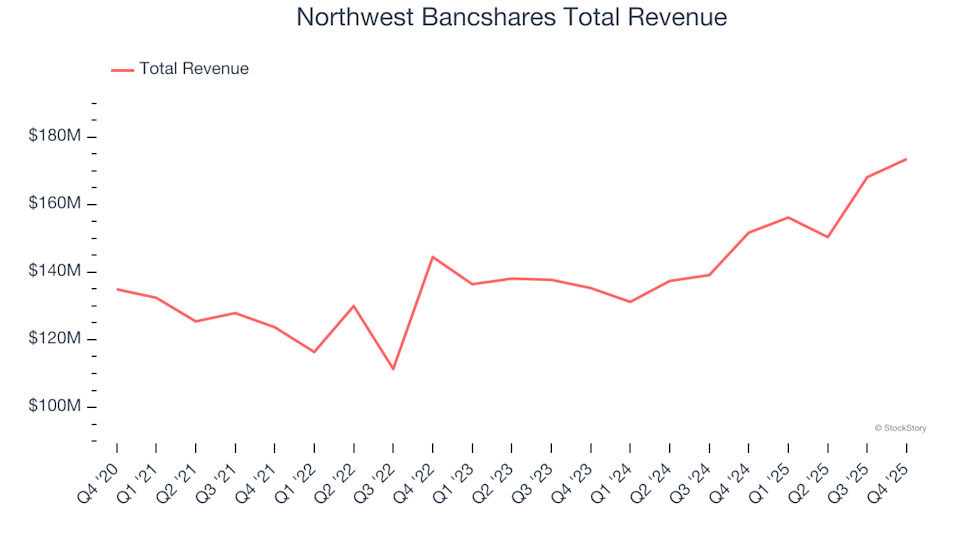
Podsumowanie Q4 akcji Thrifts & Mortgage Finance: Northwest Bancshares (NASDAQ:NWBI)