EyePoint mianuje Michaela Campbella na stanowisko Chief Commercial Officer
– Doświadczony menedżer handlowy z ponad 30-letnim doświadczeniem w kierowaniu obszarem chorób siatkówki w sektorze biotechnologicznym i dużych firmach farmaceutycznych –
– Przynosi ugruntowane doświadczenie w zakresie udanych wprowadzeń produktów na rynek oraz nadzoru nad wiodącymi franczyzami okulistycznymi, w tym Lucentis
WATERTOWN, Massachusetts, 18 lutego 2026 (GLOBE NEWSWIRE) -- EyePoint, Inc. (Nasdaq: EYPT), firma zaangażowana w rozwój i komercjalizację innowacyjnych terapii poprawiających życie pacjentów z poważnymi chorobami siatkówki, ogłosiła dziś, że Michael Campbell został mianowany Dyrektorem ds. Handlowych (Chief Commercial Officer). Pan Campbell, doświadczony lider handlowy z udokumentowanymi sukcesami we wprowadzaniu produktów na rynek oraz zarządzaniu wiodącymi franczyzami okulistycznymi, przejmie odpowiedzialność za strategię handlową EyePoint oraz przygotowanie do wprowadzenia na rynek produktu DURAVYU
„Mike jest uznanym liderem handlowym i cieszymy się, że dołącza do EyePoint w prawdziwie przełomowym momencie dla firmy” – powiedział dr Jay S. Duker, Prezes i Dyrektor Generalny EyePoint. „Mike wnosi sprawdzone doświadczenie w skutecznym wprowadzaniu innowacyjnych produktów okulistycznych, które zrewolucjonizowały leczenie chorób siatkówki, w tym przełomowe wprowadzenie Lucentis, które wyznaczyło standardy w opiece nad siatkówką. Mając na uwadze, że dane końcowe z naszego kluczowego programu fazy 3 w wet AMD spodziewane są od połowy 2026 roku, jego głęboka wiedza handlowa będzie kluczowa w przygotowaniu DURAVYU do udanego wprowadzenia na rynek USA jako potencjalnie pierwszego długo działającego inhibitora TKI na rynku. Przywództwo i doświadczenie handlowe Mike’a dodatkowo wzmacniają naszą zdolność do realizacji, skalowania i dostarczania pacjentom nowych opcji terapeutycznych.”
„Cieszę się, że mogę dołączyć do EyePoint w kluczowym momencie i być częścią firmy, która mocno współgra z moją pasją do dostarczania pacjentom innowacyjnych terapii” – powiedział Pan Campbell. „Jestem pod wrażeniem zdecentralizowanego, skoncentrowanego na pacjencie podejścia EyePoint do wdrażania programów fazy 3, w tym przemyślanych projektów badań odzwierciedlających praktykę kliniczną i mających potencjał wsparcia dla przekonującej etykiety produktu. Dzięki solidnym danym klinicznym zarówno w wet AMD, jak i DME, wielomechanizmowemu działaniu oraz jako jedyny TKI rozwijany w leczeniu DME, DURAVYU oferuje znaczny potencjał komercyjny i szansę na stanie się nowym złotym standardem leczenia chorób siatkówki. Liczę na wykorzystanie doświadczeń z wielu wprowadzeń produktów na rynek siatkówki opartych na innowacji, precyzyjnej realizacji i koncentracji na pacjencie, by pomóc EyePoint osiągnąć długoterminowy sukces.”
Pan Campbell wnosi do EyePoint ponad 30 lat doświadczenia w kierowaniu działaniami handlowymi, w których budował globalne organizacje handlowe i wprowadzał strategie skoncentrowane na pacjencie dla komercjalizacji innowacyjnych produktów okulistycznych.
Przed dołączeniem do EyePoint, pan Campbell był Dyrektorem ds. Handlowych w Opthea, gdzie budował organizację handlową i prowadził przygotowania przedpremierowe dla potencjalnego nowego produktu do leczenia wet AMD. Wcześniej pełnił funkcję Starszego Wiceprezesa i Szefa Działu Handlowego w Viatris Eye Care, gdzie kierował wprowadzeniem na rynek Tyrvaya
Pan Campbell pełnił również funkcje kierownicze w dziale handlowym w Genentech, gdzie był kluczową osobą przy wprowadzaniu na rynek Lucentis
Pan Campbell zajmował także różne stanowiska sprzedażowe i handlowe w Johnson & Johnson Vision Care, Eli Lilly oraz AstraZeneca / Medimmune. Ukończył studia licencjackie na Auburn University oraz jest absolwentem Executive Education na Wharton School of Business Uniwersytetu Pensylwanii.
Przyznanie opcji motywacyjnych zgodnie z zasadą Nasdaq Listing Rule 5635(c)(4)
W związku z zatrudnieniem pana Campbella, Komisja ds. Wynagrodzeń Rady Dyrektorów EyePoint przyznała opcje na zakup łącznie 175 000 akcji zwykłych w ramach nagrody motywacyjnej istotnej dla podjęcia przez pana Campbella pracy w Spółce zgodnie z zasadą Nasdaq Listing Rule 5635(c)(4). Opcje mają cenę wykonania równą cenie zamknięcia akcji zwykłych EyePoint z dnia 17 lutego 2026 r. i będą nabywane w następujący sposób: 25% w pierwszą rocznicę i następnie miesięcznie do czwartej rocznicy daty przyznania, zgodnie z warunkami przyznania.
O EyePoint
EyePoint, Inc. (Nasdaq: EYPT) to firma biofarmaceutyczna w fazie klinicznej, zaangażowana w rozwój i komercjalizację innowacyjnych terapii poprawiających życie pacjentów z poważnymi chorobami siatkówki. Wiodącym kandydatem na produkt firmy jest DURAVYU
Firma jest zaangażowana we współpracę ze środowiskiem specjalistów siatkówki w celu poprawy jakości życia pacjentów przy jednoczesnym tworzeniu długoterminowej wartości, z czterema zatwierdzonymi lekami w ciągu trzech dekad i dziesiątkami tysięcy leczonych oczu dzięki innowacjom EyePoint.
Siedziba EyePoint znajduje się w Watertown, Massachusetts, a zakład produkcyjny firmy zlokalizowany jest w Northbridge, Massachusetts.
Vorolanib jest licencjonowany wyłącznie dla EyePoint przez Equinox Sciences, spółkę powiązaną z Betta Pharmaceuticals, do miejscowego leczenia wszystkich chorób okulistycznych poza Chinami, Makao, Hongkongiem i Tajwanem.
DURAVYU
Oświadczenia dotyczące przyszłości
EYEPOINT – OŚWIADCZENIA BEZPIECZEŃSTWA NA MOCY PRIVATE SECURITIES LITIGATION ACT Z 1995 R.: W zakresie, w jakim jakiekolwiek oświadczenia zawarte w niniejszej informacji prasowej dotyczą informacji niehistorycznych, są to oświadczenia dotyczące przyszłości na mocy Private Securities Litigation Reform Act z 1995 r. Takie oświadczenia obejmują, lecz nie ograniczają się do, oświadczeń dotyczących naszych oczekiwań co do planów rozwoju klinicznego i regulacyjnego; naszego przekonania, że DURAVYU
Oświadczenia dotyczące przyszłości z natury dotyczą spraw, które są w różnym stopniu niepewne. Niepewności i ryzyka mogą sprawić, że rzeczywiste wyniki EyePoint będą znacząco różnić się od tych wyrażonych lub sugerowanych w oświadczeniach dotyczących przyszłości EyePoint. W przypadku EyePoint, te ryzyka i niepewności obejmują terminy, postępy i wyniki działań rozwoju klinicznego Spółki, w tym DURAVYU; niepewności i opóźnienia związane z komunikacją z Amerykańską Agencją ds. Żywności i Leków (FDA) oraz możliwość uzyskania przez FDA zgody na komercjalizację DURAVYU; nieprzewidziane koszty i wydatki; środki pieniężne i ekwiwalenty pieniężne Spółki mogą nie wystarczyć na realizację planu operacyjnego przez zakładany czas; ryzyko, że wyniki badań klinicznych mogą nie być prognostyczne dla przyszłych wyników, a dane wstępne i pośrednie podlegają dalszej analizie i mogą ulec zmianie wraz z pojawieniem się nowych danych; nieoczekiwane dane dotyczące bezpieczeństwa lub skuteczności obserwowane podczas badań klinicznych; niepewności związane z procesem autoryzacji lub zatwierdzenia regulacyjnego oraz dostępne ścieżki rozwoju i uzyskania zgody na kandydatów na produkty Spółki; zmiany w otoczeniu regulacyjnym; zakłócenia w FDA, w tym spowodowane redukcją zatrudnienia w FDA i/lub niewystarczającym finansowaniem dla FDA; zmiany w polityce handlowej USA i międzynarodowej; zmiany w oczekiwanej lub istniejącej konkurencji; sukces obecnych i przyszłych umów licencyjnych; nasza zależność od organizacji prowadzących badania kliniczne, innych zewnętrznych dostawców i usługodawców; odpowiedzialność za produkt; wpływ ogólnych warunków biznesowych i ekonomicznych; ochrona własności intelektualnej i unikanie naruszeń praw własności intelektualnej; zatrzymanie kluczowych pracowników; opóźnienia, przerwy lub niepowodzenia w produkcji i dostawach kandydatów na produkty; dostępność i potrzeba dodatkowego finansowania; nasza zdolność do uzyskania dodatkowych środków na wsparcie programów rozwoju klinicznego; niepewności dotyczące czasu i wyników wezwania z sierpnia 2022 r. ze strony Prokuratury Stanów Zjednoczonych dla Okręgu Massachusetts; niepewności dotyczące listu ostrzegawczego FDA dotyczącego zakładu produkcyjnego Spółki w Watertown, MA; oraz inne czynniki opisane w naszych dokumentach składanych do Amerykańskiej Komisji Papierów Wartościowych i Giełd. Nie możemy zagwarantować, że wyniki i inne oczekiwania wyrażone, przewidywane lub sugerowane w jakimkolwiek oświadczeniu dotyczącym przyszłości zostaną zrealizowane. Różnorodne czynniki, w tym te ryzyka, mogą spowodować, że nasze rzeczywiste wyniki i inne oczekiwania będą się znacząco różnić od przewidywanych lub innych oczekiwań wyrażonych, przewidywanych lub sugerowanych w naszych oświadczeniach dotyczących przyszłości. Jeśli znane lub nieznane ryzyka się zmaterializują, lub jeśli założenia okażą się błędne, rzeczywiste wyniki mogą się znacząco różnić od wyników z przeszłości i tych przewidywanych, szacowanych lub projektowanych w oświadczeniach dotyczących przyszłości. Należy mieć to na uwadze, rozważając jakiekolwiek oświadczenia dotyczące przyszłości. Bardziej szczegółowa dyskusja ryzyk i niepewności, które mogą spowodować, że nasze rzeczywiste wyniki będą się znacząco różnić od tych wyrażonych lub sugerowanych w oświadczeniach dotyczących przyszłości zawartych w niniejszej informacji prasowej, została opisana w sekcji "Czynniki ryzyka" w naszym najnowszym Rocznym Raporcie na formularzu 10-K, w innych naszych dokumentach składanych do Amerykańskiej Komisji Papierów Wartościowych i Giełd (SEC) oraz w przyszłych raportach składanych do SEC, które są dostępne pod adresem . Nasze oświadczenia dotyczące przyszłości dotyczą wyłącznie dat, w których zostały złożone. EyePoint nie zobowiązuje się do aktualizacji ani rewizji jakiegokolwiek oświadczenia dotyczącego przyszłości, czy to w wyniku nowych informacji, przyszłych wydarzeń, czy z innych powodów.
Zastrzeżenie: Treść tego artykułu odzwierciedla wyłącznie opinię autora i nie reprezentuje platformy w żadnym charakterze. Niniejszy artykuł nie ma służyć jako punkt odniesienia przy podejmowaniu decyzji inwestycyjnych.
Może Ci się również spodobać
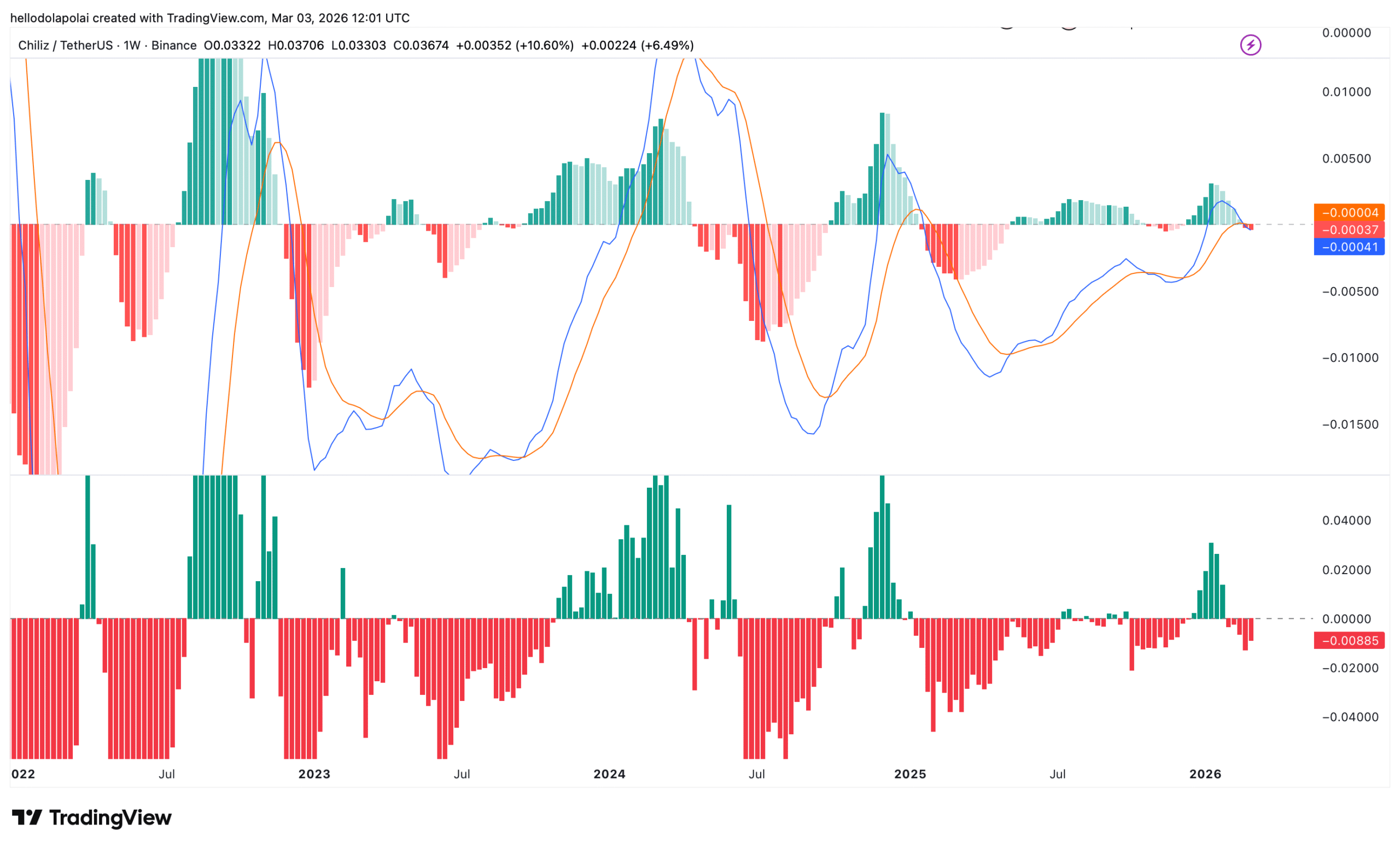
Chiliz zbliża się do kluczowego oporu: Co stoi za kruchym rajdem CHZ?
Marvell: "Kupuj na spadkach" według Cramera kontra szum wokół "utraconej transakcji"
Katalizator OFC Lumentum: strategiczny ruch wykorzystujący falę wzrostu infrastruktury AI
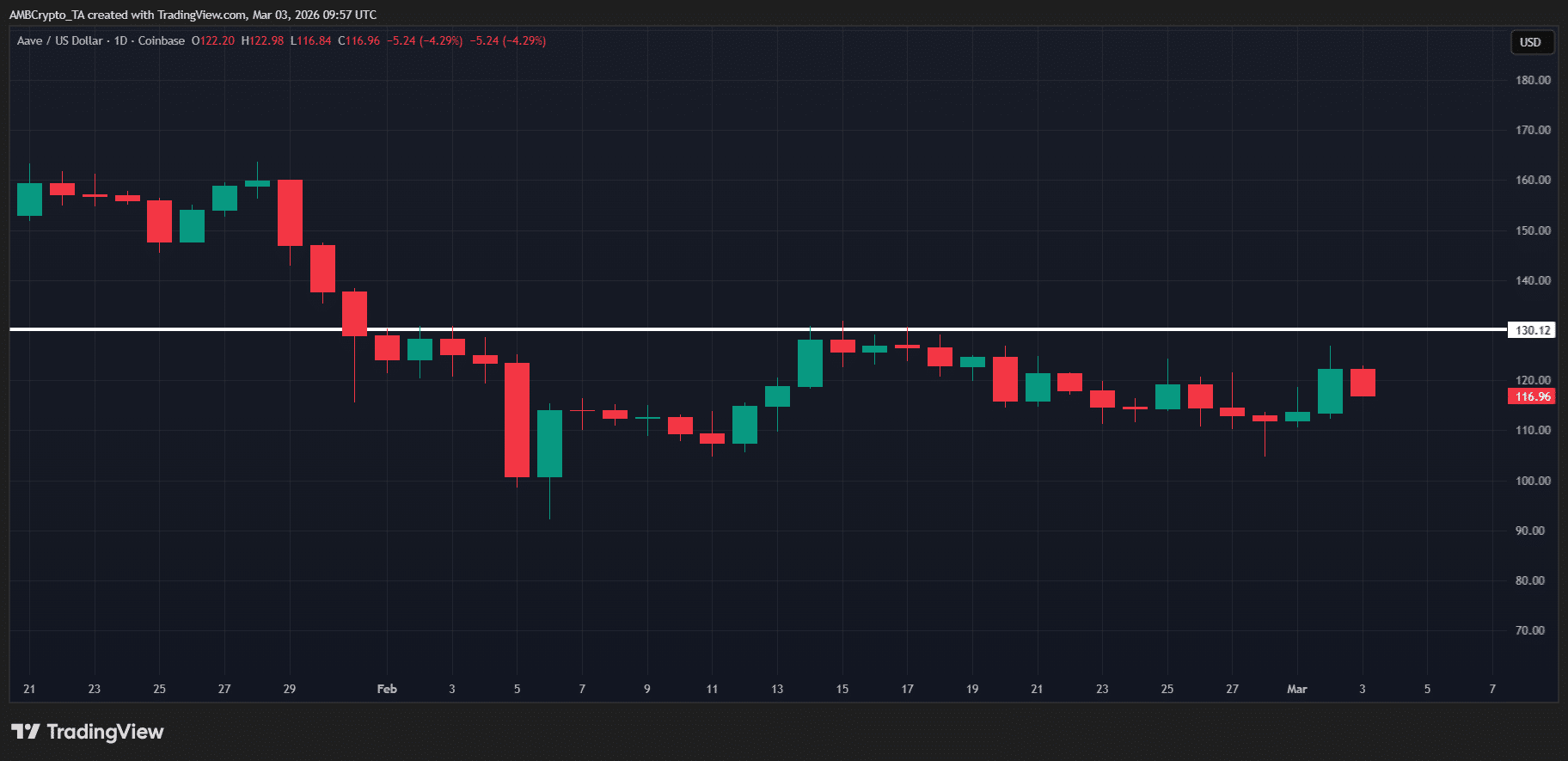
AAVE rośnie o 7% po wzmocnieniu zarządzania o wartości 42,5 mln USD – czy przebije 130 USD?