Ultragenyx ogłasza, że amerykańska FDA przyjęła do rozpatrzenia i nadała priorytetowy tryb przeglądu wniosku o licencję biologiczną (BLA) dla terapii genowej DTX401 AAV na chorobę spichrzania glikogenu typu Ia (GSDIa)
Data podjęcia decyzji PDUFA wyznaczona na 23 sierpnia 2026 r.
Jeśli zostanie zatwierdzony, DTX401 będzie pierwszą terapią adresującą pierwotną przyczynę GSDIa
NOVATO, Kalifornia, 23 lutego 2026 r. (GLOBE NEWSWIRE) -- Ultragenyx Pharmaceutical Inc. (NASDAQ: RARE) ogłosiła dziś, że Amerykańska Agencja ds. Żywności i Leków (FDA lub Agencja) przyjęła do rozpatrzenia Wniosek o Licencję Biologiczną (BLA) dotyczący zatwierdzenia terapii genowej DTX401 AAV (pariglasgene brecaparvovec) do leczenia choroby spichrzania glikogenu typu Ia (GSDIa). FDA przyznała BLA priorytetową ścieżkę rozpatrzenia i wyznaczyła datę decyzji PDUFA na 23 sierpnia 2026 r.
„Obecne podejścia dietetyczne w leczeniu GSDIa nakładają ogromne obciążenie na pacjentów i ich rodziny, przy czym nadal pozostają niezaspokojone istotne potrzeby medyczne, w tym ryzyko potencjalnie zagrażających życiu epizodów ostrej hipoglikemii oraz nagromadzenia długoterminowych powikłań przez całe życie pacjenta”, powiedział Eric Crombez, M.D., dyrektor medyczny Ultragenyx. „Jeśli DTX401 zostanie zatwierdzony, będzie to pierwsze leczenie adresujące chorobę u jej podstaw. Doceniamy szybką akceptację BLA przez FDA i będziemy nadal współpracować z Agencją w trakcie procesu przeglądu.”
BLA opiera się na danych z rygorystycznego programu rozwoju klinicznego obejmującego 52 leczonych pacjentów i do sześciu lat obserwacji. Wcześniej ogłoszone dane z randomizowanego, podwójnie zaślepionego, kontrolowanego placebo badania fazy 3 GlucoGene wykazały, że pacjenci leczeni DTX401 doświadczyli istotnych i klinicznie znaczących redukcji zarówno ilości, jak i częstości dziennego spożycia skrobi kukurydzianej, przy jednoczesnym utrzymaniu niskiego poziomu hipoglikemii, poprawie poziomów euglikemii oraz zwiększonej tolerancji na głodówkę. Te korzyści kliniczne przełożyły się na znaczną poprawę jakości życia zgłaszaną przez pacjentów, mierzoną skalą Patient Global Impression of Change (PGIC). DTX401 było dobrze tolerowane, z akceptowalnym profilem bezpieczeństwa.
Jeśli zostanie zatwierdzony, DTX401 będzie produkowany w całości w USA, w nowym zakładzie produkcji terapii genowych Ultragenyx w Bedford w stanie Massachusetts.
O DTX401 (pariglasgene brecaparvovec)
DTX401 to eksperymentalna terapia genowa AAV8 zaprojektowana w celu zapewnienia stabilnej ekspresji i aktywności G6Pazy pod kontrolą rodzimego promotora, by umożliwić komórkom wątroby reagowanie na normalne sygnały hormonalne regulujące gospodarkę glukozą, takie jak insulina i kortyzol. DTX401 jest podawany jako pojedynczy wlew dożylny i w badaniach przedklinicznych wykazano, że poprawia aktywność G6Pazy oraz zmniejsza poziom glikogenu w wątrobie, będący dobrze opisanym biomarkerem postępu choroby. DTX401 uzyskał oznaczenia: choroby rzadkiej pediatrycznej, leku sierocego, Fast Track oraz zaawansowanej terapii medycyny regeneracyjnej (RMAT) od FDA, a także oznaczenia leku sierocego oraz PRIority MEdicines (PRIME) od Europejskiej Agencji Leków.
O chorobie spichrzania glikogenu typu Ia (GSDIa)
GSDIa to rzadka, poważna i zagrażająca życiu choroba wynikająca z wrodzonego błędu metabolizmu węglowodanów spowodowanego patogennymi wariantami genu G6PC, kodującego G6Pazę, enzym kluczowy dla uwalniania glukozy z glikogenu i innych źródeł metabolicznych. Niedobór aktywności G6Pazy prowadzi do ciężkiej hipoglikemii podczas okresów głodówki między posiłkami i w nocy, a także do nadmiernego odkładania glikogenu w wątrobie, zaburzeń metabolicznych i innych powikłań związanych z chorobą. Skrobia kukurydziana odgrywa kluczową rolę w leczeniu GSDIa przez całą dobę, dostarczając zewnętrzne źródło glukozy, by unikać nagłych i poważnych spadków poziomu glukozy we krwi; jednak obecne strategie leczenia są dużym obciążeniem dla pacjentów i ich rodzin. Nie istnieją zatwierdzone terapie farmakologiczne. Szacuje się, że GSDIa dotyka około 6 000 osób w regionach o dostępie komercyjnym.
O Ultragenyx
Ultragenyx to firma biofarmaceutyczna zaangażowana w dostarczanie nowatorskich terapii pacjentom z poważnymi rzadkimi i ultrarzadkimi chorobami genetycznymi. Firma zbudowała zróżnicowane portfolio zatwierdzonych leków oraz kandydatów na terapie, ukierunkowanych na choroby o wysokim niezaspokojonym zapotrzebowaniu medycznym i jasno określonej biologii, dla których zazwyczaj nie istnieją zatwierdzone terapie leczące przyczynę choroby.
Firmą kieruje zespół zarządzający doświadczony w rozwoju i komercjalizacji terapii na choroby rzadkie. Strategia Ultragenyx opiera się na efektywnym czasowo i kosztowo rozwoju leków, z celem dostarczania bezpiecznych i skutecznych terapii pacjentom z najwyższą pilnością.
Oświadczenia dotyczące przyszłości i wykorzystania mediów cyfrowych
Z wyjątkiem informacji historycznych zawartych w niniejszym komunikacie prasowym, kwestie przedstawione w tym komunikacie, w tym oświadczenia dotyczące oczekiwań i prognoz Ultragenyx dotyczących przyszłych wyników operacyjnych i finansowych, planów biznesowych i celów dla DTX401, oczekiwań związanych z tolerancją i bezpieczeństwem DTX401, oczekiwań dotyczących adekwatności danych klinicznych do wsparcia aplikacji i zatwierdzenia marketingowego DTX401, potencjalnego harmonogramu i sukcesu aplikacji marketingowej i innych zatwierdzeń regulacyjnych dla DTX401, oczekiwań związanych z terminem uzyskania potencjalnej zgody dla DTX401, oczekiwań dotyczących liczby pacjentów DTX401, przyszłych interakcji regulacyjnych, oczekiwań co do możliwości rozwiązania z FDA uwag zawartych w liście z pełną odpowiedzią oraz wartości, którą ma generować DTX401, a także przyszłych rozwojów klinicznych i regulacyjnych dla DTX401, stanowią oświadczenia dotyczące przyszłości w rozumieniu przepisów „safe harbor” Private Securities Litigation Reform Act z 1995 roku. Takie oświadczenia dotyczące przyszłości wiążą się z istotnym ryzykiem i niepewnością, które mogą spowodować, że nasze programy rozwoju klinicznego, współpraca z podmiotami trzecimi, przyszłe wyniki, wydajność lub osiągnięcia będą się znacząco różnić od tych wyrażonych lub sugerowanych w oświadczeniach dotyczących przyszłości. Takie ryzyka i niepewności obejmują między innymi niepewność rozwoju klinicznego leków oraz nieprzewidywalność i długotrwałość procesu uzyskiwania zgód regulacyjnych, zdolność firmy do skutecznego rozwoju DTX401, możliwość osiągnięcia zakładanych celów rozwojowych w oczekiwanych ramach czasowych, ryzyka związane z działaniami niepożądanymi, ryzyka związane z poleganiem na partnerach zewnętrznych przy wykonywaniu określonych działań w imieniu firmy, ograniczone doświadczenie firmy w prowadzeniu własnego zakładu produkcyjnego, zdolność firmy i jej zewnętrznych producentów do spełnienia wymagań regulacyjnych, naszą zdolność do skutecznego zarządzania rozwojem firmy, opóźnienia lub nieoczekiwane koszty oraz inne negatywne skutki związane z niedawno ogłoszonym planem restrukturyzacji strategicznej, mniejsze niż przewidywane możliwości rynkowe dla produktów i kandydatów firmy, ryzyka produkcyjne, konkurencję ze strony innych terapii lub produktów oraz inne kwestie, które mogą wpłynąć na wystarczalność istniejącej gotówki, ekwiwalentów gotówkowych oraz krótkoterminowych inwestycji do finansowania działalności, przyszłe wyniki operacyjne i finansowe firmy, harmonogram działań w badaniach klinicznych i raportowania wyników z nich oraz dostępność lub potencjał komercyjny produktów i kandydatów Ultragenyx. Ultragenyx nie zobowiązuje się do aktualizacji ani rewizji jakichkolwiek oświadczeń dotyczących przyszłości.
Zastrzeżenie: Treść tego artykułu odzwierciedla wyłącznie opinię autora i nie reprezentuje platformy w żadnym charakterze. Niniejszy artykuł nie ma służyć jako punkt odniesienia przy podejmowaniu decyzji inwestycyjnych.
Może Ci się również spodobać
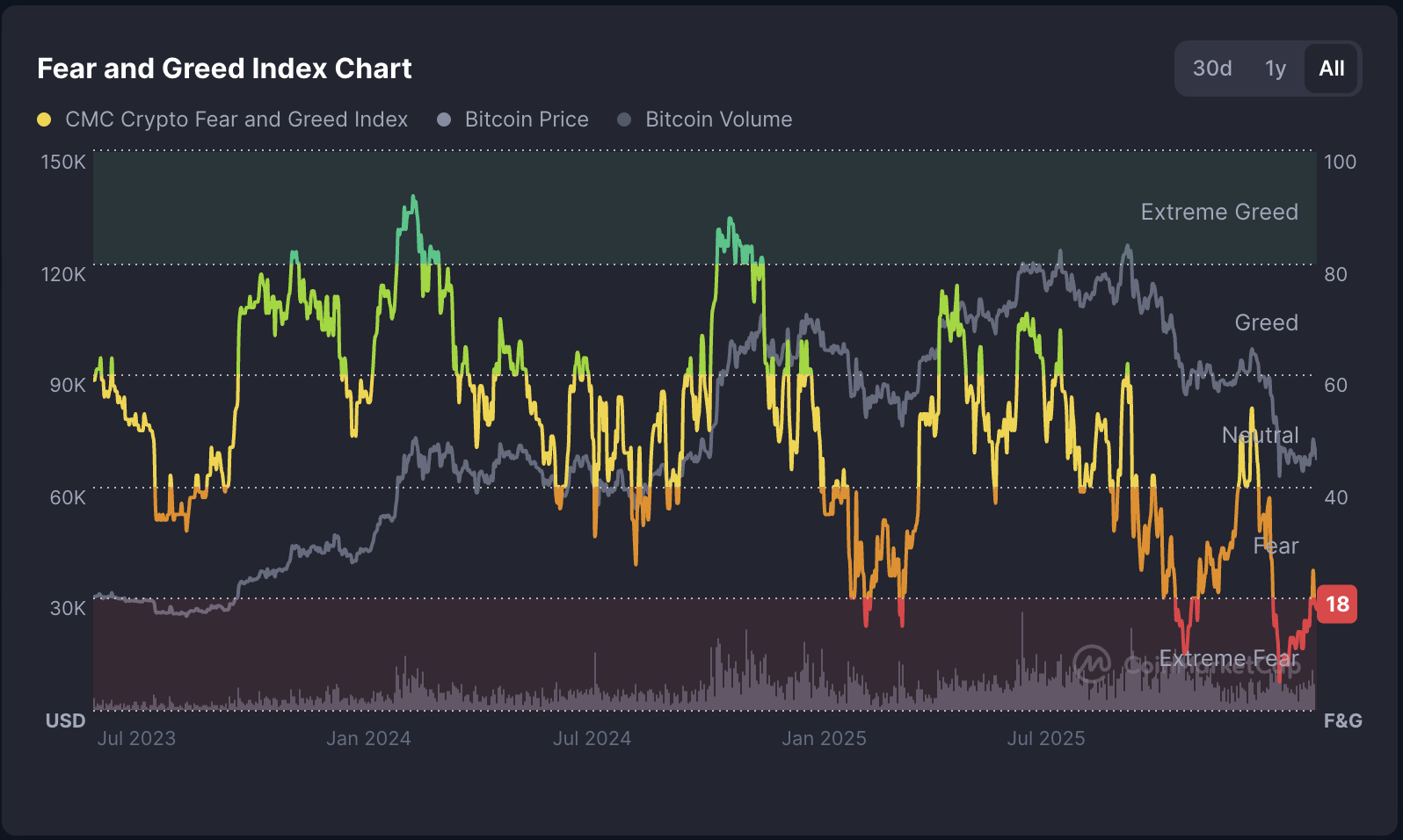
Indeks Strachu i Chciwości Kryptowalut spada z powrotem do poziomów "skrajnego strachu"
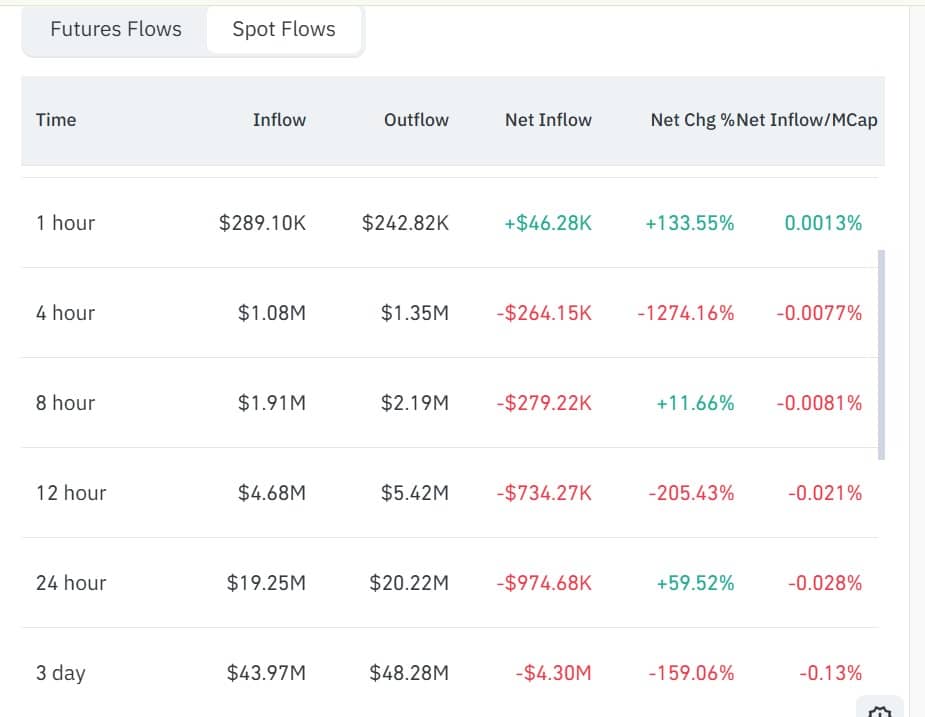
Ocena, czy wsparcie Zcash na poziomie 200 dolarów jest zagrożone po spadku ZEC o 8%
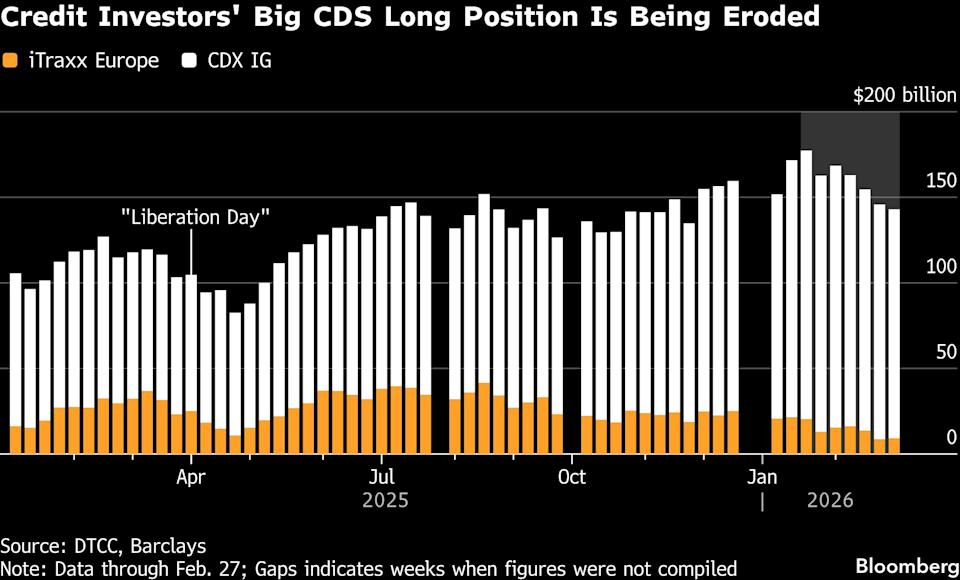
Traderzy spieszą się z nabyciem instrumentów pochodnych w obliczu rosnącego ryzyka: Tygodnik Kredytowy