Rhapsido firmy Novartis otrzymuje pozytywną rekomendację CHMP w leczeniu pokrzywki w UE
Remibrutinib firmy Novartis otrzymuje pozytywną rekomendację od panelu EMA
Novartis ogłosił, że Komitet ds. Produktów Leczniczych do Stosowania u Ludzi (CHMP), będący częścią Europejskiej Agencji Leków (EMA), wydał pozytywną opinię wspierającą zatwierdzenie remibrutinib jako terapii doustnej dla dorosłych z przewlekłą samoistną pokrzywką (CSU), którzy nie reagują odpowiednio na leki przeciwhistaminowe typu histamina-1 (H1AH). Komisja Europejska spodziewana jest podjąć ostateczną decyzję w ciągu najbliższych dwóch miesięcy.
We wrześniu 2025 roku remibrutinib, wprowadzony na rynek jako „Rhapsido”, został zatwierdzony w Stanach Zjednoczonych dla tej grupy pacjentów, stając się pierwszym doustnym inhibitorem kinazy tyrozynowej Brutona (BTKi) dopuszczonym przez FDA dla CSU. Leczenie jest również dostępne w Chinach.
Dowody kliniczne wspierające Rhapsido
Rekomendacja CHMP opiera się na wynikach badań REMIX-1 i REMIX-2 fazy III, które obejmowały pacjentów nadal doświadczających objawów pomimo stosowania leków przeciwhistaminowych drugiej generacji H1AH. Badania wykazały, że Rhapsido prowadziło do znaczących redukcji swędzenia i pokrzywki, a korzyści utrzymywały się do 52 tygodni. Ponadto, pacjenci zgłaszali poprawę jakości życia, a profil bezpieczeństwa był korzystny, bez obaw związanych ze zdrowiem wątroby.
O Rhapsido i jego szerszym potencjale
Rhapsido jest wysoko selektywnym doustnym inhibitorem BTK działającym poprzez ograniczenie uwalniania histaminy, co łagodzi objawy CSU.
Novartis bada również inne zastosowania Rhapsido. Firma niedawno przedstawiła obiecujące rezultaty fazy III badania RemIND, w którym oceniano lek w przypadku przewlekłej wywołanej pokrzywki. Trwają dalsze badania mające ocenić skuteczność w leczeniu innych schorzeń związanych z układem immunologicznym, takich jak hidradenitis suppurativa i alergie pokarmowe, poszerzając portfolio immunologiczne Novartis.
CSU to przewlekła choroba skóry charakteryzująca się nawracającą swędzącą pokrzywką i/lub obrzękiem (angioedema) bez możliwych do zidentyfikowania zewnętrznych przyczyn, dotykająca szacunkowo 40 milionów osób na całym świecie. Schorzenie może poważnie wpływać na życie pacjentów, często zakłócając sen, zwiększając poziom lęku i depresji oraz ograniczając produktywność w pracy.
Dupixent rekomendowany do rozszerzonego zastosowania w pediatrycznym CSU
Regeneron Pharmaceuticals oraz jego partner Sanofi otrzymali również pozytywną opinię od CHMP, rekomendującą rozszerzenie zastosowania ich leku Dupixent w leczeniu umiarkowanej do ciężkiej CSU u dzieci. Rekomendacja dotyczy pacjentów w wieku od 2 do 11 lat, którzy nie reagują na H1AH i nie otrzymywali wcześniej terapii anty-immunoglobuliną E. Ostateczna decyzja Komisji Europejskiej jest oczekiwana w najbliższych miesiącach.
Regeneron i Sanofi współpracują globalnie przy rozwoju oraz komercjalizacji Dupixent. Na mocy ich umowy Sanofi rejestruje światową sprzedaż netto dla Dupixent i Kevzara, podczas gdy Regeneron otrzymuje udział w zyskach lub stratach z globalnej sprzedaży.
Następna fala inwestycji w sztuczną inteligencję
Sektor sztucznej inteligencji już przyniósł znaczące bogactwo, ale najbardziej znane firmy mogą nie oferować najwyższych zwrotów w najbliższej przyszłości. Nowo powstające firmy AI, rozwiązujące ważne globalne wyzwania, mogą wkrótce zaoferować większe możliwości inwestycyjne.
Zastrzeżenie: Treść tego artykułu odzwierciedla wyłącznie opinię autora i nie reprezentuje platformy w żadnym charakterze. Niniejszy artykuł nie ma służyć jako punkt odniesienia przy podejmowaniu decyzji inwestycyjnych.
Może Ci się również spodobać
Factbox - Największe firmy farmaceutyczne ścigają się w wypuszczeniu na rynek tabletki na odchudzanie

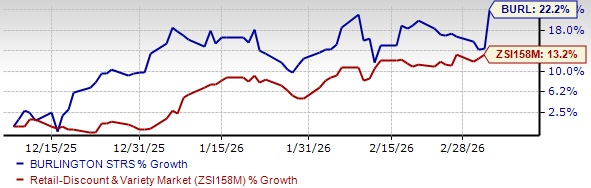
Akcje BURL rosną o 7% po wynikach za IV kwartał przewyższających oczekiwania i wzroście sprzedaży rok do roku
Gap widzi szansę na odbicie napędzaną przez warunki pogodowe po ostrym spadku o 10%
