Opus Genetics: Aprovação do sNDA de Phentolamina e a Verdadeira Disparidade nas Expectativas
Progresso da Revisão pela FDA: O Que Isso Significa para a Opus Genetics
A decisão da FDA de revisar o pedido suplementar de novo medicamento (sNDA) da Opus Genetics para a solução oftálmica de fentolamina foi um marco processual que o mercado já antecipava. Os investidores não foram pegos de surpresa, já que a empresa havia anunciado anteriormente sua intenção de protocolar o sNDA até o final de 2025, e os dados necessários do programa de Fase 3 VEGA já estavam em mãos. Ambos os estudos principais, VEGA-2 e VEGA-3, atingiram com sucesso seus objetivos primários e secundários, fornecendo evidências claras de eficácia. Esse resultado foi essencial para o pedido e provavelmente já havia sido incorporado ao preço das ações da empresa.
Essencialmente, a aceitação pela FDA foi um passo previsível no processo. O verdadeiro ponto de inflexão para a ação está por vir, com a data-alvo do PDUFA marcada para 17 de outubro de 2026. À medida que essa data se aproxima, o sentimento do mercado passará das expectativas processuais para o resultado binário de aprovação ou rejeição regulatória. Qualquer mudança na percepção da probabilidade de aprovação nessa época deve impulsionar movimentos significativos nas ações. Por enquanto, a aceitação da FDA apenas prepara o terreno para uma decisão regulatória mais importante que está por vir.
Perspectiva Financeira: Equilibrando Preocupações com Diluição e Reservas de Caixa
As classificações atuais dos analistas e os preços-alvo para a Opus Genetics (+5,51%) não são o principal foco. A questão crítica é se a empresa possui recursos financeiros suficientes para alcançar a aprovação sem recorrer a mais diluição de ações. A recente captação de recursos desempenha um papel central nessa avaliação.
Em novembro, a Opus Genetics garantiu aproximadamente US$ 23 milhões por meio de uma oferta direta registrada liderada pela Perceptive Advisors e Balyasny Asset Management. Esses fundos são destinados ao avanço dos programas clínicos de terapia gênica LCA5 e BEST-1, incluindo o próximo estudo de Fase 3 para OPGx-LCA5. Além disso, a empresa obteve financiamento não dilutivo de organizações de defesa dos pacientes, fortalecendo ainda mais sua posição financeira.
Com esses recursos combinados, a Opus Genetics projeta que suas reservas de caixa sustentarão as operações até a segunda metade de 2027, com base nos planos atuais e receitas antecipadas. Esse cronograma vai muito além da data do PDUFA em outubro de 2026 para o sNDA de fentolamina, o que deve aliviar preocupações imediatas sobre falta de caixa.
Apesar disso, o mercado permanece sensível ao risco de mais diluição. A empresa tem um histórico de captação de recursos para financiar seu pipeline, e qualquer indicação de necessidade adicional de capital — especialmente antes da decisão da FDA — pode ser vista negativamente. Os investidores acompanharão de perto se os fundos atuais são suficientes e se o processo regulatório segue conforme o planejado. A recente captação oferece uma margem de segurança, mas também aumenta as expectativas de uso eficiente dos recursos e mínima dependência de futuras ofertas de ações que possam pressionar o preço dos papéis.
Oportunidade de Mercado e Concorrência: Navegando em um Espaço Grande e Concorrido
O potencial comercial da fentolamina é sustentado por uma vasta população de pacientes. A presbiopia afeta cerca de 90% dos adultos dos EUA com mais de 45 anos, representando aproximadamente 128 milhões de pessoas. Essa realidade demográfica define a escala do mercado, mas a verdadeira oportunidade está em capturar uma parcela daqueles que atualmente usam métodos de correção estabelecidos.
Hoje, o mercado de presbiopia é dominado por soluções não medicamentosas, como óculos de leitura, lentes multifocais, lentes de contato e procedimentos cirúrgicos como a cirurgia de catarata. Essas opções são bem estabelecidas e facilmente acessíveis. A fentolamina busca se diferenciar como uma alternativa farmacológica de uso diário, não invasiva, que atua relaxando o músculo dilatador da íris, melhorando a visão de perto sem afetar o músculo ciliar. Esse mecanismo único pode atrair pacientes que procuram uma solução medicamentosa em vez de cirurgia ou óculos.
No entanto, a concorrência está se intensificando. Embora a abordagem da fentolamina ofereça vantagens, ela não garante exclusividade de mercado. Outras empresas também estão desenvolvendo tratamentos para presbiopia, tornando o cenário competitivo cada vez mais disputado. Apesar do tamanho do mercado, o principal desafio será convencer os pacientes a abandonarem hábitos antigos, como o uso de óculos de leitura. Em última análise, o sucesso comercial dependerá da eficácia no mundo real, segurança e aceitação dos pacientes — fatores que ainda precisam ser demonstrados.
Por ora, o mercado está focado na decisão regulatória que se aproxima. O tamanho da oportunidade e o ambiente competitivo fornecem contexto importante, mas o veredito da FDA em outubro será o catalisador imediato para reavaliar as perspectivas comerciais do medicamento.
Eventos-Chave à Frente: O Que os Investidores Devem Monitorar
As perspectivas de curto prazo da Opus Genetics são definidas por vários marcos críticos. A jornada da aceitação pela FDA até uma possível aprovação de mercado gira em torno de três eventos principais que podem reforçar a trajetória positiva da empresa ou revelar novos riscos.
- Apresentação na ASCRS em abril de 2026: O primeiro evento significativo é a apresentação dos dados do VEGA-3 na reunião da ASCRS. Este destaque pré-PDUFA oferece a oportunidade de exibir o perfil completo de eficácia e segurança para um público especializado. Feedback positivo pode aumentar a confiança nas chances de aprovação, enquanto preocupações levantadas podem esfriar o entusiasmo.
- Decisão do PDUFA – 17 de outubro de 2026: O momento mais crucial será a decisão da FDA sobre o sNDA. A aprovação validaria os dados clínicos e abriria as portas para um grande mercado, provavelmente resultando em uma reavaliação significativa das ações. Por outro lado, uma rejeição exigiria uma grande reavaliação do futuro do medicamento e da estratégia da empresa.
- Atualizações de Comercialização da Viatris: A Viatris detém direitos exclusivos de comercialização nos EUA para a solução oftálmica de fentolamina 0,75%. Qualquer novidade sobre prontidão de lançamento, preços ou planos de distribuição será acompanhada de perto. Mudanças na parceria ou no nível de comprometimento da Viatris podem impactar o acesso ao mercado e as perspectivas comerciais do medicamento.
Em resumo, os próximos grandes movimentos da Opus Genetics serão moldados por esses eventos. A apresentação dos dados em abril prepara o terreno, a decisão da FDA em outubro é o momento definidor e a execução da Viatris determinará a transição da aprovação para o sucesso comercial.
Aviso Legal: o conteúdo deste artigo reflete exclusivamente a opinião do autor e não representa a plataforma. Este artigo não deve servir como referência para a tomada de decisões de investimento.
Talvez também goste
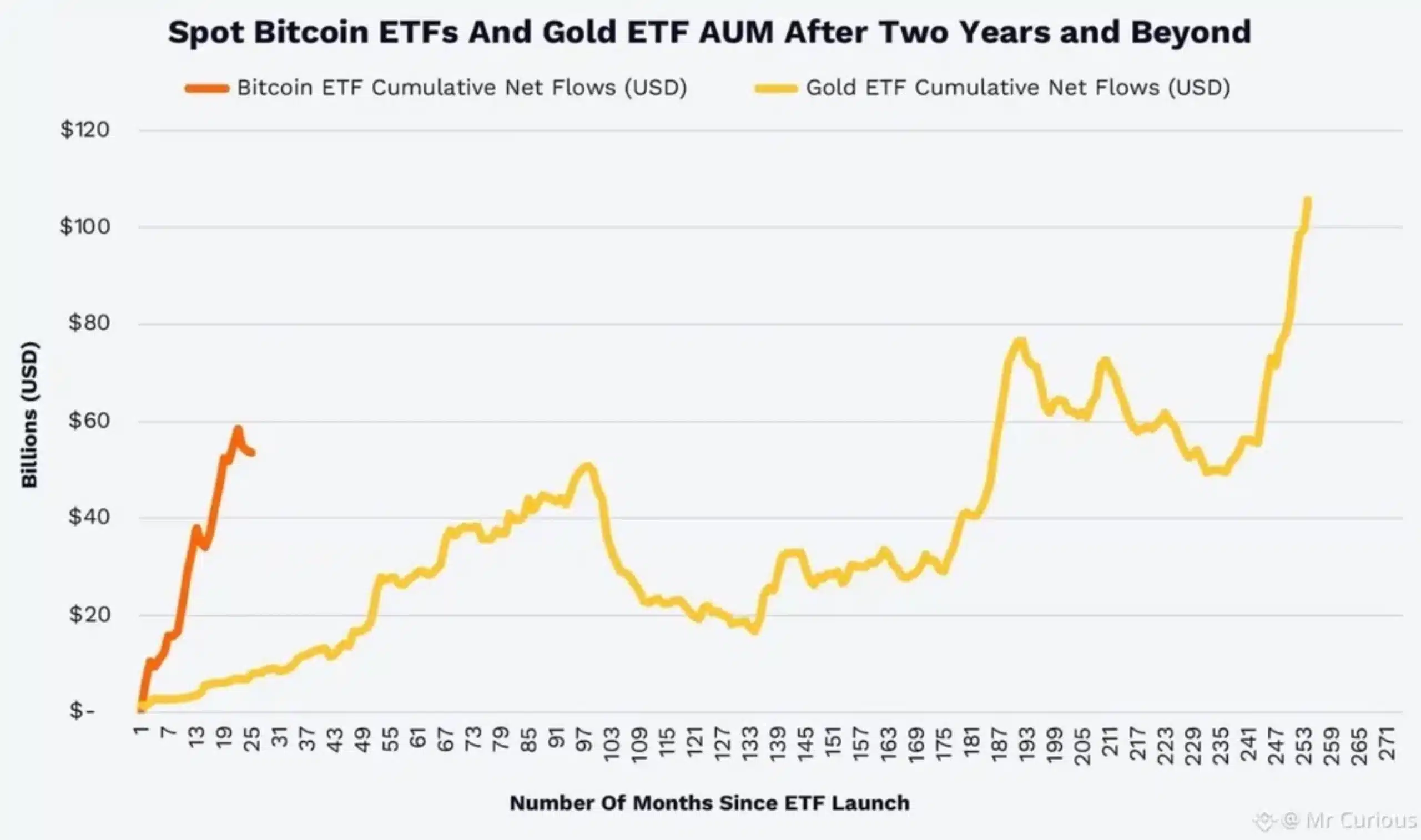
Bitcoin cai 21%, ouro sobe 79% – então por que os investidores ainda apostam em bitcoin?
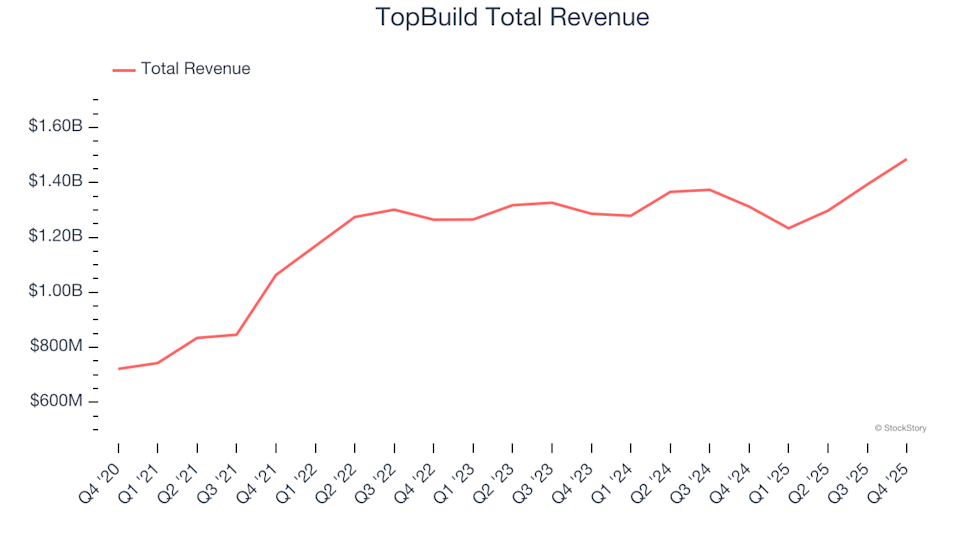
Refletindo sobre os resultados do quarto trimestre das ações de construção civil: TopBuild (NYSE:BLD)