Dare Bioscience объявляет о получении разрешения FDA на проведение клинического исследования фазы 2 препарата DARE-HPV — потенциального средства для лечения персистирующей высокорисковой инфекции HPV, самой распространённой причины рака шейки матки
Разработка DARE-HPV поддерживается контрактом ARPA-H на сумму 10 миллионов долларов; программа направлена на решение важной неудовлетворенной медицинской потребности в отсутствии одобренных FDA методов терапии
САН-ДИЕГО, 23 февраля 2026 г. (GLOBE NEWSWIRE) -- Daré Bioscience, Inc. (NASDAQ: DARE), биотехнологическая компания, ориентированная на здравоохранение и ставящая своей целью устранение разрыва между многообещающими научными достижениями и реальными решениями в области женского здоровья, сегодня объявила, что Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США (FDA) одобрило заявку компании на проведение клинических исследований нового препарата (IND) для DARE-HPV — экспериментальной, запатентованной фиксированной дозированной формы лопинавира и ритонавира в виде вагинальной капсулы с мягким гелем, что позволяет начать запланированное клиническое исследование II фазы для оценки DARE-HPV как потенциального лечения персистирующей высокоонкогенной инфекции вируса папилломы человека (HPV).
DARE-HPV разрабатывается как нехирургическая, локальная, самоприменяемая терапия, предназначенная для устранения персистирующей высокоонкогенной инфекции HPV. Инфекция HPV является основной причиной 99% случаев рака шейки матки в США. В настоящее время не существует одобренных FDA фармакологических методов лечения инфекции HPV.
Благодаря тому, что DARE-HPV направлен непосредственно на сам вирус, а не на ожидание развития клеточных изменений, препарат имеет потенциал изменить парадигму лечения и профилактики заболеваний шейки матки.
HPV — одна из самых распространённых вирусных инфекций, передающихся половым путем, во всем мире. Только в США, по оценкам, более 11 миллионов женщин ежегодно заражаются новой инфекцией HPV. Хотя большинство инфекций HPV проходят самостоятельно, миллионы женщин сталкиваются с персистирующей высокоонкогенной инфекцией HPV — именно этот тип инфекции может привести к развитию предраковых поражений шейки матки и, в конечном итоге, к раку шейки матки, если не проводить лечение. По данным Центров по контролю и профилактике заболеваний, высокоонкогенные типы HPV ответственны практически за все случаи рака шейки матки в США.
Сегодняшний стандарт лечения не направлен на устранение вируса. Вместо этого женщины с персистирующей высокоонкогенной инфекцией HPV наблюдаются посредством повторных скринингов. Вмешательство, как правило, проводится только после развития предраковых изменений, зачастую требуя хирургических процедур, таких как иссечение или абляция тканей шейки матки. Эти процедуры могут увеличить риск преждевременных родов в будущих беременностях и негативно сказаться на фертильности — что создает значительную физическую и эмоциональную нагрузку для женщин.
«Одобрение FDA перехода к II фазе является важной регуляторной вехой для DARE-HPV и для женщин, которые в настоящее время не имеют вариантов лечения персистирующей высокоонкогенной инфекции HPV», — сказала Сабрина Джонсон, президент и генеральный директор Daré Bioscience. — «На протяжении десятилетий женщинам говорили “наблюдать и ждать”, чтобы увидеть, устранится ли вирус самостоятельно. Если этого не происходит, единственным вариантом остается операция после появления предраковых изменений. DARE-HPV создан для более раннего вмешательства — воздействия непосредственно на вирус до развития заболеваний шейки матки, с целью сократить частые и обременительные визиты к врачу, которые сопряжены с высокими затратами и способствуют социально-экономическим и расовым различиям в заболеваемости раком шейки матки».
В ходе запланированного исследования II фазы планируется оценить безопасность и противовирусную активность DARE-HPV у женщин с персистирующей высокоонкогенной инфекцией HPV. Программа, включая запланированное клиническое исследование II фазы, поддерживается контрактом на сумму 10 миллионов долларов, финансируемым Advanced Research Projects Agency for Health (ARPA-H), частью Министерства здравоохранения и социальных служб США, из которых 6,5 миллионов долларов уже получено на сегодняшний день.
Персистирующая высокоонкогенная инфекция HPV представляет собой значительную неудовлетворенную медицинскую потребность:
- Высокоонкогенные типы HPV вызывают практически все случаи рака шейки матки
- Не существует одобренных FDA фармакологических методов лечения высокоонкогенной инфекции HPV
- Текущие стратегии вмешательства основаны на хирургическом удалении аномальных тканей шейки матки
- Хирургические процедуры связаны с повышенным риском преждевременных родов и возможным влиянием на фертильность
«Эта программа отражает нашу приверженность продвижению научных решений там, где у женщин исторически было мало или совсем не было вариантов терапии», — добавила Джонсон. — «Благодаря поддержке ARPA-H и одобрению FDA мы готовы эффективно продвинуть DARE-HPV во II фазу и получить клинические данные, которые могут значительно изменить подход к лечению персистирующей высокоонкогенной инфекции HPV».
Daré Bioscience предоставит дополнительные детали относительно дизайна исследования II фазы и ожидаемых сроков его начала, которое компания планирует на 2026 год, в ближайшие месяцы.
О компании Daré Bioscience
Daré Bioscience — это биотехнологическая компания, ориентированная на здравоохранение и сосредоточенная исключительно на устранении разрыва между многообещающими научными достижениями и реальными решениями в области женского здоровья. Каждое нововведение Daré основывается на передовой науке и подтверждено строгими, рецензируемыми исследованиями. От контрацепции до менопаузы, от тазовой боли до фертильности, от вагинального здоровья до инфекционных заболеваний — Daré работает над устранением критических пробелов в уходе, используя науку, которая отвечает потребностям женщин.
Десятилетиями женщинам говорили “подождать” или “привыкнуть к этому”, в то время как инновации, способные улучшить качество их жизни, застревали на этапах регулирования или финансирования. С ростом осведомленности о менопаузе, сексуальном и вагинальном здоровье, дискуссия меняется. Однако доступ к реальным, основанным на доказательствах решениям по-прежнему отстает. Daré была основана для того, чтобы изменить эту ситуацию. Как компания, руководимая женщинами, Daré ускоряет разработку надежных, научно обоснованных решений, отвечающих высоким стандартам клинической строгости — рандомизированным контролируемым исследованиям, валидированным конечным точкам, публикациям в рецензируемых журналах и требованиям надлежащей производственной практики (cGMP).
Руководство Daré Bioscience включено в список Power List журнала Medicine Maker и Women in Biopharma издания Endpoints News, а генеральный директор Daré была отмечена как одна из самых влиятельных людей в биофарме по версии Fierce Pharma за вклад компании в инновации и защиту интересов женщин в области здравоохранения.
Daré может публиковать существенную информацию о своих финансах, продуктах и кандидатах в продукты, клинических исследованиях и других вопросах, используя раздел для инвесторов на своем сайте, отчеты в SEC, пресс-релизы, общедоступные телеконференции и веб-трансляции. Daré будет использовать эти каналы для распространения существенной информации о компании, а также может использовать социальные сети для передачи важной информации о компании, ее финансах, продуктах и кандидатах в продукты, клинических исследованиях и других вопросах. Информация, размещаемая Daré на сайте для инвесторов или через каналы социальных сетей, может считаться существенной. Daré призывает инвесторов, СМИ и всех заинтересованных лиц следить за обновлениями в разделе для инвесторов на сайте компании. Любые обновления списка социальных сетей, которые компания может использовать для публикации информации, будут размещаться в разделе для инвесторов на сайте Daré.
Источник: Daré Bioscience, Inc.
Дисклеймер: содержание этой статьи отражает исключительно мнение автора и не представляет платформу в каком-либо качестве. Данная статья не должна являться ориентиром при принятии инвестиционных решений.
Вам также может понравиться
План Трампа в области кибербезопасности теперь поддерживает Bitcoin и безопасность blockchain
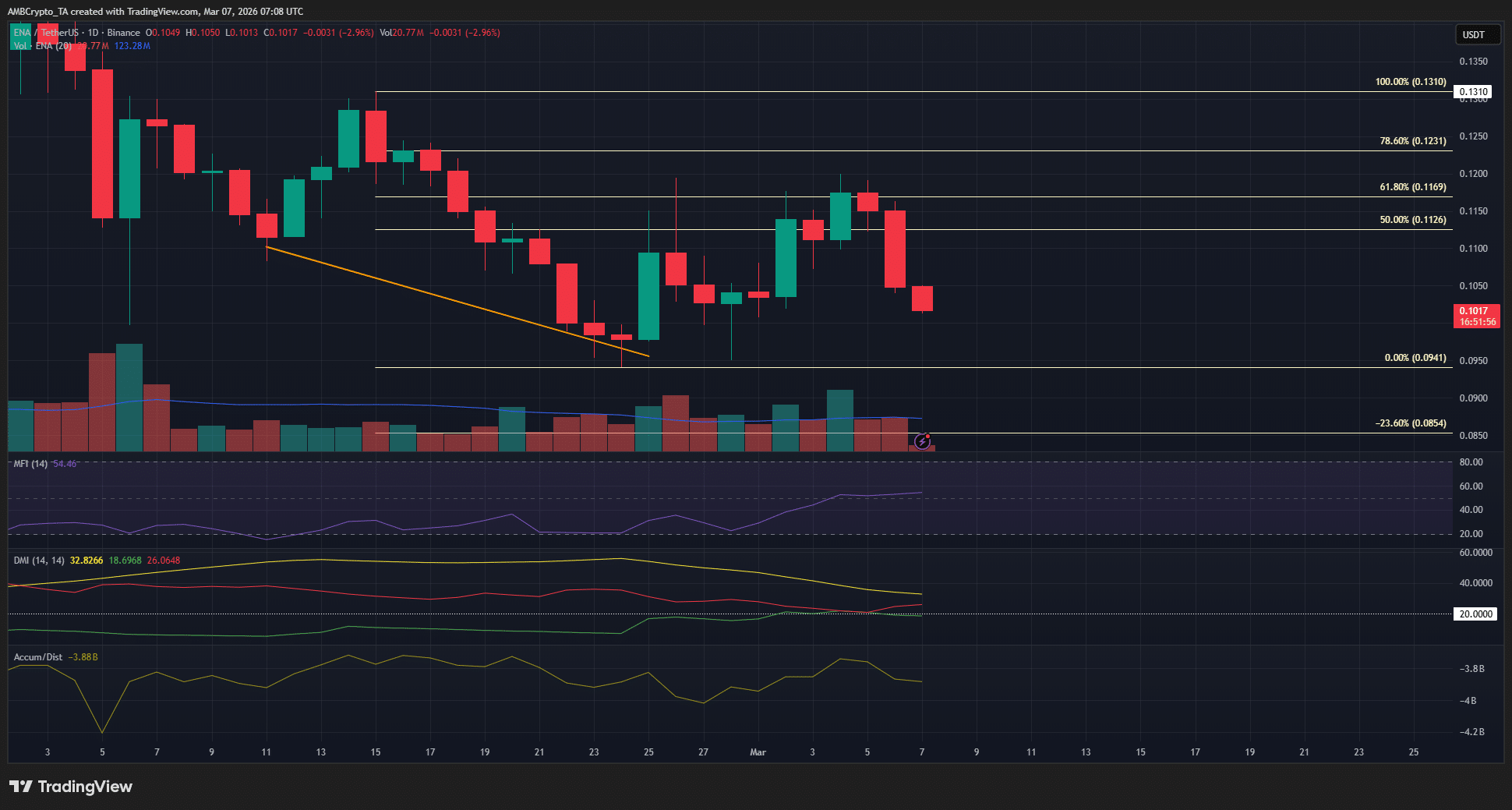
Цена Ethena снизилась на 15% от недельного максимума — впереди более глубокие потери?

Всплеск цен на энергоносители, вызванный конфликтом с Ираном, выявил уязвимости Европы


