Kyntra Bio宣佈FG-3246聯合Enzalutamide用於轉移性去勢抗性前列腺癌患者的研究者主導1b/2期臨床試驗獲得積極數據,將於ASCO GU 2026發表
- FG-3246 與 enzalutamide 聯合療法在未經生物標誌物篩選、接受過雄激素受體通路抑制劑(ARPI)治療但未接受過紫杉烷類藥物治療的轉移性去勢抗性前列腺癌(mCRPC)患者中,在整體研究隊列中達到中位放射學無進展生存期(rPFS)7.0 個月,僅接受過一次 ARPI 治療且病情進展的患者中觀察到中位 rPFS 為 10.1 個月
- FG-3180(CD46 靶向 PET 影像劑)在腫瘤的攝取量較高者,PSA50 應答率的機會也呈現上升趨勢,顯示其在患者篩選中的潛力
- 聯合療法的安全性與暴露特徵與先前 FG-3246 第一階段單藥治療試驗相似
- 結果進一步驗證了 FG-3246 第二階段單藥治療設計的關鍵要素,最重要的是納入僅接受過一次 ARPI 並出現病情進展的患者,以及所有入組患者均整合基線 FG-3180 PET
- FG-3246 第二階段單藥治療試驗預計於 2026 年下半年進行期中分析
舊金山,2026 年 2 月 23 日(GLOBE NEWSWIRE)——Kyntra Bio(Nasdaq: KYNB,前身為 FibroGen,Nasdaq: FGEN)今日宣布,FG-3246 聯合 enzalutamide 用於治療轉移性去勢抗性前列腺癌(mCRPC)患者的抗腫瘤活性數據,來自研究者發起的第一階段 b/第二階段臨床試驗,將在 2026 年美國臨床腫瘤學會泌尿生殖系腫瘤研討會(ASCO GU)上發表,該會議將於 2026 年 2 月 26-28 日在加州舊金山舉行。
「這項第一階段 b/第二階段研究者主導的試驗結果顯示,FG-3246 聯合 enzalutamide 在 mCRPC 患者中展現出令人鼓舞的初步抗腫瘤活性。值得注意的是,僅接受過一次 ARPI 的患者中位 rPFS 達 10.1 個月,突顯 FG-3246 在早期治療線中的潛力,」舊金山加州大學醫學院教授、該研究首席研究員 Rahul Aggarwal 醫師表示。「腫瘤對 FG-3180(CD46 靶向 PET)攝取與 PSA50 應答之間的積極關聯趨勢,儘管患者數量有限,尤其值得關注,我很期待在第二階段單藥治療試驗中進一步探索這一生物標誌物的潛在應用。」
「這項研究者發起的試驗數據,進一步擴展了先前 FG-3246 在臨床上取得的有意義成果,」Kyntra Bio 執行長 Thane Wettig 表示。「在僅接受過一次 ARPI 治療且病情進展的患者中觀察到的 10.1 個月中位 rPFS,以及採用預防性 G-CSF 緩解中性球減少相關不良事件,這些都進一步驗證了我們第二階段單藥治療試驗的設計。我們期待在 2026 年下半年分享第二階段單藥治療試驗的期中分析,並進一步確認 FG-3180 作為患者篩選生物標誌物的潛力。」
本次發表包含 44 名未經生物標誌物篩選、病情進展的轉移性去勢抗性前列腺癌患者數據,其中 17 名參與了第一階段 b 劑量遞增部分。試驗納入標準包括至少接受過一次 ARPI 且病情進展的患者,曾在去勢抗性階段接受化療的患者被排除。超過 60% 患者曾接受過兩次或以上 ARPI,包括先前的 enzalutamide 治療。劑量遞增階段的主要終點為評估劑量限制性毒性反應(DLT)及確定最大耐受劑量和第二階段建議劑量——最終確定為 FG-3246 2.1 mg/kg 與 enzalutamide 160 mg/天。第二階段擴展部分的主要終點為複合應答率(PSA50 應答和/或依據 RECIST v1.1 的客觀應答)。次要終點包括 PSA50 應答率、客觀應答率、放射學無進展生存期(rPFS)、總生存期及治療相關不良事件(TRAEs)。
FG-3246 聯合 enzalutamide 展現抗腫瘤活性,在整體隊列中複合應答率為 21%,而在僅接受過一次 ARPI 的患者中複合應答率為 40%。整體隊列中中位 rPFS 為 7.0 個月。值得注意的是,在僅接受過一次 ARPI 並進展的患者中觀察到中位 rPFS 為 10.1 個月,這一結果在不同先前 ARPI 治療組間一致。此外,FG-3180 腫瘤攝取量較高者,PSA50 應答機率呈現上升趨勢(p=0.053),突顯 FG-3180 作為患者篩選生物標誌物的潛力。
FG-3246 與 enzalutamide 聯合治療的安全性與先前 FG-3246 第一階段單藥治療試驗相似。使用 G-CSF 預防性治療可有效降低中性球減少風險。聯合療法最常見的治療相關不良事件包括疲勞、周邊神經病變、食慾下降及味覺障礙。累積性毒性,包括周邊神經病變,導致部分患者停藥。
本次海報發表題為「FOR46(FG-3246)聯合 enzalutamide(enza)治療轉移性去勢抗性前列腺癌(mCRPC)患者的第一階段 b/第二階段試驗」,預計於 2026 年 2 月 26 日上午 11:30 至 12:45(太平洋時間)海報展示環節進行。
FG-3246 目前正於第二階段單藥治療試驗中接受評估,期中數據預計於 2026 年下半年公佈。該試驗同時納入 FG-3180(CD46 靶向 PET 影像劑)治療,將檢測 CD46 陽性病灶的表達水平。這將進一步評估 CD46 表達與 FG-3246 治療反應的相關性,以及 FG-3180 作為患者篩選生物標誌物的潛力,以支持未來 FG-3246 臨床試驗的患者選擇。
關於 FG-3246 與 FG-3180
FG-3246(FOR46)是一種潛在的同類首創全人源抗體藥物複合體(ADC),獨家授權自 Fortis Therapeutics,由 Kyntra Bio 開發,適應症為轉移性去勢抗性前列腺癌及潛在其他腫瘤類型。FG-3246 可結合 CD46 的一個表位,這是一種細胞受體靶點,抗體結合後誘導細胞內吞,在前列腺癌及其他腫瘤類型中表達量高,而在大多數正常組織中表達極低。FG-3246 由抗 CD46 抗體 YS5 與抗有絲分裂藥物 MMAE(經臨床和商業驗證的 ADC 載體)連結組成。FG-3246 已於臨床前及臨床研究中展現抗腫瘤活性。FG-3180 是一種配套診斷用 PET 影像劑,採用相同 CD46 靶向抗體及一個
關於 FG-3246 聯合 Enzalutamide 的第一階段 b/第二階段試驗
本第一階段 b/第二階段試驗由研究者發起,在舊金山加州大學進行,評估 FG-3246(FOR46)聯合 enzalutamide 治療在至少接受過一次雄激素受體通路抑制劑治療後進展的轉移性去勢抗性前列腺癌(mCRPC)患者中的效果。第一階段 b 研究的主要目標是確定 FG-3246 聯合 enzalutamide 的最大耐受劑量(MTD)及第二階段建議劑量。第二階段研究目標為確定複合應答率(CRR)、PSA 降低 50% 或以上的患者比例(PSA50)、客觀應答率(ORR)、中位應答持續時間、中位放射學無進展生存期(rPFS)及中位總生存期(OS)。
關於 Kyntra Bio
Kyntra Bio 是一家專注於腫瘤及罕見疾病新療法開發的生物製藥公司。Roxadustat(愛瑞卓
免責聲明:文章中的所有內容僅代表作者的觀點,與本平台無關。用戶不應以本文作為投資決策的參考。
您也可能喜歡
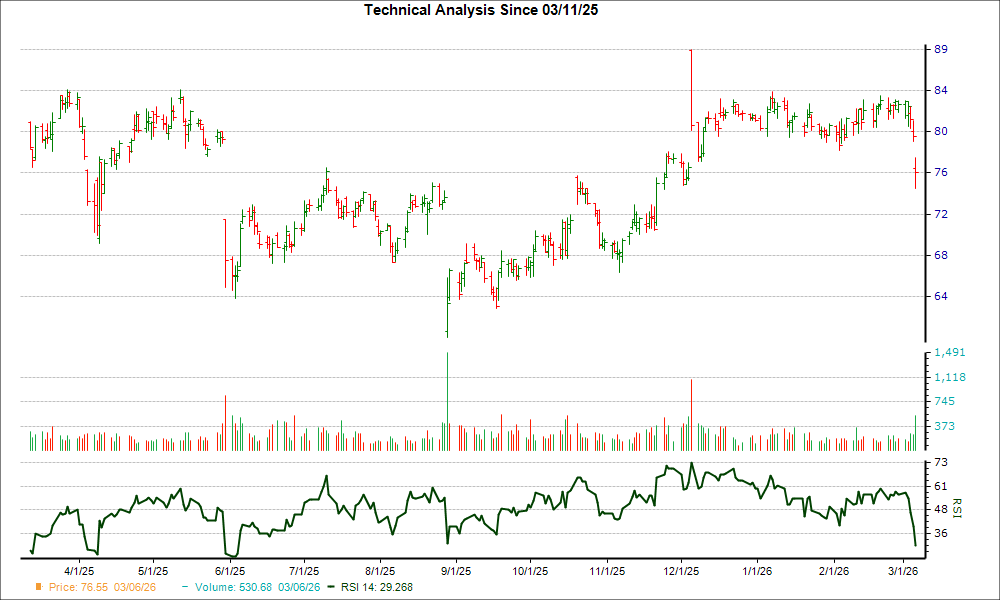
Ferguson plc(FERG)過去一個月下跌13.6%——潛在的反轉或許正在接近
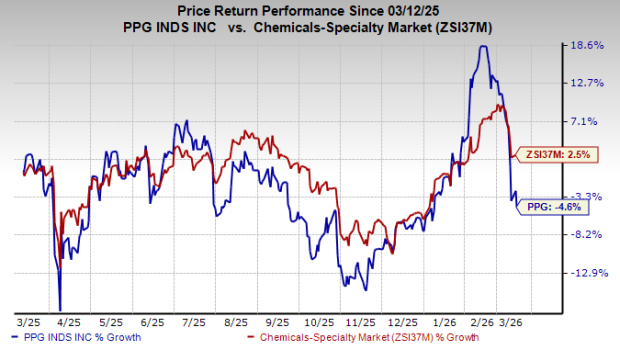
PPG Aquacron WSP 亮相,展現卓越的固化表現與環保責任
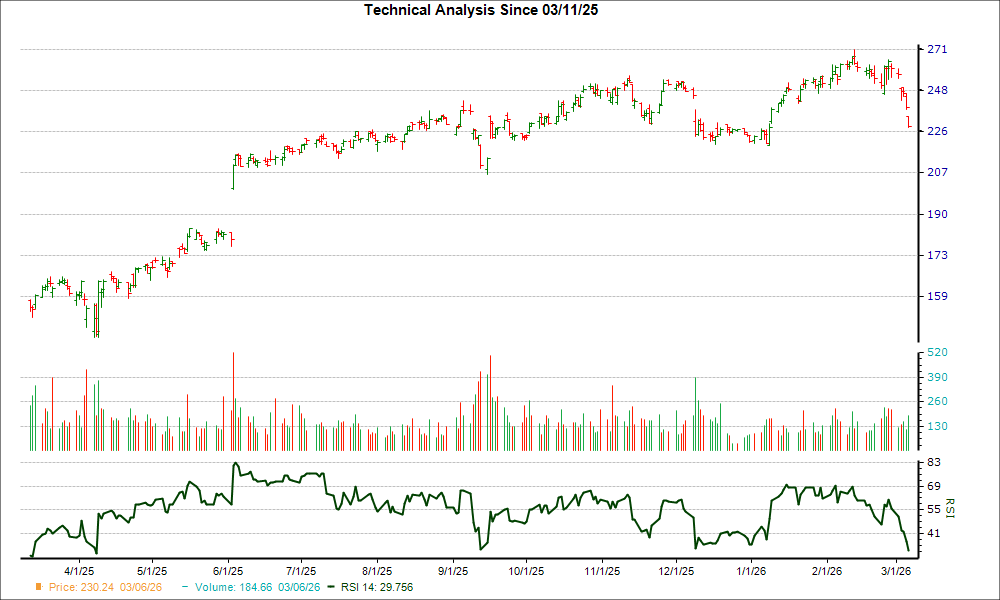
Dave的交易價格低於業內同行:抄底機會還是潛在風險?

The Cooper Companies(COO)過去四週下跌8.8%——潛在的反轉可能即將到來