Humacyte annuncia la presentazione dei risultati a lungo termine sulla sicurezza e sull'efficacia di Symvess al meeting VESS
- Dati presentati al Winter Meeting Annuale 2026 della Vascular & Endovascular Surgery Society -
- Dopo fino a 36 mesi di follow-up, i pazienti con trauma arterioso agli arti hanno mostrato alti tassi di salvataggio dell'arto, bassi tassi di infezione e nessun cedimento strutturale non provocato -
- I risultati sulla durabilità a lungo termine hanno mostrato nessuna dilatazione né restringimento del diametro di Symvess fino a 36 mesi -
DURHAM, N.C., 18 febbraio 2026 (GLOBE NEWSWIRE) -- Humacyte, Inc. (Nasdaq: HUMA), una piattaforma biotecnologica commerciale che sviluppa tessuti umani bioingegnerizzati universalmente impiantabili su scala commerciale, ha annunciato oggi la presentazione di dati a lungo termine che valutano la durabilità di Symvess nei pazienti con trauma arterioso agli arti durante il Winter Meeting Annuale 2026 della Vascular & Endovascular Surgery Society (VESS) a Olympic Valley, CA.
La presentazione, intitolata “Long-Term Outcomes of the Acellular Tissue Engineered Vessel in Extremity Arterial Trauma Repair: Results from the V005 Trial,” è stata tenuta dal Dr. Michael Curi, MD, MPA, Chief, Division of Vascular Surgery, Vice Chair, Department of Surgery, Assoc Prof of Surgery, Rutgers – New Jersey Medical School. Nel trial V005, Symvess ha mantenuto l'integrità strutturale a lungo termine, ha mostrato bassi tassi di infezione e ha supportato alti tassi di salvataggio dell'arto in pazienti seguiti fino a 36 mesi.
"Questi risultati a lungo termine dimostrano il potenziale di Symvess di rispondere alle esigenze dei pazienti traumatizzati quando la vena autologa non è disponibile o fattibile," ha dichiarato il Dr. Curi. "Durante lo studio V005, si sono riscontrati tassi di infezione costantemente bassi, nessun decesso correlato al condotto e un'eccellente durabilità di Symvess fino a tre anni—risultati che si traducono in benefici concreti per pazienti che affrontano lesioni potenzialmente letali per la vita o l’arto, laddove la ricostruzione autologa non è un’opzione."
Tra i partecipanti trattati nello studio di Fase 2/3 V005 vi erano 54 pazienti sottoposti a riparazione vascolare degli arti con Symvess per i quali il trattamento con vena autologa, standard di cura, non era fattibile. All'interno di questa popolazione, una volta risolte le complicanze precoci delle lesioni traumatiche, i tassi di infezione del condotto, salvataggio dell’arto e sopravvivenza dei pazienti si sono stabilizzati e sono rimasti relativamente costanti durante i tre anni di follow-up. Symvess ha mantenuto un tasso di assenza di infezione del 92,9% dai 3 ai 36 mesi, senza infezioni dopo il giorno 37 e solo tre infezioni del condotto in totale. I tassi di salvataggio dell’arto erano dell’87,3% a 12 mesi e dell’82,5% a 24 mesi, nonostante una coorte traumatica gravemente ferita.
La durabilità meccanica a lungo termine è stata anch’essa dimostrata durante lo studio V005. L’ecografia duplex è stata utilizzata per valutare la pervietà e il diametro a metà vaso ad ogni visita di follow-up fino al mese 36. Il diametro medio del vaso del graft non si è discostato materialmente dal valore iniziale di 6mm nei 36 mesi. Inoltre, non vi è stata evidenza di tendenze né verso la dilatazione né verso il restringimento del diametro di Symvess fino a 36 mesi. Gli eventi avversi e quelli avversi gravi sono diminuiti nel tempo, supportando la durabilità a lungo termine di questa riparazione vascolare. Importante, nessun decesso, amputazione o cedimento meccanico è stato attribuito a Symvess. Inoltre, non vi è stata evidenza di rotture spontanee o cedimenti strutturali in alcun paziente durante l’intero periodo di follow-up.
Le ferite vascolari rappresentano una sfida per i chirurghi, e i graft venosi autologhi sono tradizionalmente considerati lo standard di cura grazie alla loro durabilità e ai bassi tassi di infezione. Tuttavia, i graft autologhi non sono sempre fattibili in contesti traumatici in cui le vene sono danneggiate o il tempo per il prelievo è limitato. Symvess (vaso bioingegnerizzato acellulare (ATEV)) è progettato per essere immediatamente disponibile “off-the-shelf”—risparmiando tempo chirurgico critico nelle situazioni di emergenza—e ha anche dimostrato costantemente bassi tassi di infezione.
INDICAZIONE
Symvess è un vaso bioingegnerizzato acellulare indicato per l’uso negli adulti come condotto vascolare per lesioni arteriose agli arti quando è necessario un rivascolarizzazione urgente per evitare la perdita imminente dell’arto, e il graft venoso autologo non è fattibile.
INFORMAZIONI IMPORTANTI SULLA SICUREZZA
AVVERTENZA: CEDIMENTO DEL GRAFT
La perdita di integrità di Symvess dovuta a rottura a metà graft o cedimento anastomotico può causare emorragia potenzialmente letale.
CONTROINDICAZIONI
NON utilizzare Symvess in pazienti che presentano una condizione medica che preclude la terapia antiaggregante a lungo termine (come aspirina o clopidogrel) dopo la risoluzione delle lesioni acute.
AVVERTENZE E PRECAUZIONI
- Rottura del Graft
La rottura del graft vascolare si è verificata in pazienti trattati con Symvess. Informare i pazienti che il sanguinamento arterioso può essere pericoloso per la vita e di richiedere una valutazione medica urgente per qualsiasi segno o sintomo di rottura del graft, come sanguinamento, dolore e gonfiore all’arto, o segni di ischemia dell’arto.
- Cedimento Anastomotico
Il cedimento anastomotico si è verificato in pazienti trattati con Symvess. Negli studi clinici di Symvess, il cedimento anastomotico si è verificato entro i primi 36 giorni dall’impianto. Monitorare i pazienti per segni di cedimento anastomotico come dolore e gonfiore nel sito chirurgico, diminuzione dell’emoglobina o altri segni e sintomi di sanguinamento. Informare i pazienti di richiedere una valutazione medica urgente se presentano segni o sintomi che possano indicare cedimento anastomotico, come sanguinamento, gonfiore o dolore in peggioramento nel sito chirurgico o cambiamenti di colore della pelle sovrastante.
- Trombosi
La trombosi si è verificata in pazienti trattati con Symvess. Nei trial clinici di Symvess, i pazienti hanno ricevuto terapia antiaggregante dopo l’impianto di Symvess per ridurre il rischio di trombosi. Il rischio di trombosi può aumentare nei pazienti che interrompono la terapia antiaggregante. La terapia antiaggregante è raccomandata dopo il trattamento con Symvess.
- Trasmissione di Malattie Infettive
Symvess è prodotto utilizzando cellule e reagenti che possono trasmettere malattie infettive o agenti infettivi. Le cellule utilizzate nella produzione di Symvess derivano da un donatore che soddisfa i requisiti di idoneità per la donazione rispetto alle malattie infettive trasmissibili, che includono screening e test per i rischi associati a virus dell’immunodeficienza umana 1 (HIV-1), virus dell’immunodeficienza umana 2 (HIV-2), virus dell’epatite B (HBV), virus dell’epatite C (HCV) e sifilide (Treponema pallidum). Le banche cellulari risultano negative per virus umani e animali, retrovirus, batteri, funghi, lieviti e micoplasmi. Sebbene tutti i reagenti di origine animale siano testati per virus animali, batteri, funghi e micoplasmi prima dell’uso, queste misure non eliminano il rischio di trasmissione di queste o altre malattie infettive trasmissibili e agenti patogeni. Il siero fetale bovino è selezionato per minimizzare il rischio di trasmissione di una proteina prionica che causa l’encefalopatia spongiforme bovina e la causa di una rara condizione fatale nell’uomo chiamata variante della malattia di Creutzfeldt-Jakob. Non sono state riportate infezioni da agenti trasmissibili durante i test clinici.
REAZIONI AVVERSE
Le reazioni avverse più comuni (con incidenza ≥ 10%) sono state trombosi del graft vascolare, piressia (febbre) e dolore.
Informazioni su Humacyte
Humacyte, Inc. (Nasdaq: HUMA) sta sviluppando una piattaforma biotecnologica dirompente per fornire tessuti umani bioingegnerizzati universalmente impiantabili, costrutti tissutali avanzati e sistemi d’organo progettati per migliorare la vita dei pazienti e trasformare la pratica della medicina. L’azienda sviluppa e produce tessuti acellulari per trattare un’ampia gamma di malattie, lesioni e condizioni croniche. La Biologics License Application di Humacyte per il vaso bioingegnerizzato acellulare (ATEV) per l’indicazione trauma vascolare è stata approvata dalla FDA a dicembre 2024. Gli ATEV sono attualmente anche in fase avanzata di trial clinici per altre applicazioni vascolari, inclusi accesso artero-venoso (AV) per emodialisi e malattia arteriosa periferica (PAD). È inoltre in corso lo sviluppo preclinico per bypass coronarico, cardiochirurgia pediatrica, trattamento del diabete di tipo 1 e molteplici nuove applicazioni cellulari e tissutali. L’ATEV da 6mm di Humacyte per accesso AV in emodialisi è stato il primo candidato prodotto a ricevere la designazione FDA di Regenerative Medicine Advanced Therapy (RMAT) e ha anche ricevuto la designazione Fast Track della FDA. Gli ATEV da 6mm di Humacyte per riparazione arteriosa urgente dopo trauma vascolare agli arti e per PAD avanzata hanno anch’essi ricevuto designazioni RMAT. L’ATEV ha ricevuto la designazione prioritaria per il trattamento del trauma vascolare dal Segretario della Difesa degli Stati Uniti.
Per usi diversi dall’approvazione FDA per l’indicazione trauma vascolare agli arti, l’ATEV è un prodotto sperimentale e non è stato approvato per la vendita dalla FDA né da altre agenzie regolatorie.
Esclusione di responsabilità: il contenuto di questo articolo riflette esclusivamente l’opinione dell’autore e non rappresenta in alcun modo la piattaforma. Questo articolo non deve essere utilizzato come riferimento per prendere decisioni di investimento.
Ti potrebbe interessare anche
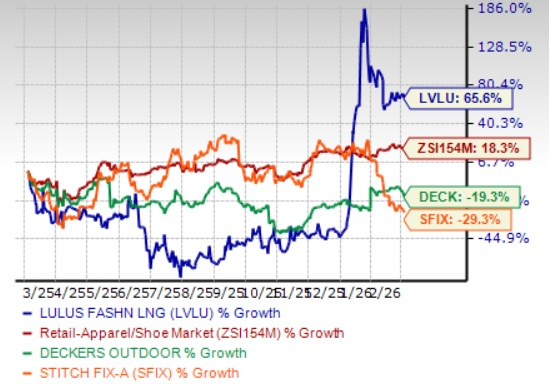
Il titolo Lulus aumenta del 66% nell'ultimo anno: è questo il momento giusto per investire?
Le azioni rafforzate dalle aspettative di una rapida risoluzione del conflitto con l'Iran
SHIB aumenta del 5% mentre le meme coin attirano investitori: cosa succede ora a Shiba Inu?

Globus Medical (GMED) alzata a Strong Buy: quali sono le implicazioni per il titolo?

