FDAがDisc Medicineの希少疾患治療薬の承認を延期
Disc Medicine Inc.(NASDAQ:IRON)の株価は金曜日に約22%下落して取引を終えました。同社は、bitopertinに関する米国食品医薬品局(FDA)からの完全回答書(CRL)という規制上の問題に直面しています。火曜日には株価が上昇しています。
Bitopertinは迅速承認の審査対象となっており、Commissioner’s National Priority Voucher(CNPV)パイロットプログラムの一環でもあります。
1月、FDAの審査担当者はbitopertinの決定を約2週間延期し、2月10日までとしました。
規制当局は、試験の副次的評価項目である「痛みのない太陽下での時間」が効果の統計的に信頼できる指標であるか、またはバイオマーカーのデータが承認の裏付けとなるかどうかについて疑問を呈しました。
FDAによる阻止
FDAは、Disc Medicineのbitopertinに関する新薬承認申請にCRLを発行しました。この薬は、極度の光過敏症を引き起こす稀な疾患である赤芽球性プロトポルフィリン症(EPP)の治療を目的としています。
当局は、臨床試験が全血の遊離金属PPIXを低減する薬剤の有効性を示す証拠は提供したものの、臨床的利益との明確な関連性を示せなかったと結論付けており、これが承認プロセスを遅らせています。
同社は金曜日、迅速承認は提案されている代替エンドポイント(全血遊離金属PPIXの%変化)への効果の証拠、ならびに変化の大きさを含めたこの代替エンドポイントが臨床的利益を予測する合理的可能性があるかどうかに依存すると述べました。
最初の点については、FDAはAURORAとBEACONがbitopertinが全血遊離金属PPIXを有意に低減することを十分に証明していることに同意しました。
二つ目の点については、AURORAとBEACONの結果のレビューに基づき、FDAはPPIXの%変化と日光曝露に基づくエンドポイントとの関連性を示す証拠がなかったと結論付けました。これは、プロトポルフィリン症におけるPPIXバイオマーカーの使用を支持する強い力学的および生物学的妥当性があるにもかかわらずです。
FDAは、APOLLO試験の結果が従来型承認を支持する証拠となり得ると示唆しました。
CRLへの対応として、Disc Medicineは現在進行中のAPOLLO試験に自信を示しており、2026年第4四半期にトップラインデータが得られる見込みです。
同社は次のステップについてFDAとのType Aミーティングを要請する計画です。Discは2025年12月31日時点で約7億9100万ドルのキャッシュポジションを維持しており、2029年まで資金が持続する見通しを示しています。
テクニカル分析
現在、株価は20日単純移動平均(SMA)を4.4%上回り、100日SMAを2.2%下回っています。これは短期的な強さを示す一方で、長期的な平均での抵抗がある可能性を示唆しています。過去12か月で株価は2.42%上昇しており、現在は52週高値に近い位置にあります。これは比較的強いパフォーマンスを示しています。
RSIは中立水準にあり、現時点で株価が買われすぎでも売られすぎでもないことを示しています。一方でMACDはシグナルラインを下回っており、株価に弱気圧力がかかっていることを示唆しています。
中立的なRSIと弱気のMACDの組み合わせは、現時点でDisc Medicineに混合的なモメンタムがあることを示しています。
- 主要レジスタンス: $60.00
- 主要サポート: $55.00
アナリストのコンセンサスと最近の動向:この株はBuyレーティングで、平均目標株価は$102.00です。最近のアナリストの動きは以下の通りです:
- Wells Fargo: Overweight(目標株価を$109に引き上げ)
- Truist Securities: Buy(目標株価を$114に引き上げ)
- Stifel: Buy(目標株価$125)
IRONの値動き:Disc Medicineの株価は火曜日のプレマーケット取引で4.40%高の$58.41となっています。
画像:Tada Images/Shutterstockより
免責事項:本記事の内容はあくまでも筆者の意見を反映したものであり、いかなる立場においても当プラットフォームを代表するものではありません。また、本記事は投資判断の参考となることを目的としたものではありません。
こちらもいかがですか?
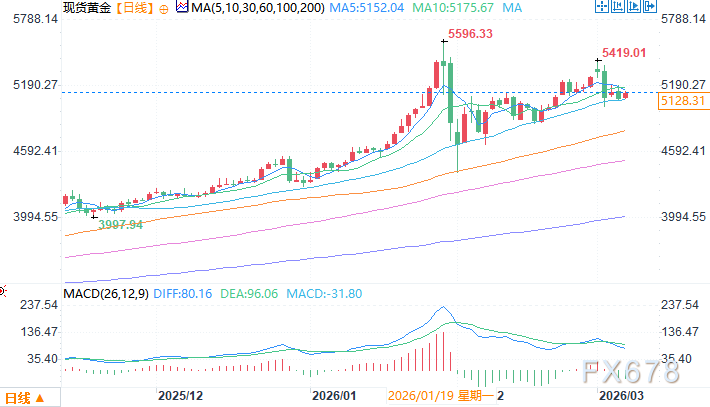
経済学者が重大警告:短期取引を長期投資と見なさないでください 金価格は5年以内に8000ドルに達する可能性
NVIDIAの喉元

1兆ドル市場がウォール街を震撼させる!ゴールドマン・サックス伝説のCEOが警告:プライベート・クレジットのリスクは2008年直前に酷似
カストディ銀行株の2023年第4四半期業績: State Street(NYSE:STT)との比較