Inanunsyo ng Larimar Therapeutics ang FDA Breakthrough Therapy Designation para sa Nomlabofusp sa FA at muling tiniyak ang nakaplanong BLA submission sa Hunyo 2026
- Ang Nomlabofusp program ay nabigyan ng Breakthrough Therapy Designation para sa paggamot ng mga matatanda at bata na may FA batay sa pagsusuri ng FDA ng magagamit na klinikal na datos mula sa open label na pag-aaral
- Ang mga sulat mula sa FDA pagkatapos ng kamakailang START na pagpupulong ay patuloy na sumusuporta sa paggamit ng skin FXN upang suportahan ang BLA submission na naghahangad ng pinabilis na pag-apruba
- Inaasahan ang pangunahing datos mula sa open label na pag-aaral upang suportahan ang BLA submission sa Q2 2026
- Nakaplanong BLA submission na naghahangad ng pinabilis na pag-apruba ay nasa tamang landas para sa Hunyo 2026; Target ang paglulunsad sa U.S. sa unang kalahati ng 2027, kung maaaprubahan
BALA CYNWYD, Pa., Peb. 24, 2026 (GLOBE NEWSWIRE) -- Inanunsyo ngayon ng Larimar Therapeutics, Inc. (Larimar) (Nasdaq: LRMR), isang clinical-stage biotechnology company na nakatuon sa pag-develop ng mga paggamot para sa mga komplikadong bihirang sakit, na ang U.S. Food and Drug Administration (FDA) ay nagbigay ng Breakthrough Therapy Designation (BTD) sa nomlabofusp, isang frataxin (FXN) protein replacement therapy na may potensyal na baguhin ang sakit, para sa paggamot ng mga matatanda at bata na may Friedreich’s ataxia (FA). Dagdag pa rito, matapos ang isang Support for Clinical Trials Advancing Rare Disease Therapeutics (START) pilot program meeting sa FDA, inanunsyo ng kumpanya ang patuloy na pagkakaayon sa FDA upang isaalang-alang ang paggamit ng skin FXN bilang isang bagong surrogate endpoint na malamang na magpredict ng klinikal na benepisyo upang suportahan ang nakaplanong Biologics License Application (BLA) submission na naghahangad ng pinabilis na pag-apruba. Mayroon ding kasunduan tungkol sa mga may kaugnayang klinikal na kinalabasan na may konsistenteng positibong pagbabago sa lahat ng apat na klinikal na kinalabasan na sinuri at ang uri ng pagsusuri na kinakailangan upang suportahan ang exposure response relationships para sa nomlabofusp program. Sinabi ng FDA na ang sapat ng safety database ay rerepasuhin sa oras ng BLA submission. Target ng nakaplanong BLA submission ang Hunyo 2026.
Ang Breakthrough Therapy Designation at feedback ng FDA ukol sa BLA submission ay nakabase sa pagsusuri ng FDA sa magagamit na klinikal na datos mula sa nagpapatuloy na open label (OL) study ng Kumpanya na sinusuri ang nomlabofusp sa mga adult at pediatric na pasyente na may FA.
Nabigyan ng Breakthrough Therapy Designation ng FDA ang Nomlabofusp para sa Paggamot ng FA
Layunin ng Breakthrough Therapy Designation na pabilisin ang pag-unlad at regulatory review ng isang gamot na nilalayon para sa isang seryosong kondisyon. Ang isang gamot ay kwalipikado para sa BTD kung ang paunang klinikal na ebidensiya ay nagpapahiwatig na ang gamot ay maaaring magpakita ng malaking pagpapabuti kumpara sa mga kasalukuyang paggamot sa isa o higit pang klinikal na makabuluhang endpoints.
Ang Breakthrough Therapy Designation request para sa nomlabofusp ay kinabibilangan ng paunang klinikal na datos mula sa OL study na nagpapakita ng pagtaas ng skin FXN sa mga lebel na inaasahan sa mga asymptomatic carriers at konsistenteng positibong pagbabago sa apat na pangunahing klinikal na kinalabasan kabilang ang modified Friedreich Ataxia Rating Scale (mFARS) score, FARS-Activities of Daily Living (ADL), 9 Hole Peg Test (9-HPT), at Modified Fatigue Impact Scale (MFIS) pagkatapos ng 1-taon ng paggamot. Ang mga natuklasan na ito ay nagpapatibay sa potensyal ng nomlabofusp na mapabuti ang takbo ng sakit na FA kumpara sa patuloy na paglala na napansin sa reference group mula sa Friedrich’s Ataxia Clinical Outcomes Measure Study (FACOMS) natural history study.
“Patuloy na mayroong malaking pasanin ng sakit na nararanasan ng tinatayang 5,000 bata at matatanda sa U.S. na may FA. Ang pagkakatanggap ng Breakthrough Therapy Designation ay nagpapahiwatig ng pagkilala ng FDA sa mataas na hindi natutugunang pangangailangang medikal at sa potensyal ng nomlabofusp na magpakita ng malaking pagpapabuti kumpara sa kasalukuyang therapy sa mga klinikal na makabuluhang endpoints,” sabi ni Dr. Rusty Clayton, Chief Medical Officer ng Larimar. “Bilang bahagi ng BTD request, sinuri ng FDA ang paunang datos ng nomlabofusp na nagpapakita ng mga pagpapabuti sa mFARS score, ADL, 9-HPT performance, pati na rin sa nabawasang pagkapagod, sa konteksto ng pagtaas ng tissue FXN sa mga lebel na katulad ng nakikita sa mga asymptomatic carriers na walang senyales ng sakit. Kami ay na-eenganyo sa lumalaking katawan ng klinikal na datos na sumusuporta sa potensyal ng nomlabofusp na baguhin ang pag-usad ng sakit sa pamamagitan ng pagtutok sa pinagmulan ng FA, ang kakulangan sa FXN. Inaasahan naming ang patuloy na pakikipagtulungan sa FDA habang kami ay tumutungo sa potensyal na pagrerehistro.”
Mga Komento mula sa FDA Meeting na Sumusuporta sa Nakaplanong BLA Submission para sa Nomlabofusp sa Hunyo 2026
Dagdag ni Dr. Carole Ben-Maimon, MD, Pangulo at Chief Executive Officer ng Larimar, “Kami ay natutuwa na patuloy na may aktibong pakikipag-ugnayan sa FDA tungkol sa aming nakaplanong BLA submission para sa nomlabofusp at pinahahalagahan namin ang masusing pagsusuri ng FDA sa paunang klinikal na datos. Ang regulatory progress na ito ay sumusuporta sa aming kahandaan sa BLA na naghahangad ng pinabilis na pag-apruba at nagbibigay daan upang kami ay makapagpokus sa patuloy na pagpapatupad. Kami ay nakatuon sa pagbibigay ng matatag at komprehensibong data package na sumasalamin sa paborableng benefit-risk profile ng nomlabofusp at sa potensyal nito na makapagbigay ng makabuluhang pagpapabuti ng kinalabasan para sa mga pasyente na may FA. Patuloy naming pinaplano ang BLA submission sa Hunyo 2026 na naghahangad ng pinabilis na pag-apruba at nasasabik kaming simulan ang aming confirmatory Phase 3 study sa U.S., E.U., U.K., Canada at Australia. Ipinagmamalaki naming ang mga clinical trial applications na may kaugnayan sa aming Phase 3 study ay kasalukuyang nire-review sa France at Canada, at magpapasa rin kami sa U.K. regulatory authorities sa lalong madaling panahon.”
Kaugnay ng kamakailang START meeting, sinuri ng FDA ang paunang klinikal na datos para sa nomlabofusp program at nagpatuloy sa pagbibigay ng positibong feedback ukol sa BLA content:
- FXN bilang Surrogate Endpoint: Muling pinagtibay ng FDA ang kahandaang isaalang-alang ang paggamit ng FXN bilang bagong surrogate endpoint at kinumpirma ang pagsusuri ng Larimar sa exposure-response na nag-eexplore ng relasyon ng nomlabofusp exposures at mga klinikal na outcome measures bilang uri ng pagsusuri na maaaring sumuporta sa hinaharap na BLA submission.
- Reference Population: Kumpirmado ng FDA ang proseso para sa pagpili ng reference population batay sa matched subjects mula sa FACOMS database para sa natural history comparisons ng klinikal na endpoints na gagamitin para sa BLA submission at nag-alok na magbigay ng advance review at komento sa statistical plan.
- Safety Dataset: Sinabi ng FDA na ang pagiging sapat ng safety dataset ay rerepasuhin sa oras ng BLA submission.
- Global Phase 3 Study: Kaayon ng FDA ang plano na isagawa ang global confirmatory Phase 3 study kasabay ng BLA submission at kinumpirma na ang pagbabago mula baseline sa Upright Stability Score (USS) (isang subscale ng mFARS) ay isang makatwiran at klinikal na mahalagang pangunahing endpoint para sa nakaplanong Phase 3 study.
Dagdag ni Dr. Marshall Summar, Chief Executive Officer (CEO) ng Uncommon Cures, dating Founding Director ng Rare Disease Institute at Margaret O’Malley Chair of Genetic Medicine sa Children’s National Hospital, “Bilang CEO ng isang key clinical site sa OL study at isang career Medical Geneticist, nasaksihan ko mismo ang malaking pasanin na dulot ng FA sa mga pasyente at kanilang pamilya. Ang mga datos na nalikha sa ngayon ay nagpapahiwatig na ang nomlabofusp ay may potensyal na positibong baguhin ang pinagbabatayang biyolohiya ng sakit at maisalin ito sa mga klinikal na mahalagang benepisyo. Ang mga klinikal na pagpapabuti na napansin sa ngayon ay promising at nagmamarka ng isang makabuluhang hakbang tungo sa maaaring maging unang disease-modifying therapy para sa isang populasyon ng pasyente na may malaking hindi natutugunang pangangailangang medikal.”
Inaasahang Malalapit na Milestones
- Pangunahing datos ng OL study para suportahan ang BLA submission inaasahan sa Q2 2026
- Plano na simulan ang screening sa global confirmatory Phase 3 study sa Q2 2026; inaasahan ang dosing ng unang pasyente sa gitna ng 2026
- Ang BLA na naghahangad ng pinabilis na pag-apruba planong isumite sa Hunyo 2026
- Target ang paglulunsad sa U.S. sa unang kalahati ng 2027, kung maaaprubahan
Tungkol sa Larimar Therapeutics
Ang Larimar Therapeutics, Inc. (Nasdaq: LRMR), ay isang clinical-stage biotechnology company na nakatuon sa pag-develop ng mga paggamot para sa komplikadong bihirang mga sakit. Ang pangunahing compound ng Larimar, ang nomlabofusp, ay dine-develop bilang potensyal na paggamot para sa Friedreich's ataxia. Plano rin ng Larimar na gamitin ang intracellular delivery platform nito upang magdisenyo ng iba pang fusion proteins na tutok sa karagdagang bihirang mga sakit na may kakulangan sa intracellular bioactive compounds.
Pahayag ukol sa Hinaharap
Ang press release na ito ay naglalaman ng mga pahayag ukol sa hinaharap na nakabase sa paniniwala at mga palagay ng pamunuan ng Larimar at sa impormasyon na kasalukuyang magagamit sa pamunuan. Lahat ng pahayag sa release na ito maliban sa mga pahayag ng kasaysayang katotohanan ay pahayag ukol sa hinaharap, kabilang ngunit hindi limitado sa mga pahayag ukol sa kakayahan ng Larimar na mag-develop at magkomersyalisa ng nomlabofusp at iba pang nakaplanong produkto, mga nakaplanong pagsisikap sa pananaliksik at pag-develop ng Larimar, kabilang ang iskedyul ng mga klinikal na pagsubok ng nomlabofusp, interaksyon at submission sa FDA, inaasahan ukol sa potensyal para sa pinabilis na pag-apruba o pinabilis na access at oras sa merkado at pangkalahatang plano ng pag-unlad at iba pang usapin ukol sa mga estratehiya ng negosyo ng Larimar, kakayahan na makalikom ng kapital, paggamit ng kapital, resulta ng operasyon at posisyong pinansyal, at mga plano at layunin para sa mga susunod na operasyon.
Sa ilang kaso, maaari mong matukoy ang mga pahayag ukol sa hinaharap sa mga salitang “maaari,” “magiging,” “kaya,” “dapat,” “inaasahan,” “layon,” “plano,” “inaasahan,” “naniniwala,” “tinataya,” “hinuhulaan,” “proyekto,” “potensyal,” “patuloy,” “nakatutok” o ang negatibo ng mga terminong ito o ibang katulad na termino, bagaman hindi lahat ng pahayag ukol sa hinaharap ay naglalaman ng mga salitang ito. Ang mga pahayag na ito ay may kasamang mga panganib, kawalang-katiyakan at iba pang mga salik na maaaring magdulot ng aktuwal na resulta, pagganap, o tagumpay na malayong naiiba mula sa impormasyong ipinaabot o ipinahiwatig ng mga pahayag ukol sa hinaharap na ito. Kasama sa mga panganib, kawalang-katiyakan at iba pang mga salik na ito, bukod sa iba pa, ang tagumpay, gastos at iskedyul ng mga aktibidad sa pag-unlad ng produkto ng Larimar, mga nonclinical na pag-aaral at mga klinikal na pagsubok, kabilang ang mga klinikal at regulatory milestones ng nomlabofusp at patuloy na interaksyon sa FDA; na ang paunang resulta ng clinical trial ay maaaring iba sa huling resulta ng clinical trial, na mas naunang non-clinical at klinikal na datos at pagsusuri ng nomlabofusp ay maaaring hindi magpahiwatig ng resulta o tagumpay ng mga susunod na clinical trial, at mga pagtatasa; na maaaring hindi sumang-ayon ang FDA sa huli sa development strategy ng nomlabofusp ng Larimar; kakayahan ng Larimar na makuha ang benepisyo ng Breakthrough Therapy Designation; potensyal na epekto ng mga pampublikong krisis sa kalusugan sa mga susunod na klinikal na pagsubok ng Larimar, manufacturing, regulatory, nonclinical study timelines at operasyon, at pangkalahatang kondisyon ng ekonomiya; kakayahan ng Larimar at ng mga third-party manufacturers na kinukuha ng Larimar, na i-optimize at i-scale ang manufacturing process ng nomlabofusp; kakayahan ng Larimar na makakuha ng regulatory approvals para sa nomlabofusp at mga susunod na produkto; kakayahan ng Larimar na bumuo ng sales at marketing capabilities, mag-isa man o kasama ang mga potensyal na future collaborators, at matagumpay na maikomersyalisa ang anumang naaprubahang produkto; kakayahan ng Larimar na makalikom ng kinakailangang kapital para isagawa ang mga aktibidad sa pag-unlad ng produkto; at iba pang panganib na inilarawan sa mga filing na ginawa ng Larimar sa Securities and Exchange Commission (SEC), kabilang ngunit hindi limitado sa mga periodic reports ng Larimar, tulad ng annual report sa Form 10-K, quarterly reports sa Form 10-Q at current reports sa Form 8-K, na naifile o naipadala sa SEC at makikita sa Ang mga pahayag ukol sa hinaharap na ito ay nakabase sa kombinasyon ng mga katotohanan at mga salik na kasalukuyang alam ng Larimar at ng mga projection nito sa hinaharap, na hindi nito kayang matiyak. Bilang resulta, maaaring hindi magkatotoo ang mga pahayag ukol sa hinaharap. Ang mga pahayag ukol sa hinaharap sa press release na ito ay kumakatawan lamang sa pananaw ng pamunuan ng Larimar sa petsa nito. Ang Larimar ay walang obligasyon na i-update ang anumang pahayag ukol sa hinaharap para sa anumang dahilan, maliban kung hinihingi ng batas.
Investor Contact:
Joyce Allaire
LifeSci Advisors
Company Contact:
Michael Celano
Chief Financial Officer
Disclaimer: Ang nilalaman ng artikulong ito ay sumasalamin lamang sa opinyon ng author at hindi kumakatawan sa platform sa anumang kapasidad. Ang artikulong ito ay hindi nilayon na magsilbi bilang isang sanggunian para sa paggawa ng mga desisyon sa investment.
Baka magustuhan mo rin
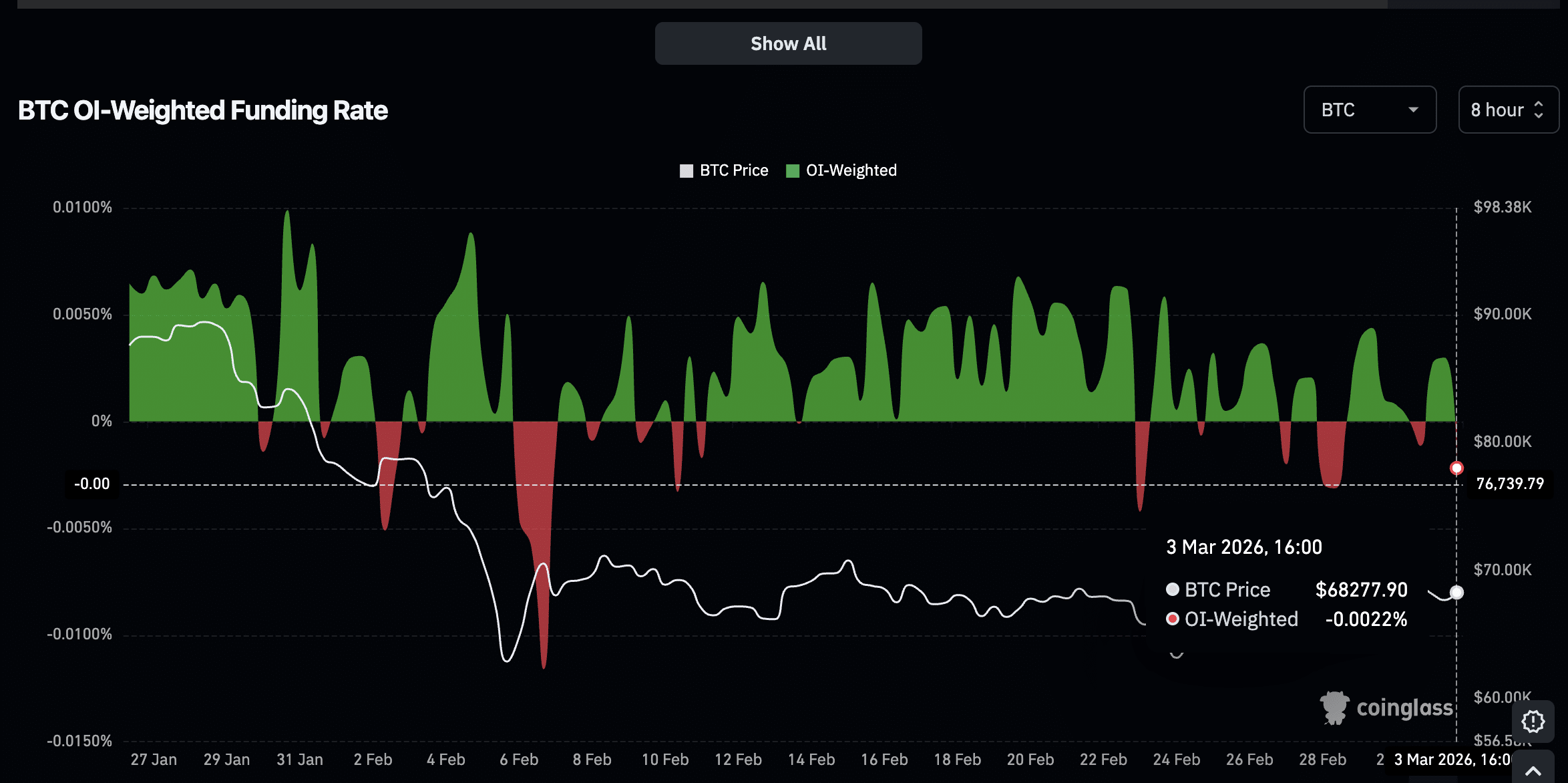
Negative ang pagpopondo sa Bitcoin habang ang BTC ay nagko-konsolida malapit sa $68K