DNLI relata prejuízo menor do que o esperado no quarto trimestre, com destaque para o tratamento da Síndrome de Hunter
Visão Financeira do Quarto Trimestre de 2025 da Denali Therapeutics
A Denali Therapeutics (DNLI) registrou um prejuízo líquido de $0,73 por ação no quarto trimestre de 2025, um resultado ligeiramente melhor do que a estimativa consensual de perda de $0,75. Isso se compara a uma perda de $0,67 por ação no mesmo período do ano anterior.
O aumento anual da perda por ação foi impulsionado principalmente pelo crescimento das despesas operacionais.
Como a Denali não possui produtos no mercado, sua receita é limitada aos rendimentos de parcerias em andamento. No trimestre reportado, a empresa não registrou receita de colaboração, ficando aquém dos $18 milhões esperados.
No último ano, as ações da DNLI subiram 13,4%, superando o setor médico, biomédico e de genética, que apresentou um aumento de 11,5%.
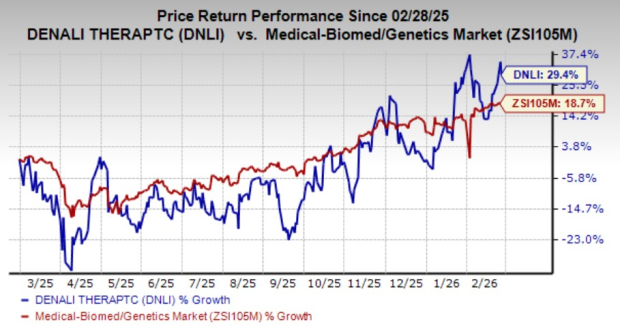
Fonte: Zacks Investment Research
Pontos-Chave dos Resultados do Quarto Trimestre
- Os custos de pesquisa e desenvolvimento caíram 1,9%, para $97,9 milhões, principalmente devido à redução de gastos em projetos de pequenas moléculas.
- As despesas gerais e administrativas aumentaram 31,3%, alcançando $39,5 milhões, refletindo preparativos para o esperado lançamento do tividenofusp alfa.
- Em 31 de dezembro de 2025, a Denali possuía aproximadamente $966,2 milhões em caixa, equivalentes de caixa e valores mobiliários negociáveis.
Resumo do Ano Fiscal de 2025
- Não houve geração de receita durante 2025.
- A perda anual por ação aumentou para $2,97, em comparação a $2,57 em 2024.
Progresso do Principal Candidato a Medicamento
A Denali está ativamente se preparando para a introdução comercial de seu principal ativo, o tividenofusp alfa.
A solicitação de licença biológica (BLA) para tividenofusp alfa, voltada para o tratamento da mucopolissacaridose tipo II (síndrome de Hunter), está atualmente sob análise dos reguladores dos EUA.
A FDA estendeu o prazo de análise de 5 de janeiro de 2026 para 5 de abril de 2026.
O tividenofusp alfa recebeu diversas designações da FDA, incluindo Breakthrough Therapy, Fast Track, Orphan Drug e Rare Pediatric Disease.
Esta terapia em investigação foi desenvolvida para administrar a enzima iduronato-2-sulfatase (IDS) através da barreira hematoencefálica, visando tanto o corpo quanto o cérebro.
O período de análise da BLA foi ampliado depois que a Denali forneceu dados atualizados de farmacologia clínica em resposta a um pedido da FDA. A empresa esclareceu que essa atualização não estava relacionada à eficácia, segurança ou biomarcadores.
A FDA classificou a submissão como uma alteração significativa, resultando na extensão da data de ação.
O estudo global de fase II/III COMPASS em andamento deverá fornecer evidências de apoio para submissões regulatórias em todo o mundo, com a inscrição de participantes neuronopáticos (Cohorte A) concluída em dezembro de 2025.
Desenvolvimentos do Pipeline
- A Denali está investigando o DNL126 para a síndrome de Sanfilippo tipo A (MPS IIIA). Resultados preliminares de fase I/II apresentados no WORLDSymposium mostraram reduções significativas em biomarcadores-chave da doença e um perfil de segurança semelhante às terapias de reposição enzimática existentes. Esses achados podem apoiar um caminho de aprovação acelerada, e um estudo confirmatório de fase III está planejado.
- Outros candidatos do pipeline estão sendo desenvolvidos em colaboração com a Takeda (TAK), Biogen (BIIB) e Sanofi (SNY).
- Denali e Takeda estão avançando com o DNL593, um tratamento potencial para demência frontotemporal associada à mutação da granulina (FTD-GRN). A inscrição para o estudo de fase I/II está completa, com 40 participantes. Os primeiros dados de pacientes são esperados em 2026.
- A Denali recebeu recentemente aprovação para um estudo de fase Ib do DNL628, com preparativos em andamento.
- Denali e Biogen estão desenvolvendo conjuntamente o BIIB122. A Biogen lidera o estudo global de fase IIb LUMA para doença de Parkinson em estágio inicial, com resultados previstos para meados de 2026. A Denali conduz o estudo de fase IIa BEACON para avaliar a inibição de LRRK2 na doença de Parkinson associada a LRRK2.
- Em outubro, a Denali submeteu um IND para o DNL952 (ETV:GAA) para iniciar estudos clínicos em doença de Pompe. A FDA desde então suspendeu a restrição clínica, e os preparativos para o estudo de fase I estão em andamento.
- A Sanofi está desenvolvendo o eclitasertib para colite ulcerativa moderada a grave, com dados de fase II esperados para o primeiro semestre do ano.
Análise das Perspectivas da Denali
A aprovação do tividenofusp alfa pode impulsionar significativamente a trajetória de crescimento da Denali. O progresso com o DNL126 também é promissor.
As robustas reservas de caixa da empresa evidenciam sua capacidade de suportar iniciativas contínuas de pesquisa e desenvolvimento.
Aviso Legal: o conteúdo deste artigo reflete exclusivamente a opinião do autor e não representa a plataforma. Este artigo não deve servir como referência para a tomada de decisões de investimento.
Talvez também goste
Abel da Berkshire compromete todo o salário para comprar ações da empresa

A ITV afirma que a venda para a Sky continua em andamento apesar da queda na receita de publicidade

A ReElement da AREC aumenta as capacidades do laboratório avançado de terras raras