Європа схвалила новий дворазовий на рік засіб від астми від GSK
Європейська комісія у вівторок схвалила GSK plc’s (NYSE:GSK) Exdensur (depemokimab) за двома показаннями, зокрема:
- Як додаткову підтримуючу терапію для важкої астми з типом 2 запалення, що характеризується рівнем еозинофілів у крові у дорослих та підлітків віком від 12 років, у яких захворювання недостатньо контролюється, незважаючи на застосування інгаляційних кортикостероїдів у високих дозах у поєднанні з іншим контролюючим препаратом від астми.
- Як додаткову терапію з інтраназальними кортикостероїдами для дорослих пацієнтів із тяжким CRSwNP, у яких системні кортикостероїди та/або хірургічне втручання не забезпечують належного контролю захворювання.
Схвалення базується на даних досліджень SWIFT та ANCHOR фази 3, які продемонстрували стійку ефективність при схемі введення depemokimab двічі на рік.
Дані дослідження
Кожне з чотирьох досліджень досягло своїх первинних або співпервинних кінцевих точок зі статистично значущими та клінічно важливими результатами, порівнюючи додавання depemokimab до стандартної терапії зі стандартною терапією окремо.
Астма уражає понад 42 мільйони людей у Європі. Близько 5-10% пацієнтів страждають на важку астму, при цьому багато хто продовжує відчувати загострення і зниження якості життя, незважаючи на лікування.
Крім того, пацієнти із CRSwNP стикаються з виснажливими щоденними симптомами, і майже половина залишається неконтрольованою.
Exdensur — це нова терапія, яка поєднує високу спорідненість до зв’язування з інтерлейкіном-5 (IL-5) та високу потужність із подовженим періодом напіввиведення, що забезпечує тривале пригнічення запалення типу 2, яке спричиняє захворювання, при введенні двічі на рік.
У дослідженнях SWIFT фази 3 лікування depemokimab призвело до значного зниження на 58% та 48% річної частоти загострень астми (астматичних нападів) протягом 52 тижнів у SWIFT-1 та SWIFT-2 відповідно.
За вторинною кінцевою точкою у SWIFT-1 та SWIFT-2 пацієнти, які отримували depemokimab, мали чисельно менше загострень, що вимагали госпіталізації та/або звернення до відділення невідкладної допомоги (1% та 4%), порівняно з плацебо (8% та 10%) відповідно.
Попередньо визначений об’єднаний аналіз двох досліджень показав 72% зниження річної частоти клінічно значущих загострень, що вимагали госпіталізації та/або звернення до відділення невідкладної допомоги протягом 52 тижнів при застосуванні depemokimab порівняно з плацебо.
Крім того, у дослідженнях ANCHOR фази 3 лікування depemokimab призвело до покращення (зниження) від вихідного рівня бала поліпів носа (шкала: 0-8) на 52 тижні та за шкалою словесної оцінки обструкції носа протягом тижнів 49-52.
Передумови
У грудні 2025 року Управління з контролю за продуктами і ліками США (FDA) схвалило Exdensur як додаткову підтримуючу терапію тяжкої астми, що характеризується еозинофільним фенотипом у пацієнтів віком від 12 років.
Також Exdensur нещодавно отримав схвалення у Великій Британії та Японії для лікування тяжкої астми та CRSwNP.
Динаміка цін: Акції GSK зросли на 2,65% до $60,49 під час передринкової сесії за останньою перевіркою у вівторок, згідно з даними Benzinga Pro.
Фото: JPC_PROD через Shutterstock
Відмова від відповідальності: зміст цієї статті відображає виключно думку автора і не представляє платформу в будь-якій якості. Ця стаття не повинна бути орієнтиром під час прийняття інвестиційних рішень.
Вас також може зацікавити
Утворюється «bull trap» на Bitcoin, оскільки ведмежий ринок переходить у середню фазу: Віллі Ву
Звіт Міністерства фінансів США визнає легітимне використання криптоміксерів
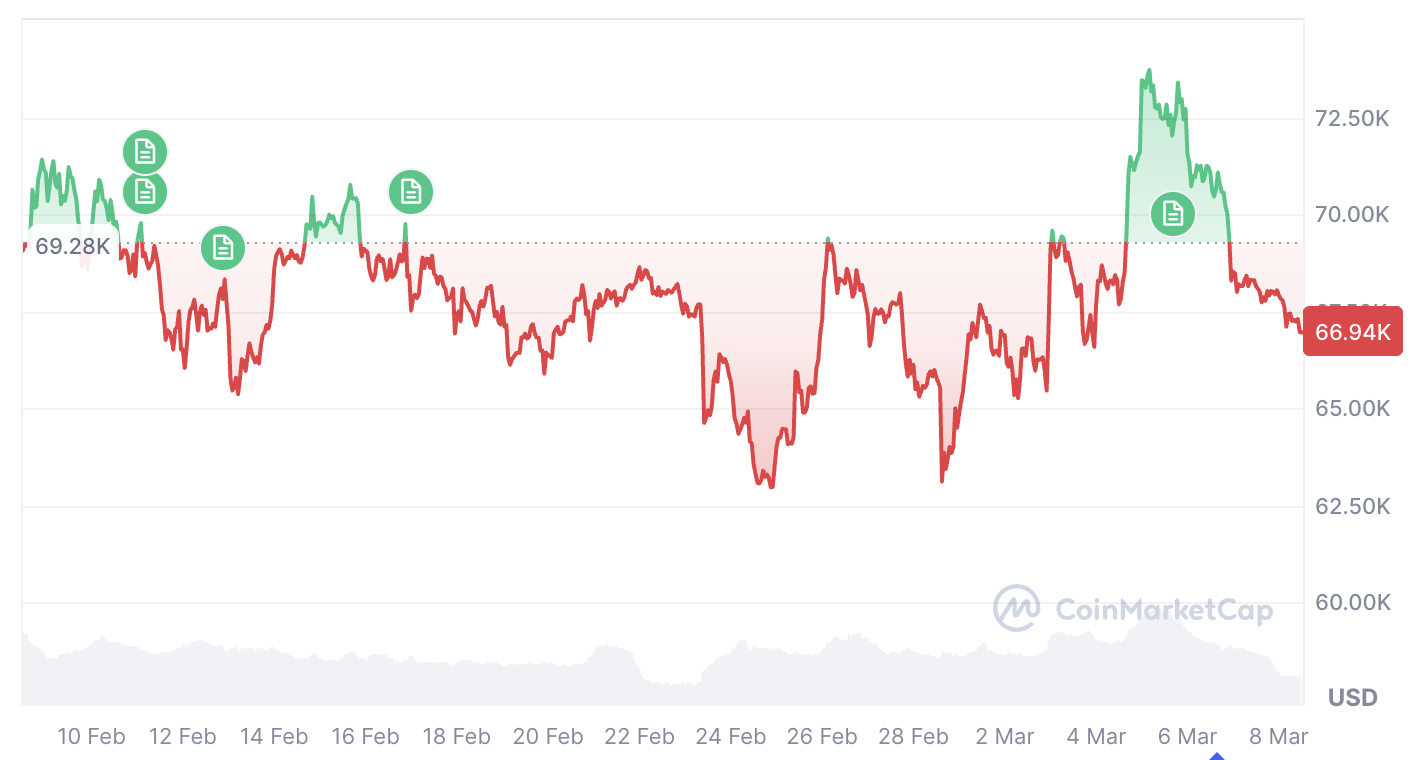
Сектор AI зростає до $14,4 млрд, однак Bittensor слабшає – чи повернеться TAO до $165?