EyePoint призначає Майкла Кемпбелла на посаду директора з комерційних питань
– Досвідчений комерційний керівник із понад 30-річним стажем у сфері захворювань сітківки в біотехнологіях та великих фармацевтичних компаніях –
– Може похвалитися перевіреним досвідом успішного запуску продуктів та управління провідними офтальмологічними франшизами, включаючи Lucentis
WATERTOWN, Массачусетс, 18 лютого 2026 (GLOBE NEWSWIRE) -- EyePoint, Inc. (Nasdaq: EYPT), компанія, що займається розробкою та комерціалізацією інноваційних терапевтичних засобів для покращення життя пацієнтів із серйозними захворюваннями сітківки, сьогодні оголосила про призначення Майкла Кемпбелла на посаду головного комерційного директора. Пан Кемпбелл, досвідчений комерційний лідер із перевіреним досвідом успішних запусків продуктів та управління провідними офтальмологічними франшизами, візьме на себе відповідальність за комерційну стратегію EyePoint та готовність до запуску DURAVYU
“Майк — досвідчений комерційний лідер, і ми раді вітати його в EyePoint у справді трансформаційний період для компанії,” — сказав Джей С. Дукер, доктор медичних наук, президент і генеральний директор EyePoint. “Майк має перевірений досвід успішного запуску інноваційних офтальмологічних продуктів, які змінили ландшафт лікування захворювань сітківки, включаючи революційний запуск Lucentis, який став еталоном у лікуванні сітківки. З оголошенням основних даних нашої ключової програми Фази 3 у wet AMD, які очікуються з середини 2026 року, його глибока комерційна експертиза буде вирішальною при позиціонуванні DURAVYU для успішного запуску в США як потенційно першого тривалого релізу TKI на ринку. Лідерство Майка та його комерційна експертиза ще більше зміцнюють нашу здатність впроваджувати, масштабувати та надавати пацієнтам нові варіанти лікування.”
“Я радий приєднатися до EyePoint у критичний час і стати частиною компанії, яка повністю відповідає моїй пристрасті до впровадження терапевтичних інновацій для пацієнтів,” — сказав пан Кемпбелл. “Мене вразив підхід EyePoint, орієнтований на зниження ризиків та пацієнтів, до просування програм Фази 3, включаючи ретельно продумані дизайни досліджень, які відображають реальну клінічну практику та можуть підтримати переконливу характеристику продукту. Завдяки значним клінічним даним як щодо wet AMD, так і DME, багатомеханізмовій дії та як єдиний TKI, що розробляється для DME, DURAVYU пропонує значний комерційний потенціал та можливість стати новим золотим стандартом лікування захворювань сітківки. Я з нетерпінням чекаю застосування досвіду, отриманого під час численних запусків на ринку сітківки, що були зумовлені інноваціями, точною реалізацією та орієнтацією на пацієнта, щоб допомогти EyePoint досягти довгострокового успіху.”
Пан Кемпбелл приносить у EyePoint понад 30 років досвіду комерційного керівництва, за час якого він масштабував глобальні комерційні організації та впроваджував стратегії, орієнтовані на пацієнта, для комерціалізації інноваційних офтальмологічних продуктів.
До приєднання до EyePoint пан Кемпбелл обіймав посаду головного комерційного директора Opthea, де він створив комерційну організацію та керував підготовкою до запуску нового потенційного продукту для лікування wet AMD. Раніше він працював старшим віце-президентом і керівником комерційного підрозділу Viatris Eye Care, де керував комерційним запуском Tyrvaya
Пан Кемпбелл також займав керівні посади у відділах продажів і комерції Genentech, де був ключовим лідером у комерційному запуску Lucentis
Пан Кемпбелл також обіймав різні посади у сфері продажів і комерції в Johnson & Johnson Vision Care, Eli Lilly та AstraZeneca / Medimmune. Він має ступінь бакалавра наук Auburn University та є випускником програми Executive Education Університету Пенсільванії, Wharton School of Business.
Стимулюючі гранти відповідно до Правила лістингу Nasdaq 5635(c)(4)
У зв’язку з наймом пана Кемпбелла Комітет з компенсацій Ради директорів EyePoint надав опціони на купівлю загалом 175 000 акцій звичайних акцій як стимулюючу винагороду, що є матеріальною умовою для вступу пана Кемпбелла на роботу в компанію відповідно до Правила лістингу Nasdaq 5635(c)(4). Опціони на акції мають ціну виконання, що відповідає ціні закриття акцій EyePoint станом на 17 лютого 2026 року, і будуть нараховуватися наступним чином: 25% у першу річницю та щомісячно до четвертої річниці дати надання з урахуванням умов надання.
Про EyePoint
EyePoint, Inc. (Nasdaq: EYPT) — біофармацевтична компанія на клінічній стадії, яка займається розробкою та комерціалізацією інноваційних терапевтичних засобів для покращення життя пацієнтів із серйозними захворюваннями сітківки. Провідний кандидат компанії, DURAVYU
Компанія прагне співпрацювати з офтальмологічною спільнотою для покращення життя пацієнтів і створення довгострокової цінності, маючи чотири схвалені препарати за три десятиліття та десятки тисяч пацієнтів, пролікованих інноваціями EyePoint.
EyePoint має штаб-квартиру в Watertown, Массачусетс, та комерційний виробничий комплекс у Northbridge, Массачусетс.
Vorolanib ліцензовано EyePoint на ексклюзивній основі компанією Equinox Sciences, афілійованою з Betta Pharmaceuticals, для локалізованого лікування всіх офтальмологічних захворювань за межами Китаю, Макао, Гонконгу та Тайваню.
DURAVYU
Заяви щодо перспектив розвитку
EYEPOINT SAFE HARBOR STATEMENTS UNDER THE PRIVATE SECURITIES LITIGATION ACT OF 1995: У тій мірі, в якій будь-які твердження в цьому прес-релізі стосуються інформації, яка не є історичною, це є заяви щодо перспектив розвитку відповідно до Private Securities Litigation Reform Act of 1995. Такі твердження включають, серед іншого, заяви щодо наших очікувань стосовно наших планів клінічного розвитку та регуляторних планів; нашу віру в те, що DURAVYU
Заяви щодо перспектив розвитку за своєю природою стосуються питань, які в різній мірі є невизначеними. Невизначеності та ризики можуть призвести до того, що фактичні результати EyePoint суттєво відрізнятимуться від заявлених або передбачених у заявах щодо перспектив розвитку. Для EyePoint ці ризики та невизначеності включають строки, хід та результати клінічної розробки компанії, включаючи DURAVYU; невизначеності та затримки, пов’язані зі спілкуванням із U.S. Food and Drug Administration та можливістю отримати регуляторне схвалення від FDA для комерціалізації DURAVYU; непередбачувані витрати; можливість того, що наявні грошові кошти та їх еквіваленти не будуть достатніми для підтримки операційного плану так довго, як очікувалося; ризик того, що результати клінічних досліджень можуть не бути прогностичними для майбутніх результатів, а проміжні та попередні дані підлягають подальшому аналізу та можуть змінюватися з надходженням додаткових даних; несподівані дані з безпеки або ефективності, отримані під час клінічних досліджень; невизначеності, пов’язані з процесом регуляторного дозволу чи схвалення, і доступними шляхами для затвердження кандидатів на продукти компанії; зміни в регуляторному середовищі; збої в роботі FDA, включаючи скорочення штату FDA та/або недостатнє фінансування FDA; зміни в політиці торгівлі США та міжнародній торгівлі; зміни в очікуваній чи існуючій конкуренції; успіх поточних і майбутніх ліцензійних угод; нашу залежність від контрактних дослідницьких організацій, інших зовнішніх постачальників і сервісних компаній; відповідальність за продукт; вплив загальних ділових та економічних умов; захист нашої інтелектуальної власності та уникнення порушення інтелектуальної власності; збереження ключового персоналу; затримки, перебої або збої у виробництві та постачанні кандидатів на продукти; доступність і необхідність додаткового фінансування; нашу здатність отримати додаткове фінансування для підтримки програм клінічного розвитку; невизначеності щодо строків і результатів субпоени серпня 2022 від U.S. Attorney’s Office for the District of Massachusetts; невизначеності щодо попереджувального листа FDA, що стосується виробничого комплексу компанії у Watertown, MA; та інші фактори, описані у наших поданнях до Securities and Exchange Commission. Ми не можемо гарантувати, що результати й інші очікування, виражені, передбачені або імпліцитно зазначені в будь-якій заяві щодо перспектив розвитку, будуть досягнуті. Різноманітні фактори, включаючи ці ризики, можуть призвести до того, що наші фактичні результати та інші очікування суттєво відрізнятимуться від прогнозованих чи інших очікувань, виражених, передбачених або імпліцитно зазначених у заявах щодо перспектив розвитку. Якщо відомі або невідомі ризики матеріалізуються, або якщо основоположні припущення виявляться неточними, фактичні результати можуть суттєво відрізнятися від попередніх результатів і тих, що передбачаються, оцінюються чи прогнозуються у заявах щодо перспектив розвитку. Вам слід враховувати це під час розгляду будь-яких заяв щодо перспектив розвитку. Більш повну інформацію про ризики та невизначеності, які можуть призвести до того, що наші фактичні результати суттєво відрізнятимуться від виражених або імпліцитно зазначених у заявах щодо перспектив розвитку в цьому прес-релізі, наведено в розділі "Фактори ризику" в нашому останньому річному звіті на Form 10-K, в інших наших поданнях до Securities and Exchange Commission (SEC) та в наших майбутніх звітах, які подаватимуться до SEC, що доступні за адресою . Наші заяви щодо перспектив розвитку є дійсними тільки на дату їх публікації. EyePoint не бере на себе зобов’язання оновлювати або переглядати жодну заяву щодо перспектив розвитку, незалежно від того, чи це пов’язано з надходженням нової інформації, майбутніми подіями чи з інших причин.
Відмова від відповідальності: зміст цієї статті відображає виключно думку автора і не представляє платформу в будь-якій якості. Ця стаття не повинна бути орієнтиром під час прийняття інвестиційних рішень.
Вас також може зацікавити
Google нещодавно надала Сундару Пічаї компенсаційний пакет на суму $692 мільйони

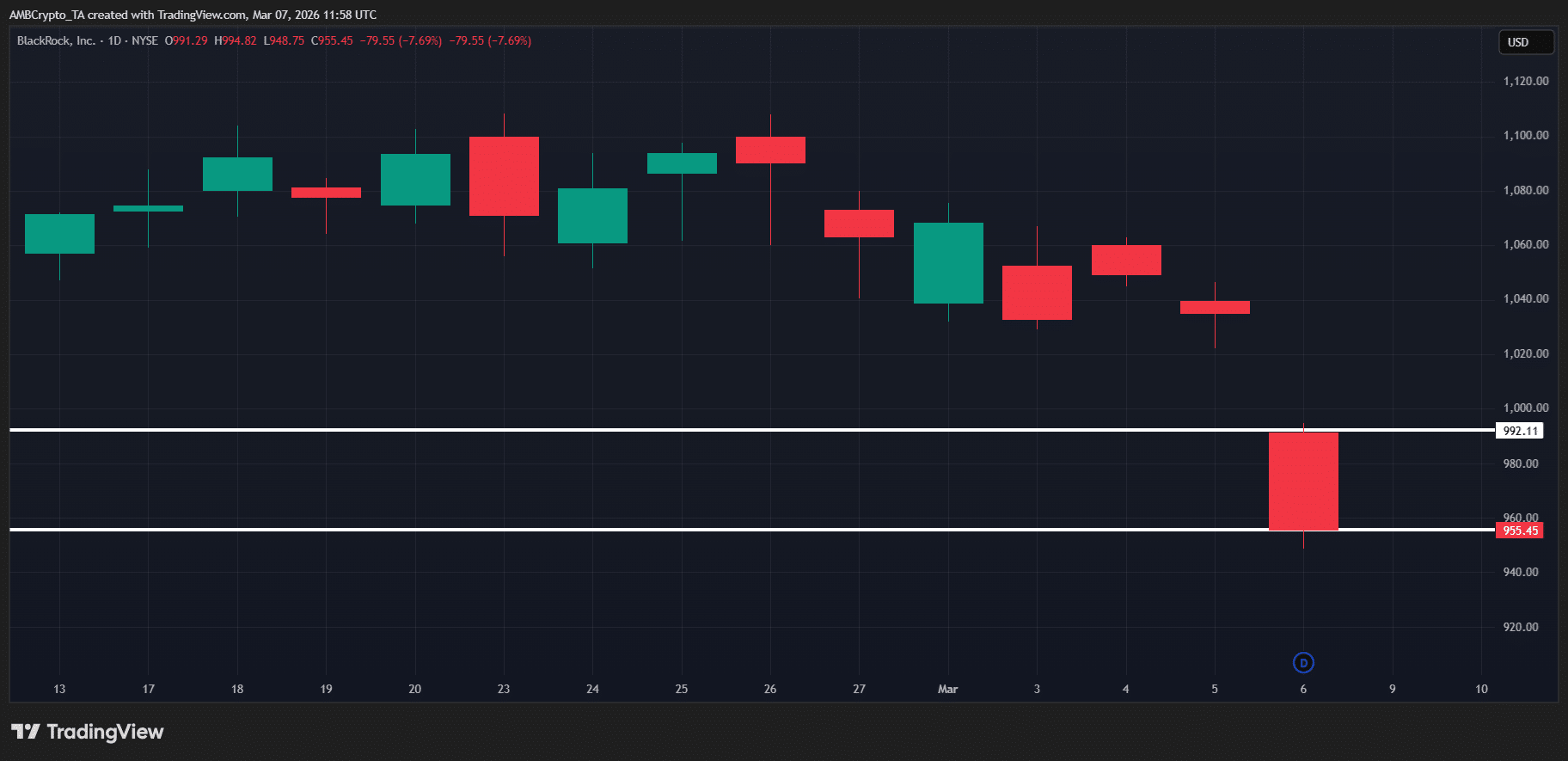
Попередження про ліквідність у $1,2 млрд – як BlackRock може «сколихнути» крипторинок
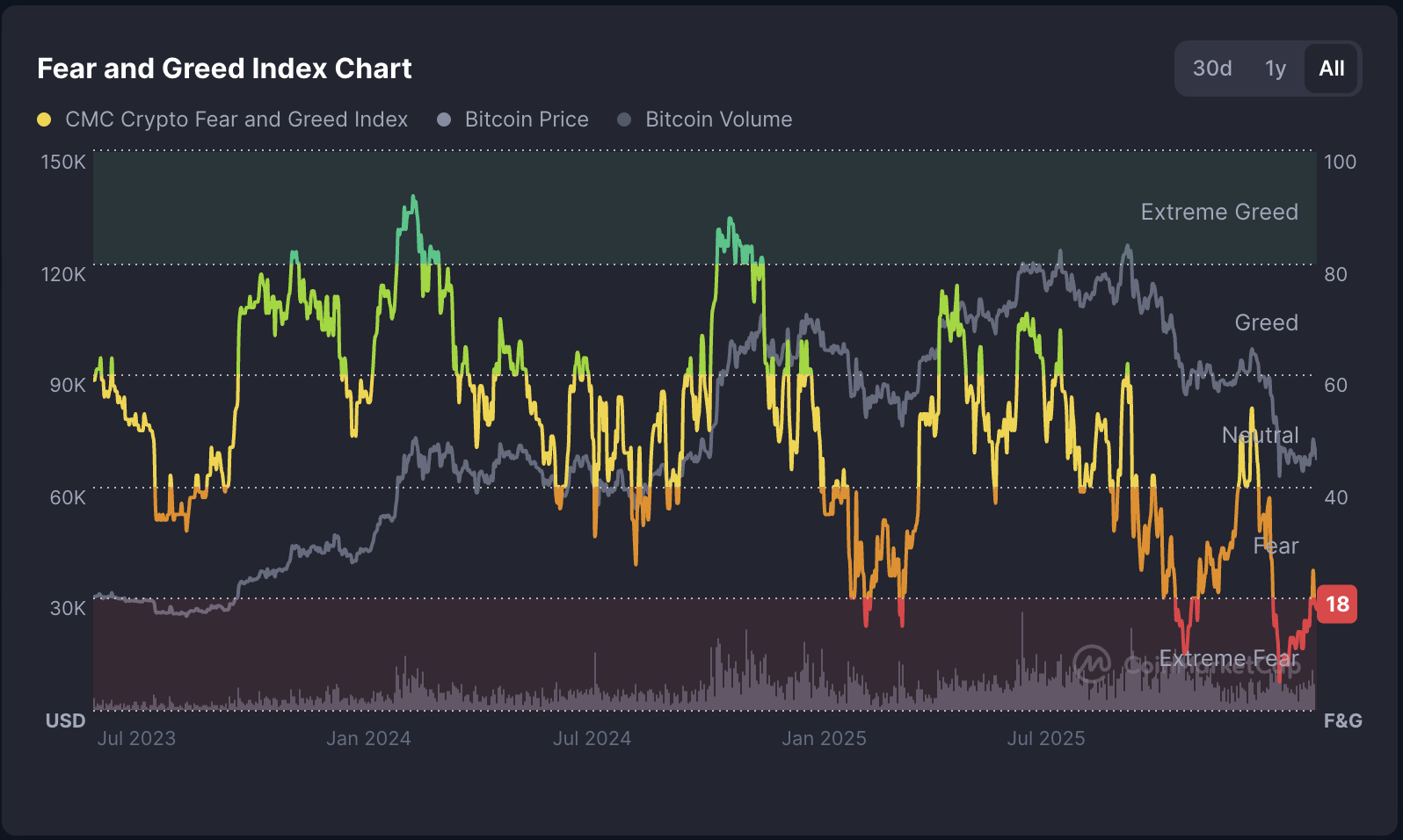
Індекс страху та жадібності криптовалют повертається до рівня «екстремального страху»
Оцінка, чи перебуває підтримка Zcash на рівні $200 під загрозою після падіння ZEC на 8%