Naglabas ang Clene ng Liham sa mga Stockholder na Binibigyang-diin ang mga Paparating na Catalyst ng CNM-Au8 sa 2026
- Sapat ang operating capital runway hanggang ika-apat na quarter ng 2026
- Isang personal na Type C FDA meeting ang naka-iskedyul bago matapos ang unang quarter ng 2026 upang talakayin ang pinakabagong CNM-Au8 data na isinumite noong huling bahagi ng 2025
- Inaasahang pagsusumite ng New Drug Application (NDA) sa FDA para sa CNM-Au8 sa pamamagitan ng isang pinabilis na regulatory pathway sa ikalawang quarter ng 2026
- Posibilidad ng pagtanggap ng FDA sa NDA na ito at paglalabas ng Prescription Drug User Fee Act (PDUFA) date sa ikalawang kalahati ng 2026
SALT LAKE CITY, Peb. 24, 2026 (GLOBE NEWSWIRE) -- Ang Clene Inc. (Nasdaq: CLNN) (kasama ang mga subsidiary nito, “Clene” o ang “Kumpanya”) at ang buong pag-aari nitong subsidiary na Clene Nanomedicine Inc., isang clinical-stage biopharmaceutical company na nakatuon sa pagpapabuti ng mitochondrial health at pagprotekta ng neuronal function upang gamutin ang mga neurodegenerative na sakit, kabilang ang amyotrophic lateral sclerosis (ALS) at multiple sclerosis (MS), ay naglabas ngayon ng liham sa mga stockholder na naglalahad ng mga pangunahing inaasahang regulatory at clinical milestones para sa CNM-Au8
Liham ng CEO para sa mga Stockholder
Habang aming tinitingnan ang darating na taon, nais kong ipahayag ang taos-pusong pasasalamat sa inyong patuloy na suporta sa Clene. Bilang founding CEO na may higit 12 taon sa pamumuno, ako ay pinapatnubayan ng misyon ng Clene na bumuo ng makabuluhan at ligtas na mga lunas para sa mga neurodegenerative na sakit, lalo na sa aming pokus sa ALS.
Matapos makumpleto ang ilang Phase 2 clinical trials at patuloy na suporta ng open label expanded access programs, nakapagbigay kami ng paggamot sa higit 800 pasyente gamit ang CNM-Au8, ang aming orally administered nanocrystal suspension, na bumubuo ng isa sa pinakamalalaking clinical experience sa ALS. Ang mga natutunan at datos na aming natuklasan ay naglalagay sa amin sa isang kapanapanabik at kritikal na yugto.
Sapat na pondo upang tustusan ang operasyon hanggang ika-apat na quarter ng 2026
Noong Enero, natapos namin ang isang oversubscribed registered direct offering na higit $28 milyon. Ang paunang tranche na higit $6 milyon ay inaasahang magbibigay ng operating runway hanggang ika-apat na quarter ng 2026, sapat upang pondohan hanggang sa potensyal na NDA acceptance decision ng FDA. Dalawang posibleng karagdagang financing tranches na kabuuang higit $22 milyon ay nakaayos upang tumugma sa NDA acceptance at FDA approval milestones at inaasahang magbibigay ng sapat na kapital sa Kumpanya hanggang 2027. Lubos kaming nagpapasalamat sa suporta ng aming mga investor na may matibay na paniniwala sa halaga ng aming mga programa.
Susunod na Regulatory Steps at mga Catalyst sa 2026
Mula noong huling bahagi ng 2024, kami ay malapit na nakipag-ugnayan nang maraming beses sa neurology division ng FDA ukol sa CNM-Au8. Ang aming mga talakayan ay nagtapos sa isang personal na Type C FDA meeting na naka-iskedyul bago matapos ang quarter na ito upang talakayin ang datos sa aming malawak na briefing package na isinumite noong huling bahagi ng 2025. Inaasahan naming matatanggap ang FDA minutes mula sa pulong na ito sa simula ng ikalawang quarter, na handa na ang Kumpanya na magsumite ng New Drug Application (NDA) sa FDA para sa CNM-Au8 sa pamamagitan ng pinabilis na regulatory pathway sa ikalawang quarter ng 2026. Ang pagtanggap ng FDA sa NDA na ito at paglalabas ng Prescription Drug User Fee Act (PDUFA) date para sa regulatory decision sa ilalim ng accelerated approval pathway ay maaaring mangyari sa ikalawang kalahati ng 2026, na may potensyal na pag-apruba para sa commercial launch sa 2027.
Batay sa kahalagahan ng aming clinical data at pakikipag-ugnayan sa FDA, naniniwala kami na ang CNM-Au8 ay angkop para sa accelerated approval pathway gaya ng inilalarawan sa ibaba:
1. Pinalawig na Kaligtasan at Kaugnay na Pagbaba ng Biomarkers ng Neurodegeneration:
Nakabuo kami ng malawak na clinical data na nagpapakita ng pinalawig na kaligtasan sa ALS kaugnay ng CNM-Au8 30mg treatment. Kritikal ang survival sa ALS, isang nakamamatay na kondisyon na may median life expectancy na humigit-kumulang 2-4 taon matapos ang diagnosis. Ang CNM-Au8 ay nagdulot ng istatistikal na makabuluhan at clinically meaningful na pagbawas ng panganib ng pagkamatay at nagpabagal ng clinical worsening, bilang pre-specified secondary at/o exploratory endpoints sa clinical trials at tuloy-tuloy na benepisyo sa open label extensions. Ang ebidensyang ito ng pinalawig na survival benefit ng CNM-Au8 treatment ay sinabayan ng istatistikal na makabuluhang pagbaba ng mga ALS-relevant biomarkers, kabilang ang neurofilament light chain (NfL) at glial fibrillary acidic protein (GFAP), mga pangunahing marker ng neuronal at glial cell injury at degeneration, na nagbibigay ng biological na batayan para sa nabawasang panganib ng pagkamatay. Naniniwala kami na ang mga pinagsamang natuklasan na ito sa mga validated biomarkers ng neurodegeneration ay sumusuporta sa NfL bilang viable surrogate endpoint para sa pinabilis na FDA approval ng CNM-Au8. Kapansin-pansin, ang pagbabago sa NfL biomarker ay kamakailan lamang ginamit para sa pinabilis na approval ng FDA ng isa pang ALS na gamot, at naniniwala kami na ang datos na ito ay tutugon sa mga kahilingan ng ahensya na iugnay ang NfL reductions sa clinical benefit. Sa huli, nagbigay din ang Clene ng supporting evidence upang tugunan ang iminungkahing balangkas ng FDA para sa posibleng accelerated approval consideration gaya ng inilarawan sa aming nakaraang FDA meeting minutes na aming naipahayag sa publiko.
2. Kanais-nais na Safety at Benefit/Risk Profile:
Ang groundbreaking na clean-surfaced nanotherapeutic suspension ng CNM-Au8, isang oral liquid na iniinom ng mga pasyente araw-araw at may lasa ng tubig, ay nagpakita ng consistent na safety at tolerability profile. Sa lahat ng aming clinical trial at expanded access programs, na umaabot na ngayon sa higit 1,000 patient years ng paggamot, ang adverse event profile ay tinasa bilang karamihang mild-to-moderate. Bukod pa rito, wala pang CNM-Au8-related Serious Adverse Events (SAEs), at walang safety signals na naugnay sa pangmatagalang paggamit. Ang benign na tolerability profile na ito ay dapat maging mahalaga sa FDA habang isinaalang-alang ang benefit/risk profile kaugnay ng CNM-Au8 treatment. Higit pa rito, may regulatory precedent sa ALS kung saan ang ibang investigational drugs na may derisked tolerability profile ay nabigyan ng pinabilis na approval batay lamang sa Phase 2 efficacy data.
3. Confirmatory Phase 3 RESTORE-ALS Trial Planong Simulan Mamaya sa 2026:
Upang kumpirmahin ang survival benefit na naobserbahan gamit ang CNM-Au8 30 mg treatment sa ilang Phase 2 trials at upang matugunan ang mga pangangailangan ng FDA para sa pinabilis na approval pathway, plano naming bigyan ng unang dosis ang pasyente sa aming confirmatory Phase 3 RESTORE-ALS trial mamaya ngayong taon. Ang pag-aaral ay magiging isang double-blind, placebo-controlled Phase 3 trial na susuriin ang epekto ng CNM-Au8 sa survival at clinical worsening events sa ALS. Ang disenyo ng trial protocol ay napag-usapan at nasuri na ng FDA.
Ang Aming Paninindigan sa ALS Community ay Nanatiling Matatag:
Ang pagbuo ng CNM-Au8 ay naging lubhang kolaboratibo sa maraming stakeholder na kasangkot. Sa halos isang dekada, kami ay nakipag-ugnayan sa ALS community, kabilang ang mga nangungunang siyentipiko, doktor na nagbibigay ng lunas, mga tagapagtaguyod ng sakit, non-profit na mga organisasyon sa ALS, at daan-daang mga pasyente at kanilang mga tagapag-alaga. Kilala ang CNM-Au8 ng marami sa mga ALS stakeholder na ito. Kilala rin ang CNM-Au8 ng mga regulator sa loob ng FDA, at inaasahan naming maipapakita ang aming matibay na ebidensya na sumusuporta sa CNM-Au8 sa kanila mamaya sa unang quarter ng 2026. Inaasahan naming ang kabuuan ng aming biomarker, survival, at bioanalytic na ebidensya na sumusuporta sa CNM-Au8, kasama ng kanais-nais na tolerability profile ng gamot at ang malaking unmet need sa ALS, ay magiging napaka-kumbinsido sa aming mga darating na talakayan sa FDA para sa konsiderasyon ng pinabilis na approval pathway.
Iba Pang Mapanagutang ‘Pipeline-in-a-Product’ Indikasyon na Uusad sa 2026:
Ipinakita rin ng CNM-Au8 ang mga mapanagutang clinical benefits sa MS at Parkinson’s disease. Sa aming MS program, plano naming ituloy ang momentum ng 2025 habang isinasama ang feedback ng FDA upang tapusin ang disenyo ng aming Phase 3 clinical trial na nakatuon sa cognition sa MS bilang dagdag sa standard of care therapies. Tinitingnan namin ang CNM-Au8 bilang isang potensyal na “pipeline in a product”, na ang paunang ALS indication ang magsisilbing pundasyon para sa mas malawak na clinical development pipeline sa loob ng neurodegenerative field.
Maraming salamat sa inyong pakikiisa sa paglalakbay na ito.
Lubos na gumagalang,
Rob Etherington, Pangulo at CEO, Clene, Inc.
Tungkol sa Clene
Ang Clene Inc. (Nasdaq: CLNN), kasama ang mga subsidiary nito, “Clene” at ang buong pag-aari nitong subsidiary na Clene Nanomedicine, Inc., ay isang late clinical-stage biopharmaceutical company na nakatuon sa pagpapabuti ng mitochondrial health at pagprotekta ng neuronal function upang gamutin ang mga neurodegenerative na sakit, kabilang ang amyotrophic lateral sclerosis, Parkinson’s disease, at multiple sclerosis. Ang CNM-Au8
Tungkol sa CNM-Au8
Ang CNM-Au8 ay isang oral suspension ng gold nanocrystals na binuo upang ibalik ang kalusugan at function ng neuron sa pamamagitan ng pagtaas ng energy production at utilization. Ang catalytically active nanocrystals ng CNM-Au8 ay nagpapasigla ng mahahalagang cellular energy producing reactions na nagbibigay-daan sa neuroprotection at remyelination sa pamamagitan ng pagtaas ng neuronal at glial resilience sa disease-relevant stressors. Ang CNM-Au8
Disclaimer: Ang nilalaman ng artikulong ito ay sumasalamin lamang sa opinyon ng author at hindi kumakatawan sa platform sa anumang kapasidad. Ang artikulong ito ay hindi nilayon na magsilbi bilang isang sanggunian para sa paggawa ng mga desisyon sa investment.
Baka magustuhan mo rin
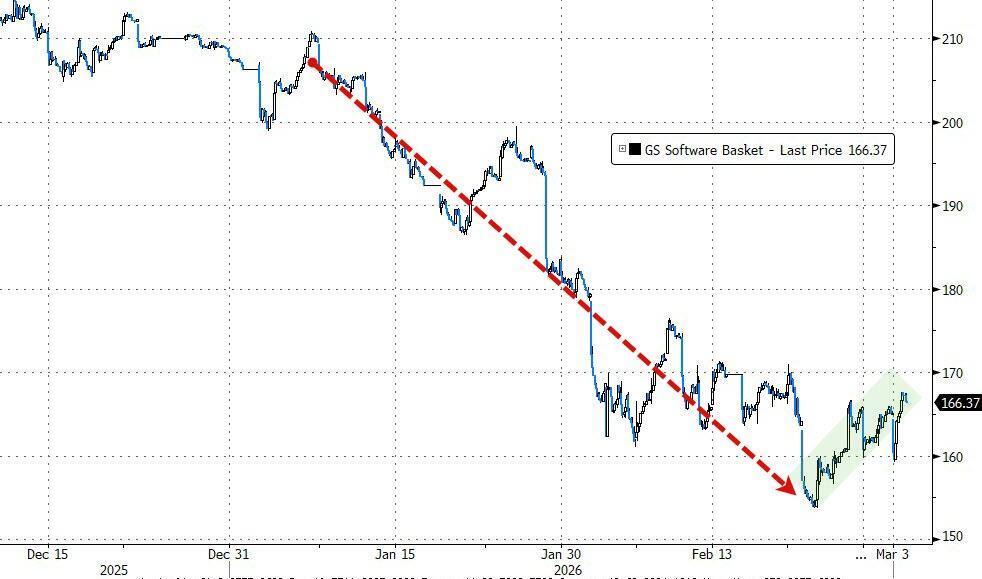
Ang mga pandaigdigang pondo ay nagmamadaling bumili ng dolyar para sa kaligtasan!


