Cue Biopharma оголошує доклінічні дані щодо безпеки та переносимості CUE-401 для лікування аутоімунних та запальних захворювань
У двох не GLP-дослідженнях CUE-401 добре переносився, не було виявлено жодних побічних явищ
Дослідження proof-of-concept підкріплюють багатообіцяючий доклінічний профіль і терапевтичний потенціал CUE-401
BOSTON, Массачусетс, 17 лютого 2026 (GLOBE NEWSWIRE) -- Cue Biopharma, Inc. (Nasdaq: CUE), клінічна біофармацевтична компанія, яка розробляє новий клас терапевтичних біологічних препаратів для вибіркової взаємодії та модуляції Т-клітин, специфічних до захворювань, з метою лікування аутоімунних та запальних захворювань, сьогодні оголосила доклінічні дані про безпеку та переносимість, які додатково підтверджують доклінічний профіль CUE-401, провідного активу компанії в галузі аутоімунних захворювань.
«Ми дуже задоволені цими доклінічними даними, які показали, що CUE-401 добре переносився і не було виявлено жодних побічних явищ», — сказав Усман Азам, M.D., президент і генеральний директор Cue Biopharma. «Дані, отримані з цих доклінічних досліджень, є важливим доповненням до зростаючих доказів, що підтверджують потенціал CUE-401 як першого в своєму класі біфункціонального толерогенного агента для лікування аутоімунних захворювань. Ми з нетерпінням очікуємо поділитися подальшими науковими даними і деталями щодо запланованої подачі заявки на проведення клінічних досліджень (IND) для CUE-401 у найближчі місяці».
Дизайн дослідження та основні результати:
Два окремі не GLP-дослідження на мишах і приматах (NHPs) оцінювали безпеку та переносимість CUE-401 із використанням ступінчастої схеми дозування, коли тварини послідовно отримували вищі дози CUE-401 щотижня. CUE-401 вводився внутрішньовенно.
Дослідження на мишах (n=24, 12 самців, 12 самок)
- Тварини отримували зростаючі дози CUE-401: 1 мг/кг, 3 мг/кг та 10 мг/кг
- Усі рівні доз добре переносилися, побічних явищ не було виявлено
Дослідження на NHP (n=6, 3 самці, 3 самки)
- Основне дослідження: Тварини отримували зростаючі дози CUE-401: 0,1 мг/кг, 0,3 мг/кг та 1 мг/кг
- Усі рівні доз добре переносилися в основному дослідженні, не було виявлено жодних побічних спостережень
- Подальше дозування: Після підтвердження переносимості та безпеки в основному дослідженні тваринам було введено додаткову дозу CUE-401 через тиждень у дозі 1 мг/кг (n=2 тварини, 1 самка, 1 самець) або 3 мг/кг (n=4 тварини, 2 самці, 2 самки)
- Повторне введення CUE-401 у дозі 1 мг/кг переносилося краще, ніж повторне введення у дозі 3 мг/кг
Про CUE-401
CUE-401 — це новий біфункціональний терапевтичний агент, який містить інноваційний фрагмент "дихальної маски" TGF-beta разом із клінічно валідаваним мутеїном інтерлейкіну 2 (IL-2) від Cue Biopharma в одному ін'єкційному біопрепараті. Дизайн CUE-401 був натхненний Нобелівською премією 2025 року за роль IL-2 та TGF-beta як ключових елементів у формуванні імунної толерантності шляхом регуляції сигналізації FOXP3. CUE-401 створений для сприяння імунній регуляції та толерантності за допомогою трьох взаємодоповнюючих механізмів: 1. Пряма регуляція прозапальних механізмів через TGF-beta; 2. Розширення вже існуючих Treg через IL-2; 3. Перетворення FOXP3- звичайних CD4+ T-клітин у FOXP3+ індуковані Treg через скоординоване забезпечення сигналами TGF-beta та IL-2, які обидва необхідні для de novo індукції експресії FOXP3.
Про Cue Biopharma
Cue Biopharma, клінічна біофармацевтична компанія, розробляє новий клас ін'єкційних біопрепаратів для вибіркової взаємодії та модуляції Т-клітин, специфічних до захворювань, безпосередньо в організмі пацієнта. Власна платформа компанії Immuno-STAT™ (Selective Targeting and Alteration of T cells) та біологічні препарати покликані використати лікувальний потенціал власної імунної системи організму без побічних ефектів широкої системної імунної модуляції. CUE-401, провідний актив компанії в галузі аутоімунних захворювань, розроблений для механістичної дії як регулятор прозапальних механізмів та як головний перемикач для диференціації регуляторних Т-клітин (Treg) з метою індукції толерантності. Це високотехнологічна, толерогенна біфункціональна молекула, що поєднує фрагмент "дихальної маски" TGF-beta з клінічно валідаваним мутеїном інтерлейкіну 2 (IL-2) від Cue Biopharma в одному ін'єкційному біопрепараті.
Штаб-квартира знаходиться у Бостоні, Массачусетс, нами керує досвідчена управлінська команда з глибокою експертизою в імунології та білковій інженерії, а також у розробці та клінічному впровадженні білкових біопрепаратів.
Відмова від відповідальності: зміст цієї статті відображає виключно думку автора і не представляє платформу в будь-якій якості. Ця стаття не повинна бути орієнтиром під час прийняття інвестиційних рішень.
Вас також може зацікавити
BlackRock під тиском: фінансовий гігант обмежує зняття коштів

Ripple: Ми використовуємо XRP для забезпечення ліквідності платіжних потоків
Утворюється «bull trap» на Bitcoin, оскільки ведмежий ринок переходить у середню фазу: Віллі Ву
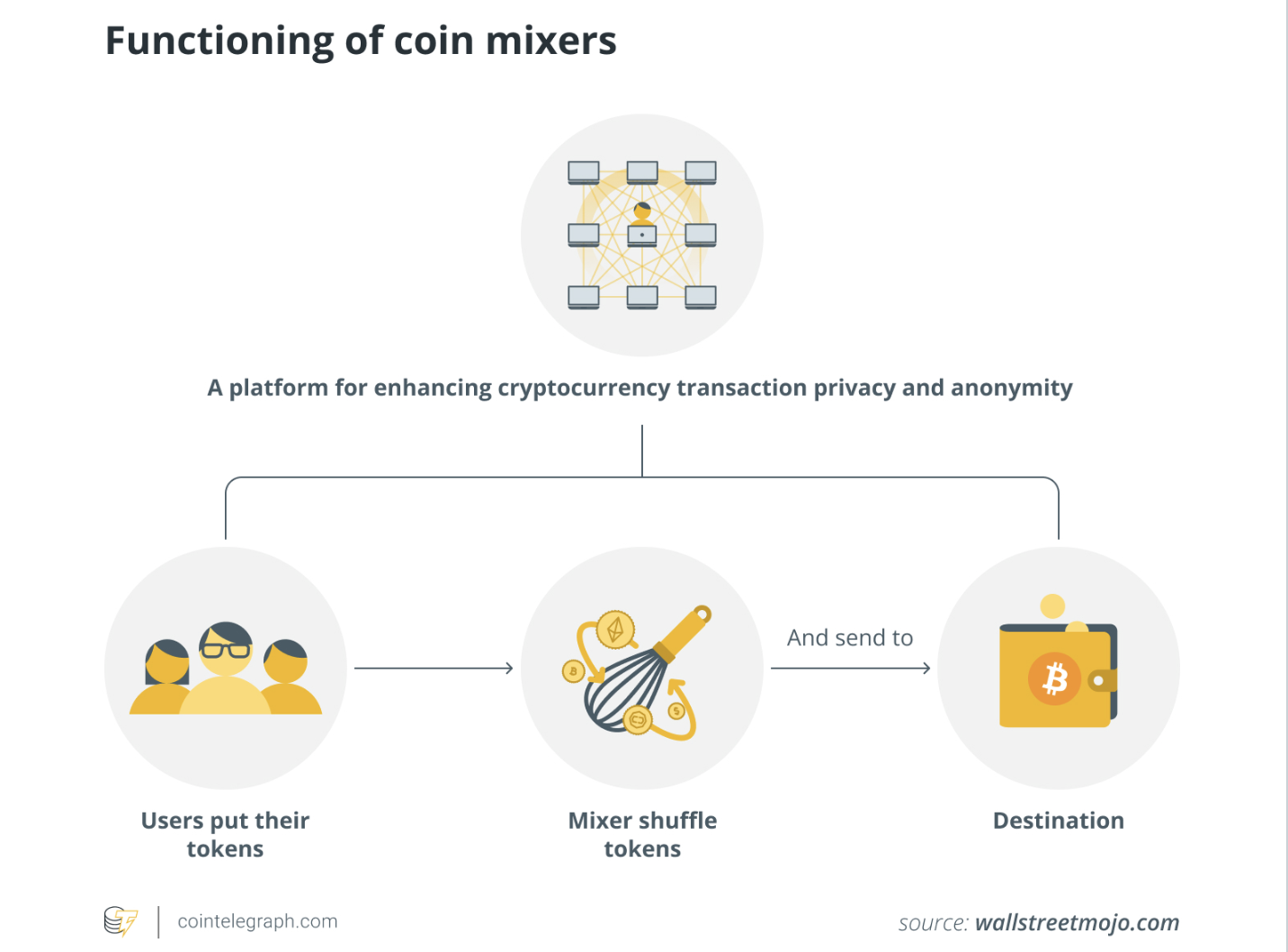
Звіт Міністерства фінансів США визнає легітимне використання криптоміксерів